Cho 1,03g muối natri halogen ( NaX ) tác dụng với dung dịch Agno3 dư thì thu được một kết tủa, kết tủa này sau khi phân hủy hoàn toàn cho 1,08g bạc. X là

Những câu hỏi liên quan
Cho 1,03 gam muối natri halogen (NaX) tác dụng hết với dung dịch AgNO3 dư thì thu được một kết tủa, kết tủa này sau phản ứng phân hủy hoàn toàn cho 1,08 gam Ag. X là :
A. brom
B. flo
C. clo
D. iot
Đáp án A
nAg = 0,01 (mol)
NaX + AgNO3 →AgX + NaNO3
0,01 ← 0,01 (mol)
AgX →Ag
0,01 ← 0,01 (mol)
![]() , MX =80 (Br)
, MX =80 (Br)
Đúng 0
Bình luận (0)
Cho 3,09 gam muối natri halogenua (X) tác dụng với dung dịch
A
g
N
O
3
dư thì thu được một kết tủa, kết tủa này sau khi phân hủy hoàn toàn cho 3,24 gam bạc. Công thức của muối X là A. NaF B. NaBr C. NaI D. NaCl
Đọc tiếp
Cho 3,09 gam muối natri halogenua (X) tác dụng với dung dịch A g N O 3 dư thì thu được một kết tủa, kết tủa này sau khi phân hủy hoàn toàn cho 3,24 gam bạc. Công thức của muối X là
A. NaF
B. NaBr
C. NaI
D. NaCl
Chọn đáp án B
NaY + A g N O 3 → A g N O 3 + AgY
2AgY → 2Ag + Y 2
n N a Y = n A g Y = n A g = = 0,03 (mol
0,03(23+ M Y ) = 3,09 => M Y = 80 (Br)
Đúng 0
Bình luận (0)
Cho 1,03 gam muối natri halogenua (X) tác dụng với dung dịch
A
g
N
O
3
dư thì thu được một kết tủa, kết tủa này sau khi phân hủy hoàn toàn cho 1,08 gam bạc. Công thức của muối X là A. NaF B. NaBr C. NaI D. NaCl
Đọc tiếp
Cho 1,03 gam muối natri halogenua (X) tác dụng với dung dịch A g N O 3 dư thì thu được một kết tủa, kết tủa này sau khi phân hủy hoàn toàn cho 1,08 gam bạc. Công thức của muối X là
A. NaF
B. NaBr
C. NaI
D. NaCl
Chọn đáp án B
NaY + A g N O 3 → N a N O 3 + AgY
2AgY → 2Ag + Y 2
n N a Y = n A g Y = n A g = = 0,01 (mol)
=> 0,01(23 + M Y ) = 1,03 => M Y = 80 (Br)
Đúng 0
Bình luận (0)
Cho 1,03 gam muối natri halogenua (A) tác dụng với dung dịch AgNO3 dư thì thu được một kết tủa, kết tủa này sau khi phân hủy hoàn toàn cho 1,08 gam bạc. Xác định tên muối A.
nAg = 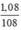 = 0,01 mol
= 0,01 mol
Phương trình hóa học của phản ứng:
Đặt X là kí hiệu, nguyên tử khối của halogen
NaX + AgNO3 → AgX↓ + NaNO3
0,01mol 0,01mol
2AgX → 2 Ag + X2
0,01mol 0,01mol
Theo pt: nNaX = nAgX = nAg = 0,1 mol
MNaX = 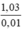 = 103 → X = 103 – 23 = 80 (Br)
= 103 → X = 103 – 23 = 80 (Br)
Muối A có công thức phân tử là NaBr
Đúng 0
Bình luận (0)
Cho 0,515 gam muối natri halogenua (A) tác dụng với dung dịch A g N O 3 dư thu được một kết tủa, kết tủa này sau khi phân hủy hoàn toàn cho 0,54 gam Ag. Muối A là
A. NaF.
B. NaCl.
C. NaBr.
D. NaI.
cho 1,03 gam muối natri halogenua (A) tác dụng với dung dịch AgNO3 dư thì thu được 1 kết tủa , kết tủa này sau khi phân hủy hoàn toàn cho 1,08 gam bạc . Xác định tên của muối A .
nAg=0,01 mol
NaX+AgN03------->NaN03+AgX,áp dụng bảo toàn nguyên tố Ag,nAg sau=nAg truoc
0,01--------------------------------0,01
MNaX=1,03/0,01=103------------------->X=80------->Br
Đúng 0
Bình luận (0)
từ đâu bạn lại suy ra nAg là 0,01 mol và nAg sau lại bằng nAg trước
Đúng 0
Bình luận (0)
Xem thêm câu trả lời
cho 1,03g muối natri halogen (NaX) tác dụng hết vs dd AgNO3 dư thì thu được 1 kết tủa, kết tủa này sau phản ứng phân hủy hoàn toàn cho 1,08g Ag. X là
cho 1,03g muối natri halogen (NaX) td hết với dd AgNO3 dư thì thu đc một kết tủa, kết tủa này sau pư phân hủy hoàn toàn cho 1,08g Ag. X là?
sục khí clo dư vào dd chứa hai muối NaBr và KBr thu đc 2 muối NaCl và KCl, đồng thời thấy khối lượng muối giảm 4,45g. Lượng clo đã tham gia pư với 2 muối trên là bao nhiêu mol?
Giúp nhanh nha
nAg = 0,01 (mol)
NaX + AgNO3 →AgX + NaNO3
0,01 ← 0,01 (mol)
AgX →Ag
0,01 ← 0,01 (mol)
, MX =80 (Br)
bài 2
x mol ion Br sẽ bị thay thế bởi x mol ion Cl
1/ \(NaX+AgNO_3\rightarrow AgX+NaNO_3\)
\(2AgX\rightarrow2Ag+X_2\)
\(n_{Ag}=\frac{1,08}{108}=0,01mol\)
\(n_{Ag}=n_{AgX}=n_{NaX}=0,01mol\)
Mà \(m_{NaX}=1,03g\)
\(\rightarrow M_{NaX}=\frac{1,03}{0,01}=103\)
\(\rightarrow23+X=103\rightarrow X=80\)
Vậy X là Br
Cho 0,03 mol hỗn hợp NaX và NaY ( X, Y là hai halogen thuộc chu kì kế tiếp – đều tạo kết tủa với AgNO3) tác dụng với lượng dư dung dịch AgNO3 thu được 4,75 gam kết tủa. Công thức hai muối trên là A. NaBr, NaI B. NaF, NaCl C. NaCl, NaBr D. NaF, NaCl hoặc NaBr, NaI
Đọc tiếp
Cho 0,03 mol hỗn hợp NaX và NaY ( X, Y là hai halogen thuộc chu kì kế tiếp – đều tạo kết tủa với AgNO3) tác dụng với lượng dư dung dịch AgNO3 thu được 4,75 gam kết tủa. Công thức hai muối trên là
A. NaBr, NaI
B. NaF, NaCl
C. NaCl, NaBr
D. NaF, NaCl hoặc NaBr, NaI
Đáp án C
Gọi công thức chung của NaX và NaY là NaM.
NaM + AgNO3 → AgM↓+NaNO3
0,03 →0,03 (mol)
![]()
=> M = 50,3 => X,Y lần lượt là Cl và Br
Đúng 0
Bình luận (0)












