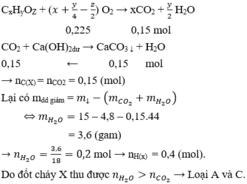Ai giúp em với :((
Đốt cháy hoàn toàn một hidrocacbon A khối lượng là m (gam) thu được 9m/13(gam)H. Biết rằng tỉ khối hơi của A so với không khí nhỏ hơn 1,79.Công thức phân tử của A là
A.C2H2 B.C2H4 C.C3H4 D. C3H6
Đốt cháy hoàn toàn 3,2 gam hidrocacbon A trong không khí thu được 8,8 gam \(CO_2\) và hơi nước. Tìm công thức phân tử của A, biết tỉ khối của A so với khí oxi bằng 0,5.
Gọi CTHH là \(C_xH_y\)
\(n_{CO_2}=\dfrac{8,8}{44}=0,2mol\Rightarrow m_C=2,4g\)
\(d_A\)/O2=0,5\(\Rightarrow M_A=0,5\cdot32=16đvC\)
\(n_A=\dfrac{3,2}{16}=0,2mol\)
\(\overline{C}=\dfrac{n_{CO_2}}{n_A}=\dfrac{0,2}{0,2}=1\)
Vậy A là \(CH_4\).
Đun hỗn hợp gồm ancol A và axit B (đều là chất có cấu tạo mạch hở, không phân nhánh) thu được este X. Đốt cháy hoàn toàn m gam X thu được 1,344 lít khí CO2 (đktc) và 0,72 gam nước. Lượng oxi cần dùng là 1,344 lít (đktc). Biết tỉ khối hơi của X so với không khí nhỏ hơn 6. Công thức phân tử của X là:
A. C3H4O2
B. C6H8O4
C. C3H2O2
D. Đáp án khác
Đốt cháy hoàn toàn m gam hỗn hợp chất hữu cơ A chỉ thu được a gam CO2 và b gam H2O. Biết 11b = 3a và 7m = 3(a+b). Mặt khác ta có tỉ khối hơi của chất A đối với không khí nhỏ hơn 3. Công thức phân tử của chất hữu cơ A là:
A. C3H8
B. C2H6
C. C3H4O2
D. C3H6O2
Đáp án C
Vì đốt cháy A thu được CO2 và H2O nên A chứa C, H, có thể có O.
Khi đó gọi công thức phân tử của A là CxHyOz
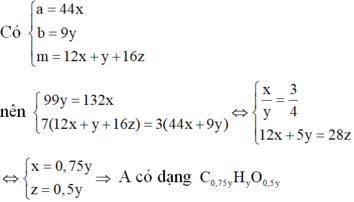
![]()
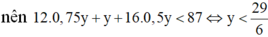
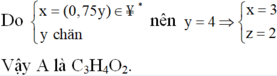
Nhận xét: Khi làm đến bước x : y = 3 :4 và kết hợp với quan sát 4 đáp án, ta có thể kết luận ngay A là C3H4O2.
Đốt cháy hoàn toàn 1,88 gam chất hữu cơ A (chứa C, H, O) cần 1,904 lít O2 (đktc) thu được CO2 và hơi nước theo tỉ lệ thể tích 4:3. Hãy xác định công thức phân tử của A. Biết tỉ khối của A so với không khí nhỏ hơn 7.
A. C8H12O5.
B. C4H8O2.
C. C8H42O3.
D. C6H12O6.
Thông thường khi đề bài cho số mol O2 cần để đốt cháy thì chắc chắn ta sẽ phải sử dụng hoặc định luật bảo khối lượng, hoặc bảo toàn nguyên tố Oxi.
Quay trở lại bài toán này, ta thấy đề cho cần dùng 1,904 lít O2, không cho khối lượng CO2 và H2O mà chỉ cho tỉ lệ thể tích (tỉ lệ số mol), do đó nhận ra được nếu ta sử dụng phương pháp bảo toàn khối lượng ta sẽ tính được số mol CO2 và số mol H2O, từ đó tính được số mol O trong A. Tiếp theo đó ta sẽ xác định công thức đơn giản nhất để tìm ra công thức phân tử.
Có: n O 2 = 1 , 904 22 , 4 = 0 , 085 ( m o l ) ⇒ m O 2 = 0 , 085 . 32 = 2 , 72 ( g a m )
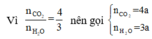
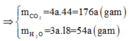
Sơ đồ phản ứng: A + O2 ⇒ CO2 + H2O
Áp dụng định luật bảo toàn khối lượng ta có: m A + m O 2 = m C O 2 + m H 2 O
Hay 1,88 + 2,72 = 176a + 54a ⟺ a = 0,02
⇒ 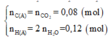
![]()
![]()
Vì C : H : O = nC : nH : nO =0,08 : 0,12 : 0,05 = 8 : 12 : 5
Nên công thức đơn giản nhất của A là C8H12O5.
Khi đó công thức phân tử của A có dạng (C8H12O5)n
Mà MA < 7Mkhôngkhí nên 188n < 7.29 ⇒ n < 1,08 ⇒ n = l
Do đó công thức phân tử của A là C8H12O5.
Đáp án A.
Hỗn hợp M gồm hai chất hữu cơ A và B (phân tử A có nhiều hơn phân tử B một nguyên tử cacbon). Đốt cháy hoàn toàn 12,96 gam hỗn hợp M bằng lượng khí oxi dư thu được sản phẩm cháy gồm H2O và 36,96 gam CO2. Biết tỉ khối hơi của hỗn hợp M so với H2 là 13,5.
a) Tìm công thức phân tử và tính thành phần phần trăm theo khối lượng mỗi chất có trong hỗn hợp M.
b) Khi dẫn toàn bộ sản phẩm cháy vào 552,9 gam dung dịch Ba(OH)2 20,72% thu được m gam chất kết tủa và dung dịch Z. Tìm giá trị của m và tính nồng độ C% của chất tan có trong dung dịch Z
Đốt cháy hoàn toàn một hidrocacbon A thì thu được 4,4 gam khí cacbon đioxit và 2,7 gam nước. Biết khối lượng mol của A là 30 gam. Hãy xác định công thức phân tử của A
giúp mình với mình đâng cần gấp
Đốt cháy hoàn toàn 4,3 g một chất A(phân tử chỉ chứa C,H,O ) thu được sản phẩm cháy gồm 8,8 gam khí cacbônic và 2,7 gam nước. 1) tính phần trăm của các nguyên tố có trong x 2) xác định công thức phân tử của A biết tỉ khối hơi của A so với H2 là 43
1)
\(n_{CO_2}=\dfrac{8,8}{44}=0,2\left(mol\right)\)
\(n_{H_2O}=\dfrac{2,7}{18}=0,15\left(mol\right)\)
Bảo toàn C: nC = 0,2 (mol)
Bảo toàn H: nH = 0,3 (mol)
\(\left\{{}\begin{matrix}\%C=\dfrac{0,2.12}{4,3}.100\%=55,81\%\\\%H=\dfrac{0,3.1}{4,3}=6,97\%\\\%O=100\%-55,81\%-6,97\%=37,22\%\end{matrix}\right.\)
2)
\(n_O=\dfrac{4,3-0,2.12-0,3}{16}=0,1\left(mol\right)\)
nC : nH : nO = 0,2 : 0,3 : 0,1 = 2:3:1
=> CTPT: (C2H3O)n
Mà M = 43.2 = 86 (g/mol)
=> n = 2
=> CTPT: C4H6O2
Đốt cháy hoàn toàn 4,2g Hidrocacbon A thu được 6,72 lít khí CO2 (đktc) và hơi nước. Biết A có tỉ khối Hidro là 21. Xác định công thức phân tử của Hidrocacbon.
Giúp em với ạ :<
Em cảm ơn nhiều :3
Đặt công thức phân tử A là CxHy ( x,y ∈ N*)
nCO2 = 3.13,2/11=3,6(g)
mH = 12x/3,6=y/0,6=42/4,2
=> x=3 , y = 6
=> CTPT : C3H6
\(n_C=\dfrac{6,72}{22,4}=0,3\left(mol\right)\\ n_H=\dfrac{4,2-0,3.12}{1}=0,6\left(mol\right)\)
\(CTPT:C_xH_y\\ \rightarrow x:y=0,3:0,6=1:2\\ \rightarrow\left(CH_2\right)_n=21.2=42\\ \rightarrow n=2\\ CTPT:C_3H_6\)
đặt CTPT của hydrocacbon A là CxHy với (x,y ≠0)
MA =21.2= 42
⇒nA = 4,2/42 = 0,1 (mol)
nCO2 = 6,72/22,4=0,3 (mol)
PT : 2CxHy + (2x - y/2) O2 → 2xCO2 + yH2O
TPT: nCO2 = xnCxHy = 0,1x (mol)
hay 0,3=0,1.x
⇒x = 3
ta có: mA = (12x + y)0,1 = 4,2(g)
hay 12.3 + y =4,2
⇒y = 6
vậy CTPT của hydrocacbon A là C3H6.
Đốt cháy hoàn toàn m gam hợp chất hữu cơ X cần vừa đủ 5,04 lít O 2 (đktc). Hấp thụ sản phẩm cháy vào dung dịch Ca ( OH ) 2 dư, thu được 15 gam kết tủa. Dung dịch còn lại có khối lượng giảm so với khối lượng của dung dịch Ca ( OH ) 2 là 4,8 gam. Tỉ khối hơi của X so với H 2 nhỏ hơn 40. Công thức phân tử của X là
A. C 3 H 4 O 2 .
B. C 3 H 8 O .
C. C 4 H 8 O .
D. C 3 H 8 O 2 .
Chọn B
Theo đáp án, đặt công thức tổng quát của X là CxHyOz