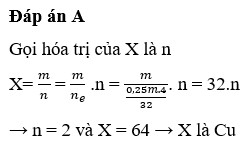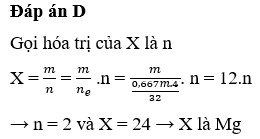Khi oxi hoá 4.8g kim loại M bằng oxi thu được 8g oxit MO. M là kim loại nào sau đây?

Những câu hỏi liên quan
khi oxi hoá 2 gam một kim loại m bằng 0,54 gam khí oxi người ta thu được 4,033 gam oxit trong đó m có hóa trị IV. Hỏi kim loại m là kim loại nào sau đây??
A.Fe(56) B.Mn(55) C.Sn(118.5) D.Pb(207)
\(M+O_2\underrightarrow{t^o}MO_2\)
\(n_{O_2}=\dfrac{0,54}{32}=0,016875\left(mol\right)\)
\(M_M=\dfrac{2}{0,016875}\approx118,5185\left(\dfrac{g}{mol}\right)\)
Sn thỏa mãn vì có hóa trị IV
-> Kim loại cần tìm là Thiếc (Sn)
Đúng 1
Bình luận (0)
Khi oxi hoá 2 gam một kim loại M thu được 2,54 gam oxit, trong đó M có hoá trị IV. Xác định kim loại M.
Để oxi hoá hoàn toàn một kim loại R thành oxit phải dùng một lượng oxi bằng 40% lượng kim loại đã dùng. R là kim loại nào sau đây ?
A. Fe ; B. Al ;
C. Mg ; D. Ca.
Đáp án D.
Gọi nguyên tử khối của kim loại R cũng là R và có hoá trị là x.
4R + x O 2 → 2 R 2 O x
Theo đề bài ta có :
32x/4R = 0,4 → R = 20x
Ta có bảng
| X | I | II | III |
| R | 20 | 40 (nhận) | 60 (loại) |
R là Ca có nguyên tử khối là 40.
Đúng 0
Bình luận (0)
Oxi hóa 1 kim loại R có khối lượng 8g thì thu được 11,2g oxi kim loiaj đó. Tìm kim loại R và và oxit đó
Đặt hóa trị của kim loại R là a
PTHH: 4R + aO2 =(nhiệt)=> 2R2Oa
Áp dụng định luật bảo toàn khối lượng, ta có:
mR + mO2 = mR2Oa
\(\Rightarrow m_{O2}=m_{R2\text{O}a}-m_{\text{R}}=11,2-8=3,2\left(gam\right)\)
\(\Rightarrow n_{O2}=\frac{3,2}{32}=0,1\left(mol\right)\)
Theo PTHH, \(n_{\text{R}}=\frac{0,4}{a}\left(mol\right)\)
\(\Rightarrow M_R=8\div\frac{0,4}{a}=20\text{a}\)
Vì R là kim loại nên a nhận các giá trị 1, 2, 3
Xét chỉ thấy a = 2 là phủ hợp
Khi đó: MR = 40 (g/mol)
\(\Rightarrow\) R là Canxi (Ca)
Đúng 0
Bình luận (6)
Để oxi hóa hoàn toàn một kim loại R thành oxit phải dùng một lượng oxi bằng 40% lượng kim loại đã dùng. R là kim loại nào sau đây? A. Fe B. Al C. Mg D. Ca
Đọc tiếp
Để oxi hóa hoàn toàn một kim loại R thành oxit phải dùng một lượng oxi bằng 40% lượng kim loại đã dùng. R là kim loại nào sau đây?
A. Fe
B. Al
C. Mg
D. Ca
Oxi hoá hoàn toàn m gam kim loại X cần vừa đủ 0,25m gam khí O 2 . X là kim loại nào sau đây
A. Cu
B. Ca
C. Al
D. Fe
Oxi hoá hoàn toàn m gam kim loại X cần vừa đủ 0,667m gam khí O 2 . X là kim loại nào sau đây
A. Zn
B. Ca
C. Al
B. Mg
Oxi hoá 16,2g một kim loại A hóa trị (III) thu được 30,6g oxit. A là kim loại:
(3 Điểm)A.AlB.CrC.AuD.Fe
\(n_A=\dfrac{16,2}{M_A}\left(mol\right)\)
PTHH: 4A + 3O2 --to--> 2A2O3
_____\(\dfrac{16,2}{M_A}\)------------->\(\dfrac{8,1}{M_A}\)
=> \(\dfrac{8,1}{M_A}\left(2M_A+48\right)=30,6=>M_A=27\left(Al\right)\)
Đúng 1
Bình luận (0)
khi khử 10g một oxit kim loại hoá trị 2 bằng khí h2 thu được 8g kim loại xác định tên kim loại đó và thể tích h2(đktc) phải dùng
CTHH: XO
\(n_{XO}=\dfrac{10}{M_X+16}\left(mol\right)\)
\(n_X=\dfrac{8}{M_X}\left(mol\right)\)
PTHH: \(MO+H_2\underrightarrow{t^o}M+H_2O\)
____\(\dfrac{10}{M_X+16}\)-->\(\dfrac{10}{M_X+16}\)________(mol)
=> \(\dfrac{10}{M_X+16}=\dfrac{8}{M_X}\) => MX = 64 (g/mol)
=> Kim loại là Cu
\(n_{CuO}=\dfrac{10}{80}=0,125\left(mol\right)\)
PTHH: \(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
_____0,125-->0,125______________(mol)
=> \(V_{H_2}=0,125.22,4=2,8\left(l\right)\)
Đúng 1
Bình luận (0)
Đặt : CTHH : MO
MO + H2 -to-> M + H2O
M+16________M
10___________8
<=> 8(M+16) = 10M
<=> M = 64
Kim loại là : Cu
nH2 = nCuO = 10/80 = 0.125 (mol)
V H2 = 2.8 (l)
Đúng 0
Bình luận (0)