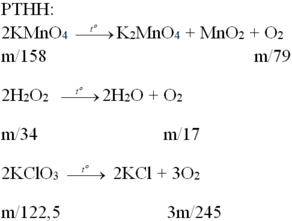
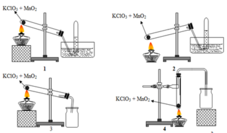
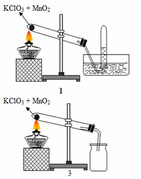
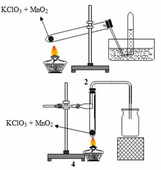
1. ĐIỀU CHẾ OXI TRONG PHÒNG THÍ NGHIỆM
- Khí oxi được điều chế bằng cách phân huỷ các hợp chất giàu oxi nhưng dễ bị phân huỷ ở nhiệt độ cao như KMnO4, KClO3.
2KMnO4 to→to K2MnO4 + MnO2 + O2
2KClO3 to→to 2KCl + 3O2
2. ĐIỀU CHẾ OXI TRONG CÔNG NGHIỆP
- Điện phân nước 2H2O to→to 2H2 + O2
- Chưng cất phân đoạn không khí lỏng.