Cho 16 g hỗn hợp bột Zn và Mg tác dụng với dung dịch HCl dư thấy có 1 gam khí Hiđrô bay ra. Hỏi cái khối lượng muối tạo ra trong dung dịch là bao nhiêu?

Những câu hỏi liên quan
Cho 16 gam hỗn hợp bột Fe và Mg tác dụng với dung dịch HCl dư thấy có 1 gam khí H2 bay ra. Khối lượng muối clorua tạo ra trong dung dịch là bao nhiêu gam?
A. 33,75 gam.
B. 1,5 gam.
C. 87 gam.
D. 51,5 gam
Đáp án D.
Số mol của Hiđro bằng: n H 2 = 1 2 = 0 , 5 ( m o l )
Lại có n C l - ( t r o n g m u ố i ) = 2 n H 2 = 2 . 0 , 5 = 1 ( m o l )
Khối lượng muối tạo thành bằng: 16 + 1. 35,5 = 51,5 (gam).
Đúng 0
Bình luận (0)
cho 20 g hỗn hợp bột Mg và Fe tác dụng với dung dịch HCl dư thấy có 1 g khí H2 bay ra . Khối lượng muối clorua tạo ra trong dung dịch là bao nhiêu gam ?
áp dụng ĐLBT nguyên tố ta có:nH(HCl)=2nH2(bay ra)=1(mol) và nCl(HCl)=nH(HCl)=1(mol).ta có khối lượng muối clorua tạo thành mmuối=mhhKL+mCl(HCl)=20+35.5=55.5(gam)..Chúc bạn học giỏi.
Đúng 0
Bình luận (0)
Cho 20g hỗn hợp bột Mg và Fe tác dụng với dung dịch HCl dư thấy có 1g khí H2 bay ra. Khối lượng muối clorua tạo ra trong dung dịch là bao nhiêu gam?
A. 40,5g.
B. 45,5g.
C. 55,5g.
D. 65,5g.
C đúng
nH2 = 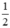 = 0,5 mol.
= 0,5 mol.
Mg + 2HCl → MgCl2 + H2
Fe + 2HCl → FeCl2 + H2
nMg = x; nFe = y.
nH2 = x + y = 0,5 mol.
mhh = 24x + 56y = 20g.
Giải hệ phương trình ta có x = y =0,25 mol.
mMgCl2 = 0, 25 × 95 = 23,75g.
mFeCl2 = 0,25 × 127 = 31,75g
Khối lượng muối clorua = 23,75 + 31,75= 55,5
Đúng 0
Bình luận (0)
Cho 44,5 gam hỗn hợp bột Al và Mg tác dụng với dung dịch HCl dư thấy có 17,92 lít khí H2 bay ra (đktc). Khối lượng muối clorua tạo ra trong dung dịch là
nH2 = 17.92/22.4 = 0.8 (mol)
nHCl = 2nH2 = 1.6 (mol)
BTKL :
mhh + mHCl = mM + mH2
=> 44.5 + 1.6*36.5 = mM + 0.8*2
=> mM = 101.3 (g)
Đúng 0
Bình luận (0)
2 Al + 6 HCl -> 2 AlCl3 + 3 H2
x_____3x______x_____1,5x(mol)
Mg + 2 HCl -> MgCl2 + H2
y__2y________y___y(mol)
Ta có hpt:
\(\left\{{}\begin{matrix}27x+24y=44,5\\22,4.1,5x+22,4y=17,92\end{matrix}\right.\)
Anh nhìn đề sai chắc luôn
Đúng 2
Bình luận (0)
Cho 4,45 gam hỗn hợp bột Zn, Mg tác dụng với dung dịch HCl dư thấy có 2,24 lít khí H2 bay ra (đktc). Khối lượng Zn trong hỗn hợp là:
A. 3,25
B. 4
C. 1,2
D. 1,625
Đáp án A.
Gọi nZn = a , nMg = b (mol)
Zn + 2HCl→ ZnCl2 + H2
a → a (mol)
Mg + 2HCl→ MgCl2 + H2
b b (mol)
Ta có: 65a + 24b = 4,45
a + b = 0,1
Giải ra ta có a = b = 0,05
mZn = 0,05.65 = 3,25 (g)
Đúng 0
Bình luận (0)
CHo 20g hỗn hợp bột Mg và Fe tác dụng với dung dịch HCl dư thấy có 1g H 2 khí H 2 bay ra. Khối lượng muối clorua tạo ra trong dung dịch là
A. 40,5g B. 45,5g
C. 55,5g D. 60,5g
Cho 10,5 gam hỗn hợp bột Mg, Fe tác dụng với dung dịch HCl dư thấy 0,4 gam khí
H
2
bay ra. Khối lượng muối thu được là A. 17,6 gam. B. 25,1 gam. C. 24,7 gam. D. 17,8 gam.
Đọc tiếp
Cho 10,5 gam hỗn hợp bột Mg, Fe tác dụng với dung dịch HCl dư thấy 0,4 gam khí H 2 bay ra. Khối lượng muối thu được là
A. 17,6 gam.
B. 25,1 gam.
C. 24,7 gam.
D. 17,8 gam.
Hòa tan hoàn toàn 15,4 gam hỗn hợp Mg và Zn trong dung dịch HCl dư thấy có 0,6 gam khí H2 bay ra. Khối lượng muối tạo ra trong dung dịch là :
A. 36,7 g.
B. 35,7 g.
C. 63,7 g.
D. 53,7 g.
Số mol H2 là nH2 = 0,6/2 = 0,3(mol)
PTHH : Mg + 2HCl → MgCl2 + H2 ↑ (1)
Zn + 2HCl → ZnCl2 + H2 ↑ (2)
Gọi x, y lần lượt là số mol của Mg và Zn trong dung dịch x, y > 0
nH2 = x + y = 0,3 mol.
mhh = 24x + 65y = 15,4.
Khối lượng muối là m = x(24 + 71) + y(65 + 71)
m = 24x + 65y + 71(x + y) = 15,4 + 71.0,3 = 36,7 (g)
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn 15,4 gam hỗn hợp Mg và Zn trong dung dịch HCl dư thấy có 0,6 gam khí H2 bay ra. Khối lượng muối tạo thành trong dung dịch là: A. 35,7 gam B. 36,7 gam C. 53,7gam D. 63,7 gam
Đọc tiếp
Hòa tan hoàn toàn 15,4 gam hỗn hợp Mg và Zn trong dung dịch HCl dư thấy có 0,6 gam khí H2 bay ra. Khối lượng muối tạo thành trong dung dịch là:
A. 35,7 gam
B. 36,7 gam
C. 53,7gam
D. 63,7 gam
Đáp án D
nCl- = 2nH2 = 2.0,3= 0,6 mol
mMuối = mKL = mCl- = 15,4 + 0,3.96 =36,7 g
Đúng 0
Bình luận (0)










