Trong nước mía có khoảng 20% về khối lượnglà đường có các thành phần các nguyên tố là : 42,11% C, 6,43%H, 51,46%O và có phân tử khối là 342 đvC. Tìm công thức hóa học của hợp chất. Help me !

Những câu hỏi liên quan
Hợp chất X có khối lượng mol phân tử là 342 g/mol, thành phần phần trăm khối lượng của C là 42,11%; của O là 51,46%; còn lại là của H. Công thức hóa học của X là
C12H22O6.
C12H22O11.
C6H10O5.
C6H12O6.
\(m_C=\dfrac{342.42,11\%}{100\%}=144\left(g\right)\)
\(n_C=\dfrac{144}{12}=12\left(mol\right)\)
\(m_O=\dfrac{342.51,46\%}{100\%}=176\left(g\right)\)
\(n_O=\dfrac{176}{16}=11\left(mol\right)\)
\(m_H=342-144-176=22\left(g\right)\)
\(n_H=\dfrac{22}{1}=22\left(mol\right)\)
\(=>CTHH:C_{12}H_{22}O_{11}\)
=> Chọn B
Đúng 4
Bình luận (0)
Gọi CTHH của X là: \(\left(C_xH_yO_z\right)_n\)
Ta có: \(x:y:z=\dfrac{42,11\%}{12}:\dfrac{100\%-51,46\%-42,11\%}{1}:\dfrac{51,46\%}{16}=3,5:6,43:3,2\approx1:2:1\)
Vậy CTHH của X là: \(\left(CH_2O\right)_n\)
Theo đề, ta có: \(M_X=\left(12+1.2+16\right).n=342\left(g\right)\)
\(\Leftrightarrow n=11,4\)
Hình như khối lượng mol sai thì phải
Đúng 3
Bình luận (0)
trong nước mía ép có khoảng 20% về kl một loại đường có tp các nt là : 42,10% C;6,43% H,51,46% O và có ptk là 342 . Xđ ctpt của đường
Số nguyên tử Cacbon = \(\dfrac{342.42,1\%}{12} = 12 \)
Số nguyên tử Hidro = \(\dfrac{342.6,43\%}{1} = 22\)
Số nguyên tử Oxi = \(\dfrac{342.51,46\%}{16} = 11\)
Vậy CTHH của đường : \(C_{12}H_{22}O_{11}\)
Đúng 1
Bình luận (0)
Câu hỏi của bùi tiến long - Toán lớp 8 - Học trực tuyến OLM
Đúng 0
Bình luận (0)
) Tìm công thức hóa học đúng của các hợp chất sau:
a. Hợp chất hữu cơ A có MA bằng 342g/mol biết %mC chiếm 42,11% về khối lượng,% mH=6,43%.
b. Hợp chất B có tỷ khối với không khí là 2,206. Trong đó nguyên tố S chiếm 50% về khối lượng, nguyên tố O chiếm 50% về khối lượng.
\(a,\) Gọi CT đơn giản nhất là \(C_xH_yO_z\)
\(\%m_{O}=100\%-42,11\%-6,43\%=51,46\%\\ x:y:z=\dfrac{\%_C}{12}:\dfrac{\%_H}{1}:\dfrac{\%_O}{12}=3,51:6,43:3,22\\ \Rightarrow x:y:z=12:22:11\\ \Rightarrow \text{CTĐGN của A là }(C_{12}H_{22}O_{11})_n\\ M_A=n.(12.12+22.1+11.16)=342\\ \Rightarrow n=1\\ \Rightarrow CTHH_A:C_{12}H_{22}O_{11}\)
\(b,d_{B/kk}=2,206\\ \Rightarrow M_B=2,206.29\approx 64(g/mol)\\ n_S=\dfrac{64.50\%}{32}=1(mol)\\ n_O=\dfrac{64.50\%}{16}=2(mol)\\ \Rightarrow CTHH_B:SO_2\)
Đúng 1
Bình luận (0)
Hãy tìm các công thức hóa học của những hợp chất có thành phần các nguyên tố như sau: a) Hợp chất A có khối lượng mol phân tử là 102 gam, thành phần các nguyên tố: 52,94% Al và 47,06% O. b) Hợp chất C có khối lượng mol phân tử là 98 gam, thành phần các nguyên tố: 2,04% H; 32,65% S;65,31% O c) Hợp chất X có khối lượng mol phân tử là 212 gam, thành phần các nguyên tố: 55,19% K; 14,62% P; 30,19% O.
Đọc tiếp
Hãy tìm các công thức hóa học của những hợp chất có thành phần các nguyên tố như sau:
a) Hợp chất A có khối lượng mol phân tử là 102 gam, thành phần các nguyên tố: 52,94% Al và 47,06% O.
b) Hợp chất C có khối lượng mol phân tử là 98 gam, thành phần các nguyên tố: 2,04% H; 32,65% S;65,31% O
c) Hợp chất X có khối lượng mol phân tử là 212 gam, thành phần các nguyên tố: 55,19% K; 14,62% P; 30,19% O.
một hỗn hợp chất A gồm các nguyên tố C,H,O trong đó %C=42,11%,,%H=6,43%, %O=51,46%.Tìm ct nguyên tử A, biết MA < 356
Ta có tỉ lệ số nguyên tử:
C:H:O=\(\dfrac{42,11}{12}=\dfrac{6,43}{1}=\dfrac{51,46}{16}\)=3:6:3=1:2:1
Nên ta có: (CH2O)n<356 => 30n<356 => n< 11,87 (n∈N*)
Xét n=11 => (CH2O)11 = C11H22O11 (loại)
...
Xét n=6 => (CH2O)6 = C6H12O6 (nhận)
...
Vậy CT nguyên tử A là C6H12O6
Đúng 1
Bình luận (0)
Hãy tìm công thức hóa học của những hợp chất có thành phần các nguyên tố như sau:
a) Hợp chất A có khối lượng mol phân tử là 58,5g có thành phần các nguyên tố 60,68% Cl và còn lại là Na.
b) Hợp chất B có khối lượng mol phân tử là 106g, thành phần 43,4% Na 11,3% C và 45,3% O.
a) %Cl = 60,68%
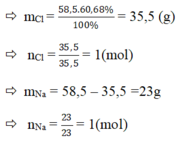
Vậy trong 1 phân tử hợp chất A có : 1 nguyên tử Na, 1 nguyên tử Cl.
⇒ CTHH của hợp chất A : NaCl
b)
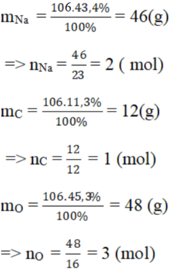
Vậy trong 1 phân tử hợp chất B có: 2 nguyên tử Na, 1 nguyên tử C, 3 nguyên tử O.
⇒ CTHH của hợp chất B : Na2CO3.
Đúng 3
Bình luận (0)
Hãy tìm các công thức hóa học của những hợp chất có thành phần các nguyên tố như sau: a) Hợp chất A có khối lượng mol phân tử là 102 gam, thành phần các nguyên tố: 52,94% Al và 47,06% O.b) Hợp chất C có khối lượng mol phân tử là 98 gam, thành phần các nguyên tố: 2,04% H; 32,65% S;65,31% Oc) Hợp chất X có khối lượng mol phân tử là 212 gam, thành phần các nguyên tố: 55,19% K; 14,62% P; 30,19% O.
Đọc tiếp
Hãy tìm các công thức hóa học của những hợp chất có thành phần các nguyên tố như sau:
a) Hợp chất A có khối lượng mol phân tử là 102 gam, thành phần các nguyên tố: 52,94% Al và 47,06% O.
b) Hợp chất C có khối lượng mol phân tử là 98 gam, thành phần các nguyên tố: 2,04% H; 32,65% S;65,31% O
c) Hợp chất X có khối lượng mol phân tử là 212 gam, thành phần các nguyên tố: 55,19% K; 14,62% P; 30,19% O.
Chất saccarozơ ( đường kính ) là hợp chất phân tử có 12 nguyên tử C , 22 nguyên tử H và 11 nguyên tử O
a, Tìm phân tử khối của hợp chất saccarozơ
b, Tính thành phần ,phần trăm theo khối lượng của các nguyên tố hóa học trong chất saccarozơ
\(CT:C_{12}H_{22}O_{11}\)
\(M=12\cdot12+22+11\cdot16=342\left(đvc\right)\)
\(\%C=\dfrac{12\cdot12}{342}\cdot100\%=42.1\%\)
\(\%H=\dfrac{22}{342}\cdot100\%=6.43\%\)
\(\%O=51.47\%\)
Đúng 2
Bình luận (0)
a)
PTH = 12.12 + 22 + 16.11 = 342(đvC)
b)
$\%C = \dfrac{12.12}{342}.100\% =42,1\%$
$\%H = \dfrac{22}{342}.100\% = 6,43\%$
$\%O = 100\% -42,1\% -6,43\% = 51,47\%$
Đúng 3
Bình luận (0)
Tìm thành phần phần trăm (theo khối lượng) các nguyên tố hóa học có trong những hợp chất sau:a) Fe3O4 và Fe2O3.b) SO2 và SO3.c. Một loại oxit đồng màu đen có khối lượng mol phân tử là 80g. Oxit này có thành phần là 80% Cu và 20% O. Hãy tìm công thức hóa học của loại oxit đồng nói trên.d. Hãy tìm công thức hóa học của khí A.- Khí A nặng hơn khí hiđro 17 lần.- Thành phần theo khối lượng của khí A là 5,88% H và 94,12% S.
Đọc tiếp
Tìm thành phần phần trăm (theo khối lượng) các nguyên tố hóa học có trong những hợp chất sau:
a) Fe3O4 và Fe2O3.
b) SO2 và SO3.
c. Một loại oxit đồng màu đen có khối lượng mol phân tử là 80g. Oxit này có thành phần là 80% Cu và 20% O. Hãy tìm công thức hóa học của loại oxit đồng nói trên.
d. Hãy tìm công thức hóa học của khí A.
- Khí A nặng hơn khí hiđro 17 lần.
- Thành phần theo khối lượng của khí A là 5,88% H và 94,12% S.
a) Với Fe3O4 thì Fe là 72,4% và O là 27,6%;
Với Fe2O3 thì Fe là 70% và O là 30%
b) Với SO2 thì S là 50% và O là 50%
Với SO3 thì S là 40% và O là 60%
c) mCu= \(\dfrac{80.80}{100}\)=64(g) ; mO=\(\dfrac{80.20}{100}\)=16(g)
nCu=\(\dfrac{64}{64}\)=1(mol) ; nO=\(\dfrac{16}{16}\)=1(mol)
Vậy CTHH của oxit đồng màu đen là: CuO
d) dA/H2=\(\dfrac{Ma}{2}\)=17 => MA=2.17=34(đvC)
H =\(\dfrac{5,88.34}{100}\)\(\approx\)2(đvC) ; S =\(\dfrac{94,12.34}{100}\)\(\approx\)32
=> CTHH của chất khí A là SH2
Đúng 0
Bình luận (0)


























