Cho 69,6g MnO2 tác dụng với dung dịch HCl đặc dư với hiệu suất phản ứng là 70% thứ đc V lít khí Cl( đktc). Xác định giá trị của V?

Những câu hỏi liên quan
Cho 8,7 gam MnO2 tác dụng với dung dịch axit HCl đậm đặc sinh ra V lít khí Cl2 (đktc). Hiệu suất phản ứng là 85%. V có giá trị là:
A. 2 lít
B. 2,905 lít
C. 1,904 lít
D. 1,82 lít
Cho 8,7 gam MnO2 tác dụng với dung dịch axit HCl đậm đặc sinh ra V lít khí Cl2 (đktc). Hiệu suất phản ứng là 85%. V có giá trị là :
A. 2 lít
B. 2,905 lít
C. 1,904 lít
D. 1,82 lít
Đáp án C
![]()
MnO2 + 4HCl →MnCl2 + 2H2O + Cl2
0,1 →0,1 (mol)
Do H% = 85% => ![]() = 0,085 (mol)
= 0,085 (mol)
V = 0,085.22,4 = 1,904 (lít)
Đúng 0
Bình luận (0)
12. Lấy 2 lít khí H2 cho tác dụng vs 3 lít khí Clo ( các V lít khí đo ở cùng điều kiện) . Hiệu suất phản ứng là 90%. Xác định thể tích hỗn hợp sau khi phản ứng?
13. Cho 69,6g MnO2 tác dụng vs ddHCl đặc , dư với hiệu suất bằng 70% thứ đc V lít khí Clo( đktc). Xác định giá trị của V?
Bài 12 :
\(PTHH:H_2+Cl_2\rightarrow2HCl\)
Ban đầu : 2______3_______
Phứng :2______2__________
Sau phứng :0______1_____4
\(\rightarrow V_{HCl_{thuc.te}}=4.90\%=3,6\left(l\right)\)
Bài 13 :
\(MnO_2+4HCl\rightarrow MnCl_2+Cl_2+2H_2O\)
0,8________________________0,8______
Ta có :
\(n_{MnO2}=\frac{69,6}{55+32}=0,8\left(mol\right)\)
\(n_{Cl2_{thuc.te}}=0,8.70\%=0,56\left(mol\right)\)
\(\rightarrow V_{Cl2}=0,56.22,4=12,544\left(l\right)\)
Cho 7,75 gam hỗn hợp hai kim loại Cu,Zn tác dụng với khí Cl2 sau phản ứng thu được 16,27 gam hỗn hợp muối.Mặt khác nếu cho hỗn hợp kim loại tác dụng với dung dịch HCl dư thu được V lít khí H2 (đktc).Xác định giá trị của V?
Xem chi tiết
Gọi a và b lần lượt là số mol của Cu và Zn
Bảo toàn khối lượng: \(m_{Cl_2}=m_{muối}-m_{hh}=8,52\left(g\right)\)
\(\Rightarrow n_{Cl_2}=\dfrac{8,52}{71}=0,12\left(mol\right)\)
Bảo toàn mol e: \(2a+2b=0,24\)
Mà \(64a+65b=7,75\)
\(\Rightarrow\left\{{}\begin{matrix}a=0,05\\b=0,07\end{matrix}\right.\)
PTHH: \(Zn+2HCl\rightarrow ZnCl_2+H_2\uparrow\)
Theo PTHH: \(n_{H_2}=n_{Zn}=0,07mol\)
\(\Rightarrow V_{H_2}=0,07\cdot22,4=1,568\left(l\right)\)
Đúng 2
Bình luận (1)
Cho m gam hỗn hợp X gồm Al và FeO (có tỉ lệ số mol tương ứng là 3 : 2) tác dụng với dung dịch
HNO
3
loãng dư thu được 4,928 lít khí NO (đktc, sản phẩm khử duy nhất) và dung dịch A. Nếu đem nung m gam hỗn hợp X đến khi phản ứng nhiệt nhôm kết thúc (giả sử hiệu suất đạt 100%) thu được hỗn hợp Y. Cho hỗn hợp Y tác dụng với dung dịch HCl dư thu được V lít khí
H
2
(đktc). Giá trị của V là A. 6,048 B. 6,272 C....
Đọc tiếp
Cho m gam hỗn hợp X gồm Al và FeO (có tỉ lệ số mol tương ứng là 3 : 2) tác dụng với dung dịch HNO 3 loãng dư thu được 4,928 lít khí NO (đktc, sản phẩm khử duy nhất) và dung dịch A. Nếu đem nung m gam hỗn hợp X đến khi phản ứng nhiệt nhôm kết thúc (giả sử hiệu suất đạt 100%) thu được hỗn hợp Y. Cho hỗn hợp Y tác dụng với dung dịch HCl dư thu được V lít khí H 2 (đktc). Giá trị của V là
A. 6,048
B. 6,272
C. 5,824
D. 6,496
Cho m gam hỗn hợp X gồm Al và FeO (có tỉ lệ số mol tương ứng là 2 : 1) tác dụng với dung dịch
HNO
3
loãng dư thu được 15,68 lít khí NO (đktc, sản phẩm khử duy nhất) và dung dịch A. Nếu đem nung m gam hỗn hợp X đến khi phản ứng nhiệt nhôm kết thúc (giả sử hiệu suất đạt 100%) thu được hỗn hợp Y. Cho hỗn hợp Y tác dụng với dung dịch HCl dư thu được V lít khí
H
2
(đktc). Giá trị của V là A. 20,48 B. 20,16 C....
Đọc tiếp
Cho m gam hỗn hợp X gồm Al và FeO (có tỉ lệ số mol tương ứng là 2 : 1) tác dụng với dung dịch HNO 3 loãng dư thu được 15,68 lít khí NO (đktc, sản phẩm khử duy nhất) và dung dịch A. Nếu đem nung m gam hỗn hợp X đến khi phản ứng nhiệt nhôm kết thúc (giả sử hiệu suất đạt 100%) thu được hỗn hợp Y. Cho hỗn hợp Y tác dụng với dung dịch HCl dư thu được V lít khí H 2 (đktc). Giá trị của V là
A. 20,48
B. 20,16
C. 10,8
D. 6,496
Tính hiệu suất của phản ứng điều chế khí clo khi cho 17,4g Mno2 tác dụng với Hcl đặc dư thì thu được 3,584 lít khí clo (đktc).giúp mình với
\(n_{MnO_2}=\dfrac{17,4}{87}=0,2\left(mol\right)\\ PTHH:MnO_2+4HCl_{đặc,nóng}\rightarrow MnCl_2+Cl_2+2H_2O\\ n_{Cl_2\left(TT\right)}=\dfrac{3,584}{22,4}=0,16\left(mol\right)\\ n_{Cl_2\left(LT\right)}=n_{MnO_2}=0,2\left(mol\right)\\ \Rightarrow H=\dfrac{n_{Cl_2\left(TT\right)}}{n_{Cl_2\left(LT\right)}}.100\%=\dfrac{0,16}{0,2}.100=80\%\)
Đúng 2
Bình luận (0)
Cho 69,6g MnO2 tác dụng với dung dịch HCl đặc, dư. Dẫn khí thoát ra đi vào 500ml dung dịch NaOH 4M (ở nhiệt độ thường).
a) Viết phương trình hóa học của phản ứng xảy ra.
b) Xác định nồng độ mol/l của những chất có trong dung dịch sau phản ứng. Biết rằng tinh thể của dung dịch sau phản ứng thay đổi không đáng kể
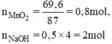
a) Phương trình hóa học của phản ứng:
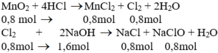
b) Theo pt (1): nCl2 = nMnCl2 = nMnO2 = 0,8 mol
Theo pt (2): nNaCl = nNaClO = nCl2 = 0,8 mol
nNaOH pư = 2. nCl2 = 2. 0,8 = 1,6 mol
⇒ nNaOH dư = 2 - 1,6 = 0,4 mol
Nồng độ mol/l của các chất trong dung dịch sau phản ứng:
CM (NaCl) = CM (NaClO) = CM(MnCl2) = 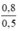 = 1,6 mol/ lit
= 1,6 mol/ lit
CM (NaOH)dư = 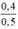 = 0,8 mol/ lit
= 0,8 mol/ lit
Đúng 2
Bình luận (0)
14. Thể tích khí Clo(đktc) thứ đc khi cho dung dịch đặc chứa 21,9g HCl tác dụng hết với KMnO4 là?
17. Hòa tan 23,7g Kmno4 vào dung dịch HCl đặc dư thì thu đc V lít khí Clo (đktc) . Biết rằng phản ứng xảy ra hoàn toàn , giá trị V là?
24. Cho 12,5g MnO2 ( có chứa 30,4% tạp chất trơ) , tác dụng với HCl đặc dư sinh ra V lít khí Clo(đktc). Biết hiệu suất phản ứng là 85%. V có giá trị là?
bài 17
nKMnO4=23,7\158=0,15 mol
| 16HCl | + | 2KMnO4 | → | 5Cl2 | + | 8H2O | + | 2KCl | + | 2MnCl2 |
2KMnO4 + 16HCl = 2KCl + 2MnCl2 + 5Cl2 + 8H2O
0,6 ----------------------- 0,1875 mol
nHCl=21,9\36,5=0,6 mol
=>VCl2=0,1875.22,4=4,2 l
\(\left(1\right)\) \(n_{HCl}=\frac{21,9}{36,5}=0,6\left(mol\right)\)
\(PTHH:2KMnO_4+16HCl_{\left(\text{đ}\right)}\underrightarrow{t^o}2KCl+2MnCl_2+5Cl_2+8H_2O\)
(mol)________________0,6__________________________3/16___________
\(V_{Cl_2}=22,4.\frac{3}{16}=4,2\left(l\right)\)
\(\left(2\right)\) \(n_{KMnO_4}=\frac{23,7}{158}=0,15\left(mol\right)\)
\(PTHH:2KMnO_4+16HCl_{\left(\text{đ}\right)}\underrightarrow{t^o}2KCl+2MnCl_2+5Cl_2+8H_2O\)
(mol)_______0,15________________________________0,375____________
\(V_{Cl_2}=22,4.0,375=8,4\left(l\right)\)
Xem thêm câu trả lời


















