Đốt cháy hoàn toàn 0,9g chất hữu cơ chứa C,H,Ở sinh ra 1,32g CO2 và 0,54g nước Phân tử khối của chất đó là 180
a, Tìm CTPT của HCHC trên
b, Tính thể tích không khí (đktc) cần dùng để đốt cháy hoàn toàn 18g HCHC trên
Đốt cháy hoàn toàn 7g hợp chất hữu cơ A thu được 11,2 l khí CO2 đo ở đktc và 9 g nước.
a, Xác định CTHH của A biết tỉ khối dA/CH4=1,75
b, Tính thể tích không khí cần dùng để đốt cháy hoàn toàn a biết oxi chiếm 20% không khí
Chất hữu cơ A chứa 7,86% H; 15,73% N về khối lượng. Đốt cháy hoàn toàn 2,225 gam A thu được CO2, hơi nước và khí nitơ, trong đó thể tích khí CO2 là 1,68 lít (đktc). Công thức phân tử của A là (biết MA < 100)
A. C3H7ON2
B. C6H14O2N
C. C3H7O2N.
D. C3H7ON
Đốt cháy hoàn toàn 1,3g một hợp chất hữu cơ A thu đc 2,24l khí CO2(đktc) và 0,9g H2O. Bt rằng A nặng hơn phân tử metan 1,625 lần.Tìm CTPT, viếtCTCT của A
\(n_{CO_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
\(n_{H_2O}=\dfrac{0,9}{18}=0,05\left(mol\right)\)
Bảo toàn C: nC = 0,1 (mol)
Bảo toàn H: nH = 0,1 (mol)
Xét mC + mH = 12.0,1 + 1.0,1 = 1,3 (g)
=> A chứa C và H
Xét nC : nH = 0,1 + 0,1 = 1 : 1
=> CTPT: (CH)n
Mà MA = 1,625.16 = 26 (g/mol)
=> n = 2
=> CTPT: C2H2
Anh chị làm ơn giúp e mấy bài này ạ.E cảm ơn!
Bài 1:
Khi đốt cháy hoàn toàn một lượng hợp chất hữu cơ X cần 0,8 gam O2 người ta thu được 1,1 gam CO2,0,45 gam H2O và không có sản phẩm nào khác. Xác định công thức phân tử của X. Biết rằng khi cho bay hơi hoàn toàn 0,6gam X ở điều kiện nhiệt độ và áp suất thích hợp đã thu được một thể tích hơi đúng bằng thể tích hơi của 0,32 gam O2 trong cùng điều kiện.
Bài 2:
Đốt cháy hoàn toàn một hợp chất hữu cơ A có thành phần C,H,O thu được CO2 có thể tích bằng 3/4 thể tích hơi nước và bằng 6/7 thể tích O2 dùng để đốt cháy. Mặt khác, 1l hơi A có khối lượng bằng 46 lần khối lượng 1 lít H2 ở cùng điều kiện.Tìm công thức phân tử của A.
Bài 3: Đốt cháy hoàn toàn 4,3 gam hợp chất hữu cơ thu được 6,72 lít CO2 và 0,35 mol H2O. Khi đốt cháy hoàn toàn 1 mol chất A cần 212,8l O2.Xác định CTPT của A.
Đốt cháy hoàn toàn 1,88 gam chất hữu cơ A (chứa C, H, O) cần 1,904 lít O2 (đktc) thu được CO2 và hơi nước theo tỉ lệ thể tích 4:3. Hãy xác định công thức phân tử của A. Biết tỉ khối của A so với không khí nhỏ hơn 7.
A. C8H12O5.
B. C4H8O2.
C. C8H42O3.
D. C6H12O6.
Thông thường khi đề bài cho số mol O2 cần để đốt cháy thì chắc chắn ta sẽ phải sử dụng hoặc định luật bảo khối lượng, hoặc bảo toàn nguyên tố Oxi.
Quay trở lại bài toán này, ta thấy đề cho cần dùng 1,904 lít O2, không cho khối lượng CO2 và H2O mà chỉ cho tỉ lệ thể tích (tỉ lệ số mol), do đó nhận ra được nếu ta sử dụng phương pháp bảo toàn khối lượng ta sẽ tính được số mol CO2 và số mol H2O, từ đó tính được số mol O trong A. Tiếp theo đó ta sẽ xác định công thức đơn giản nhất để tìm ra công thức phân tử.
Có: n O 2 = 1 , 904 22 , 4 = 0 , 085 ( m o l ) ⇒ m O 2 = 0 , 085 . 32 = 2 , 72 ( g a m )
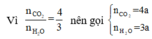
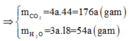
Sơ đồ phản ứng: A + O2 ⇒ CO2 + H2O
Áp dụng định luật bảo toàn khối lượng ta có: m A + m O 2 = m C O 2 + m H 2 O
Hay 1,88 + 2,72 = 176a + 54a ⟺ a = 0,02
⇒ 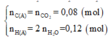
![]()
![]()
Vì C : H : O = nC : nH : nO =0,08 : 0,12 : 0,05 = 8 : 12 : 5
Nên công thức đơn giản nhất của A là C8H12O5.
Khi đó công thức phân tử của A có dạng (C8H12O5)n
Mà MA < 7Mkhôngkhí nên 188n < 7.29 ⇒ n < 1,08 ⇒ n = l
Do đó công thức phân tử của A là C8H12O5.
Đáp án A.
Đốt cháy hoàn toàn hợp chất hữu cơ A chứa C và H thu được 17,6g CO2 và 10,8g H2O a)Tính khối lượng của hợp chất A đã dùng b)Tính khối lượng của khí O2 cần để đốt hết lượng A
a) \(n_{CO_2}=\dfrac{17,6}{44}=0,4\left(mol\right)\)
=> nC = 0,4 (mol)
\(n_{H_2O}=\dfrac{10,8}{18}=0,6\left(mol\right)\)
=> nH = 1,2 (mol)
mA = mC + mH = 0,4.12 + 1,2 = 6 (g)
b)
Bảo toàn O: \(n_{O_2}=\dfrac{0,4.2+0,6}{2}=0,7\left(mol\right)\)
=> mO2 = 0,7.32 = 22,4 (g)
a, Tính thể tích của oxi (đktc) cần dùng để đốt cháy hết 3,1 gam P, biết phản ứng sinh ra chất rắn P2O5.
b, Đốt cháy hoàn toàn 1,12 lít khí CH4 (đktc) cần dùng V lít khí O2 (đktc), sau phản ứng thu được sản phẩm là khí cacbonic (CO2) và nước (H2O). Giá trị của V là
a, Theo giả thiết ta có: \(n_P=\dfrac{3,1}{31}=0,1\left(mol\right)\)
\(4P+5O_2--t^o->2P_2O_5\)
Ta có: \(n_{O_2}=\dfrac{5}{4}.n_P=0,125\left(mol\right)\Rightarrow V_{O_2\left(đktc\right)}=0,125.22,4=2,8\left(l\right)\)
b, Theo giả thiết ta có: \(n_{CH_4}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\)
\(CH_4+2O_2--t^o->CO_2+2H_2O\)
Ta có: \(n_{O_2}=2.n_{CH_4}=0,1\left(mol\right)\Rightarrow V_{O_2\left(đktc\right)}=2,24\left(l\right)\)
Đốt cháy hoàn toàn một lượng chất hữu cơ chứa C, H, Cl sinh ra 0,22 gam CO2 và 0,09 gam H2O, còn lại là khí Cl2. Khi phân tích định lượng clo của cùng một lượng chất đó bằng một lượng dung dịch AgNO3 người ta thu được 1,435 gam AgCl, CTPT của hợp chất trên là:
A. CH2Cl2
B. CH3Cl
C. C2H2Cl4
D. C2H4Cl2
Đốt cháy hoàn toàn 1,8g hợp chất hữu cơ A ( thành phần chứa C,H, O) thu được 2,64g CO2 và 1,08g H2O. Khối lượng phân tử của A bằng 180 dvc. Xđ CTPT của A Giúp em vs ạ
\(n_{CO_2}=\dfrac{2,64}{44}=0,06\left(mol\right)\)
=> nC = 0,06 (mol)
\(n_{H_2O}=\dfrac{1,08}{18}=0,06\left(mol\right)\)
=> nH = 0,12 (mol)
\(n_O=\dfrac{1,8-0,06.12-0,12.1}{16}=0,06\left(mol\right)\)
Xét nC : nH : nO = 0,06 : 0,12 : 0,06 = 1 : 2 : 1
=> CTPT: (CH2O)n
Mà PTKA = 180 đvC
=> n = 6
=> CTPT: C6H12O6