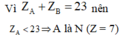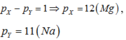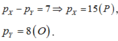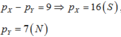1) Hai nguyên tố A, B liên tiếp nhau trong bảng tuần hoàn. B thuộc nhóm V. Ở trạng thái đơn chất A, B không phản ứng với nhau. Tổng số điện tích hạt nhân của nguyên tử A,B là 23. Viết cấu hình e của A,B
2) Khi cho 3,33g một kim loại kiềm vào nước thì có 0,48g hidro thoát ra. cho biết tên kim loại kiềm đó?
3) Khi cho 0,6g một kim loại thuộc nhóm IIA tác dụng với nước thì có 0,336 lít hidro thoát ra (dktc). Gọi tên kim loại đó
4) Cho 0,54g kim loại M thuộc nhóm IIIA tác dụng với 60g dung dịch HCL vừa đủ thu được 0,672 lít khí dktc
a) xác định tên kim loại
b) tính c% của dung dịch HCl
5) Cho 8,8g hỗn hợp hai kim loại kiềm nằm ở hai chu kì liên tiếp và nằm ở nhóm IIA, tác dụng với HCl dư thì thu được 6,72 lít khí hidro (dktc). Dựa vào bảng tuần hoàn xét xem hai kim loại đó là gì?