hai n tố X và Y thuộc cùng một nhóm, X là phi kim đc tạo với kali một hợp chất trong đó X chiếm 17,02 % khối lượng. X tạo đc với Y hai hợp chất trong đó Y chiếm 40% và 50% khối lượng. hai n tố X và Y là

Những câu hỏi liên quan
Cho 2 nguyên tố X và Y thuộc hai chu kì liên tiếp (
Z
X
Z
Y
) và cùng số thứ tự của nhóm trong bảng tuần hoàn (nhóm A và nhóm B).- Nguyên tố X tạo thành hợp chất ion với clo ứng với công thức XC1.- Nguyên tố Y cũng tạo thành hợp chất với clo hợp chất YC1 trong đó khối lượng của clo chiếm 24,7%.Xác định các nguyên tố X và Y.
Đọc tiếp
Cho 2 nguyên tố X và Y thuộc hai chu kì liên tiếp ( Z X < Z Y ) và cùng số thứ tự của nhóm trong bảng tuần hoàn (nhóm A và nhóm B).
- Nguyên tố X tạo thành hợp chất ion với clo ứng với công thức XC1.
- Nguyên tố Y cũng tạo thành hợp chất với clo hợp chất YC1 trong đó khối lượng của clo chiếm 24,7%.
Xác định các nguyên tố X và Y.
X tạo bởi chất ion với clo có công thức là XC1, vậy X là kim loại có hoá trị I.
Y cùng số nhóm với X vậy cũng có hoá trị I, công thức clorua của nó là YC1.
Ta có:
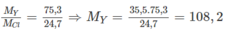
( M Y và M Cl lần lượt là NTK của nguyên tố Y và nguyên tố clo). Đó là Ag. Nguyên tố X cùng chu kì, cùng số thứ tự nhóm với Ag là kali (K))
Đúng 0
Bình luận (0)
Ba nguyên tố X,Y,Z thuộc cùng một nhóm A và ở 3 chủ kỳ liên tiếp nhau trong bảng HTTH. Biết X là phi kim, tạo hợp chất với nguyên tố natri trong đó X chiếm 25,8% về khối lượng . X tạo đc với Y hai loại hợp chất A và hợp vhaats B. Trong A và B phần trăm về khối lượng của Y lần lượt là 50% và 40%. Các nguyên tố Y,X,Z lần lượt là.?
Giúp mk vs mai mk nộp bài rồi
hợp chất a đc cấu tạo bởi nguyên tố x có hóa trị là v và nguyên tố oxi biết phân tử khối của hợp chất a bằng 108 đvc hợp chất b tạo bởi hai nguyên tố p và o trong đó oxi chiếm 43,64 về khối lượng bt d B/o2=3,44
- H/c A:
CTHH: XxOy (x, y ∈ N*)
Theo quy tắc hoá trị: x.V = y.II
Chuyển thành tỉ lệ: \(\dfrac{x}{y}=\dfrac{II}{V}=\dfrac{2}{5}\rightarrow\left\{{}\begin{matrix}x=2\\y=5\end{matrix}\right.\)
CTHH: X2O5
=> 2X + 16.5 = 108
=> X = 14 (đvC)
=> X là Photpho (P)
CTHH: P2O5
- H/c B:
CTHH: PxOy
\(M_{P_xO_y}=3,44.32=110\left(\dfrac{g}{mol}\right)\)
-> mO2 = 43,64% . 110 = 48 (g)
\(\rightarrow n_{O_2}=\dfrac{48}{16}=3\left(mol\right)\)
-> xP + 3.16 = 110
-> x = 2
CTHH: P2O3
Đúng 1
Bình luận (0)
Nguyên tố Y là phi kim thuộc chu kì 2 của BTH, Y tạo được hợp chất khí với hiđro và công thức oxit cao nhất là YO2. Hợp chất tạo bởi Y và kim loại M là MY2 trong đó Y chiếm 37,5% về khối lượng. M là *
*Xác định Y:
Y thuộc chu kì 2 => Y có 2 lớp e
Công thức oxit cao nhất của Y là YO2
=> Y có hóa trị IV
=> Y thuộc nhóm IVA
=> Y có 4e lớp ngoài cùng
=> Cấu hình e của Y: 1s22s22p2
=> Y là Cacbon
*Xác định M:
Hợp chất MC2
\(\%m_C=\dfrac{2.12}{M+2.12}.100=37,5\%\)
=> M=40 (Ca)
Vậy M là Ca
Đúng 1
Bình luận (0)
X là nguyên tố thuộc nhóm halogen. X tạo với H hợp chất trong đó X chiếm 95% về khối lượng. Nguyên tố X là
A. F.
B. Cl.
C. I.
D. Br.
X tạo với H hợp chất là HX.
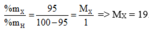
Vậy X là F. Chọn đáp án A.
Đúng 0
Bình luận (0)
Một hợp chất khí X có phân tử khối là 58 đvC, cấu tạo từ hai nguyên tố C và H. Biết trong X nguyên tố C chiếm 82,76% khối lượng. Tìm công thức hóa học của hợp chất khí Y. *
A C4H10
B C3H10
C C4H8
D C3H8
Gọi CTHH X là \(C_xH_y\)
\(\Rightarrow\dfrac{12x}{12x+y}=82,76\%\\ \Rightarrow\dfrac{12x}{58}=82,76\%\\ \Rightarrow x=4\\ \Rightarrow y=10\\ \Rightarrow C_4H_{10}\)
Chọn A
Đúng 0
Bình luận (0)
bài 1: Công thức hóa học của hợp chất giữa nguyên tố X với O có %X = 82,97% (Biết X có hóa trị I trong hợp chất với O) là (O = 16; Al = 27; Cr = 52; Fe = 56)
bài 2: Hợp chất Y tạo bởi 2 nguyên tố S và O, trong đó nguyên tố Oxi chiếm 50% về khối lượng trong hợp chất. Công thức hóa học của Y là (O = 16; S = 32)
Bài 1
Gọi CTHH của hợp chất là X2O5
Theo đề ra, ta có:
2X2X+16.5.100%=43,67%2X2X+16.5.100%=43,67%
Giải phương trình, ta được X = 31
=> X là P
=> CTHH của hợp chất: P2O5
xin lỗi tôi chỉ giúp được bạn bài 1
Đúng 0
Bình luận (0)
Bài 1:
\(\%_O=100\%-82,97\%=17,03\%\\ CTTQ:X_2O\\ \Rightarrow M_{X_2O}=\dfrac{16}{17,03\%}\approx 94(g/mol)\\ \Rightarrow M_X=\dfrac{94-16}{2}=39(g/mol)(K)\\ \Rightarrow CTHH:K_2O\)
bài 2:
\(CTTQ_Y:S_xO_y\\ \Rightarrow M_{S_xO_y}=\dfrac{16y}{50\%}=32y(g/mol)\\ \Rightarrow 32x+16y=32y\Rightarrow 32x=16y\\ \Rightarrow 2x=y\Rightarrow \dfrac{x}{y}=\dfrac{1}{2}\\ \Rightarrow x=1;y=2\\ \Rightarrow CTHH_Y:SO_2\)
Đúng 1
Bình luận (0)
Nguyên tố Y là phi kim thuộc chu kì 3, có công thức oxit cao nhất là
YO
3
. Y tạo với kim loại M một hợp chất có công thức
MY
2
, trong đó M chiếm 46,67% khối lượng. Nguyên tố M là A. Cu. B. Mg. C. Pb. D. Fe.
Đọc tiếp
Nguyên tố Y là phi kim thuộc chu kì 3, có công thức oxit cao nhất là YO 3 . Y tạo với kim loại M một hợp chất có công thức MY 2 , trong đó M chiếm 46,67% khối lượng. Nguyên tố M là
A. Cu.
B. Mg.
C. Pb.
D. Fe.
1. Cho hợp chất RH3 trong đó Hiđro chiếm 17,65% về khối lượng . Nguyên tố R là ?
2. Nguyên tố X có hóa trị cao nhất đối với oxi gấp 3 lần hóa trị đối với hiđro . Hợp chất oxit cao nhất của X có tỉ khối hơi so với Nitơ là 2,857. Vậy vị trí của X trong bảng tuần hoàn là ?
3. Nguyên tố R có công thức hợp chất khí với hiđro là RH3 . Trong hợp chất oxit cao nhất , R chiếm 43,66% khối lượng . Vậy R là ?
4. Y là một nguyên tố phi kim thuộc chu kì 3 trong BTH , Y tạo được hợp chất khí với hiđro và...
Đọc tiếp
1. Cho hợp chất RH3 trong đó Hiđro chiếm 17,65% về khối lượng . Nguyên tố R là ?
2. Nguyên tố X có hóa trị cao nhất đối với oxi gấp 3 lần hóa trị đối với hiđro . Hợp chất oxit cao nhất của X có tỉ khối hơi so với Nitơ là 2,857. Vậy vị trí của X trong bảng tuần hoàn là ?
3. Nguyên tố R có công thức hợp chất khí với hiđro là RH3 . Trong hợp chất oxit cao nhất , R chiếm 43,66% khối lượng . Vậy R là ?
4. Y là một nguyên tố phi kim thuộc chu kì 3 trong BTH , Y tạo được hợp chất khí với hiđro và có công thức oxit cao nhất là YO3 . Hợp chất tạo bởi Y và kim loại M là MY2 trong đó M chiếm 46,67% về khối lượng . Vậy M là ?
Câu 1:
Ta có
\(\frac{3}{R+3}=17,65\%\)
=>MR=14
Vậy R là Nito
Câu 2:
Ta có X có hóa trị với O gấp 3 lần hóa trị với H
=>X ở nhóm VIA
CT oxit cao nhất XO3
Ta có :
\(\text{MXO3=28}.\text{2,857=80}\)
=>MX=32
=>X là lưu huỳnh
X có Z=16
Cấu hình X:\(1s^22s^22p^63s^23p^4\)
=> X ở ô 16 chu kì 3 nhóm VIA
Câu 3:
Hợp chất với H là RH3
-->Oxit cao nhất là R2O5
Ta có :\(\frac{2R}{2R+16.5}=0,4366\)
=>R=31
->R là Photpho
Câu 4:
Y thuộc chu kỳ 3
Hợp chất oxit cao nhất là YO3 hay Y2O6
-->Y thuộc nhóm VIA
-->Y là S lưu huỳnh
->Hợp chất với kim loại là MS2
Ta có:\(\frac{M}{M+2.32}=0,4667\)
->M=56 Fe
Câu1
Ta có
\(\frac{3}{R+3}=0,1765\)
-->3=0,1765R+0,5295
--->2,4705=0,1765R
--->R=14(Nito)
Vậy R là nito..kí hiệu N
Bài 3
CTHH:R2O5
Theo bài ra ta có
\(\frac{2R}{2R+80}=0,4366\)
--->2R=0,8732R+34,938
---->1,1286R=34,938
-->R=31(P)
CTHH:P2O5




















