Nguyên tử của nguyên tố Z có tổng số hạt cơ bản là 46. Biết rằng tổng số hạt mang điện bằng 1,875 lần tổng số hạt ko mang điện. Tổng điện tích của các hạt electron trên nguyên tử Z là ?

Những câu hỏi liên quan
a. Tổng số hạt cơ bản của nguyên tử nguyên tố X là 155, số hạt mang điện nhiều hơn số hạt không mang điện là 33 hạt.a. Tổng số hạt cơ bản của nguyên tử nguyên tố X là 46, số hạt không mang điện bằng 8/15 số hạt mang điện.b. Nguyên tử titan (Ti) có tổng số hạt (p, n, e) là 70 ạthạt, trong đó hạt mang điện dương ít hơn hhhhhdsdfzhxfmhhj athạt không mang điện 4 hạt.
Đọc tiếp
a. Tổng số hạt cơ bản của nguyên tử nguyên tố X là 155, số hạt mang điện nhiều hơn số hạt không mang điện là 33 hạt.
a. Tổng số hạt cơ bản của nguyên tử nguyên tố X là 46, số hạt không mang điện bằng 8/15 số hạt mang điện.
b. Nguyên tử titan (Ti) có tổng số hạt (p, n, e) là 70 ạthạt, trong đó hạt mang điện dương ít hơn hhhhhdsdfzhxfmhhj athạt không mang điện 4 hạt.
Cho các thông tin sau: Ion
X
2
-
có cấu trúc electron:
1
s
2
2
s
2
2
p
6
3
s
2
3
p
6
Nguyên tố Y có tổng số hạt cơ bản trong nguyên tử là 40. Trong đó số hạt mang điện nhiều hơn số hạt không mang điện là...
Đọc tiếp
Cho các thông tin sau:
Ion X 2 - có cấu trúc electron: 1 s 2 2 s 2 2 p 6 3 s 2 3 p 6
Nguyên tố Y có tổng số hạt cơ bản trong nguyên tử là 40. Trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 12.
Ion Z 2 + có tổng số hạt mang điện tích dương trong hạt nhân bằng 29.
Vị trí của X, Y, Z trong bảng tuần hoàn lần lượt là:
A. (X: ô 16, chu kỳ 3, nhóm VIA); ( Y: ô 13, chu kì 3, nhóm IIIA); (Z: ô 29, chu kì 4, nhóm IB).
B. (X: ô 16, chu kỳ 3, nhóm VIA); (Y: ô 13, chu kì 3, nhóm IA); (Z: ô 29, chu kì 4, nhóm IIB).
C. (X: ô 20, chu kỳ 4, nhóm IIA); (Y: ô 13, chu kì 3, nhóm IIIA); (Z: ô 29, chu kì 4, nhóm IB).
D. (X: ô 16, chu kỳ 3, nhóm VIA); ( Y: ô 13, chu kì 3, nhóm IIIA); (Z: ô 31, chu kì 4, nhóm IIIA).
Tổng số proton, nơtron và electron trong nguyên tử X bằng 3,75 lần số hạt mang điện của nguyên tử Y. Tổng số proton, nơtron, electron trong nguyên tử Y bằng 0,65 lần số hạt mang điện của nguyên tử X. Tổng số nơtron trong 1 nguyên tử X và 1 nguyên tử Y bằng 1,875 lần số hạt mang điện của Y. Tỉ lệ số hạt mang điện giữa X và Y là A. 15:16 B. 16:15 C. 2:5 D. 5:2
Đọc tiếp
Tổng số proton, nơtron và electron trong nguyên tử X bằng 3,75 lần số hạt mang điện của nguyên tử Y. Tổng số proton, nơtron, electron trong nguyên tử Y bằng 0,65 lần số hạt mang điện của nguyên tử X. Tổng số nơtron trong 1 nguyên tử X và 1 nguyên tử Y bằng 1,875 lần số hạt mang điện của Y. Tỉ lệ số hạt mang điện giữa X và Y là
A. 15:16
B. 16:15
C. 2:5
D. 5:2
Tổng số proton, nơtron và electron trong nguyên tử X bằng 3,75 lần số hạt mang điện của nguyên tử Y. Tổng số proton, nơtron, electron trong nguyên tử Y bằng 0,65 lần số hạt mang điện của nguyên tử X. Tổng số nơtron trong 1 nguyên tử X và 1 nguyên tử Y bằng 1,875 lần số hạt mang điện của Y. Tỉ lệ số hạt mang điện giữa X và Y là A. 15:16 B. 16:15 C. 2:5 D. 5:2
Đọc tiếp
Tổng số proton, nơtron và electron trong nguyên tử X bằng 3,75 lần số hạt mang điện của nguyên tử Y. Tổng số proton, nơtron, electron trong nguyên tử Y bằng 0,65 lần số hạt mang điện của nguyên tử X. Tổng số nơtron trong 1 nguyên tử X và 1 nguyên tử Y bằng 1,875 lần số hạt mang điện của Y. Tỉ lệ số hạt mang điện giữa X và Y là
A. 15:16
B. 16:15
C. 2:5
D. 5:2
Nguyên tử X có tổng các loại hạt cơ bản là 46, trong đó số hạt mang điện tích nhiều hơn số hạt không mang điện tích là 14 hạt.
a) Tính số p, n, e, A của nguyên tử X. ( Z=15)
b) Viết kí hiệu nguyên tử và cấu hình electron của X.
Ở trạng thái cơ bản: - Phân lớp electron ngoài cùng của nguyên tử nguyên tố X là np2n+1. - Tổng số electron trên các phân lớp p của nguyên tử nguyên tố Y là 7. - Số hạt mang điện trong nguyên tử nguyên tố Z nhiều hơn số hạt mang điện trong nguyên tử nguyên tố X là 20 hạt. Nhận xét nào sau đây là sai A. Độ âm điện giảm dần theo thứ tự X, Y, Z. B. Nguyên tố X và Y thuộc 2 chu kì kế tiếp C. Oxit và hiđroxit của Y có tính lưỡng tính D. Số oxi hóa cao nhất của X trong hợp chất là +7.
Đọc tiếp
Ở trạng thái cơ bản:
- Phân lớp electron ngoài cùng của nguyên tử nguyên tố X là np2n+1.
- Tổng số electron trên các phân lớp p của nguyên tử nguyên tố Y là 7.
- Số hạt mang điện trong nguyên tử nguyên tố Z nhiều hơn số hạt mang điện trong nguyên tử nguyên tố X là 20 hạt. Nhận xét nào sau đây là sai
A. Độ âm điện giảm dần theo thứ tự X, Y, Z.
B. Nguyên tố X và Y thuộc 2 chu kì kế tiếp
C. Oxit và hiđroxit của Y có tính lưỡng tính
D. Số oxi hóa cao nhất của X trong hợp chất là +7.
Ở trạng thái cơ bản: - Phân lớp electron ngoài cùng của nguyên tử nguyên tố X là np2n+1. - Tổng số electron trên các phân lớp p của nguyên tử nguyên tố Y là 7. - Số hạt mang điện trong nguyên tử nguyên tố Z nhiều hơn số hạt mang điện trong nguyên tử nguyên tố X là 20 hạt. Nhận xét nào sau đây là sai? A. Độ âm điện giảm dần theo thứ tự X, Y, Z. B. Nguyên tố X và Y thuộc 2 chu kì kế tiếp. C. Oxit và hiđroxit của Y có tính lưỡng tính. D. Số oxi hóa cao nhất của X trong hợp chất là +7.
Đọc tiếp
Ở trạng thái cơ bản:
- Phân lớp electron ngoài cùng của nguyên tử nguyên tố X là np2n+1.
- Tổng số electron trên các phân lớp p của nguyên tử nguyên tố Y là 7.
- Số hạt mang điện trong nguyên tử nguyên tố Z nhiều hơn số hạt mang điện trong nguyên tử nguyên tố X là 20 hạt.
Nhận xét nào sau đây là sai?
A. Độ âm điện giảm dần theo thứ tự X, Y, Z.
B. Nguyên tố X và Y thuộc 2 chu kì kế tiếp.
C. Oxit và hiđroxit của Y có tính lưỡng tính.
D. Số oxi hóa cao nhất của X trong hợp chất là +7.
Ở trạng thái cơ bản:- Phân lớp electron ngoài cùng của nguyên tử nguyên tố X là
np
2
n
+
1
- Tổng số electron trên các phân lớp p của nguyên tử nguyên tố Y là 7.- Số hạt mang điện trong nguyên tử nguyên tố z nhiều hơn số hạt mang điện trong nguyên tử nguyên tố X là 20 hạt.Nhận xét nào sau đây là sai? A. Nguyên tố X và Y thuộc 2 chu kì kế tiếp B. Số oxi hóa c...
Đọc tiếp
Ở trạng thái cơ bản:
- Phân lớp electron ngoài cùng của nguyên tử nguyên tố X là np 2 n + 1
- Tổng số electron trên các phân lớp p của nguyên tử nguyên tố Y là 7.
- Số hạt mang điện trong nguyên tử nguyên tố z nhiều hơn số hạt mang điện trong nguyên tử nguyên tố X là 20 hạt.
Nhận xét nào sau đây là sai?
A. Nguyên tố X và Y thuộc 2 chu kì kế tiếp
B. Số oxi hóa cao nhất của X trong hợp chất là +7
C. Oxit và hiđroxit của Y có tính lưỡng tính
D. Độ âm điện giảm dần theo thứ tự X, Y, Z
Cho các thông tin sau: Ion X2- có cấu trúc electron: 1s22s22p63s23p6. Nguyến tố Y có tổng số hạt cơ bản trong nguyên tử là 40. Trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 12. Ion Z2+ có tổng số hạt mang điện tích dương trong hạt nhân bằng 29. Vị trí của X, Y, Z trong bảng tuần hoàn lần lượt là: A. (X: ô 16, chu kỳ 3, nhóm VIA); ( Y: ô 13, chu kì 3, nhóm IIIA); (Z: ô 29, chu kì 4, nhóm IB). B. (X: ô 16, chu kỳ 3, nhóm VIA); ( Y: ô 13, chu kì 3, nhóm IA); (Z: ô 29, chu kì 4, nhó...
Đọc tiếp
Cho các thông tin sau:
Ion X2- có cấu trúc electron: 1s22s22p63s23p6.
Nguyến tố Y có tổng số hạt cơ bản trong nguyên tử là 40. Trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 12.
Ion Z2+ có tổng số hạt mang điện tích dương trong hạt nhân bằng 29.
Vị trí của X, Y, Z trong bảng tuần hoàn lần lượt là:
A. (X: ô 16, chu kỳ 3, nhóm VIA); ( Y: ô 13, chu kì 3, nhóm IIIA); (Z: ô 29, chu kì 4, nhóm IB).
B. (X: ô 16, chu kỳ 3, nhóm VIA); ( Y: ô 13, chu kì 3, nhóm IA); (Z: ô 29, chu kì 4, nhóm IIB).
C. (X: ô 20, chu kỳ 4, nhóm IIA); ( Y: ô 13, chu kì 3, nhóm IIIA); (Z: ô 29, chu kì 4, nhóm IB).
D. (X: ô 16, chu kỳ 3, nhóm VIA); ( Y: ô 13, chu kì 3, nhóm IIIA); (Z: ô 31, chu kì 4, nhóm IIIA).
Đáp án A
Ion X2- có cấu trúc electron: 1s22s22p63s23p6
X + 2e → X2-
Vậy cấu hình electron của X là 1s22s22p63s23p4
X có 3 lớp electron → X thuộc chu kì 3.
X có số electron = 16 → X thuộc ô 16.
X có 6 electron hóa trị, electron cuối cùng điền vào phân lớp 3p → X thuộc nhóm VIA.
• Nguyên tố Y có tổng số hạt cơ bản trong nguyên tử là 40. Trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 12.
Giả sử số hiệu nguyên tử, số nơtron của Y lần lượt là Z, N
Ta có hpt: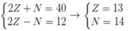
Cấu hình electron của Y là 13Y: 1s22s22p63s23p1
Y có 3 lớp electron → X thuộc chu kì 3.
Y có số electron = 13 → X thuộc ô số 13.
Y có 3 electron hóa trị, electron cuối cùng điền vào phân lớp 3p → Y thuộc nhóm IIIA.
• Ion Z2+ có tổng số hạt mang điện tích dương trong hạt nhân bằng 29.
Z có số hạt mang điện tích dương bằng ion Z2+
Cấu hình electron của Z là 29Z: 1s22s22p63s23p63d104s1
Z thuộc ô số 29.
Z có 4 lớp electron → X thuộc chu kì 4.
Z có electron cuối cùng điền vào phân lớp 3d, có 1 electron hóa trị → Z thuộc nhóm IB.
→ Chọn A.
Đúng 0
Bình luận (0)














