1,Cho 15,68 lít hỗn hợp gồm hai khí CO và CO2 ở đktc có khối lượng là 27,6 gam. Tính thành phần trăm theo khối lượng mỗi khí trong hỗn hợp.

Những câu hỏi liên quan
Cho 15,68 lít hỗn hợp gồm hai khí CO và CO2 ở đktc có khối lượng là 27,6 gam. Tính thành phần trăm theo khối lượng mỗi khí trong hỗn hợp.
\(Gọi\ n_{CO} =a(mol) ; n_{CO_2} = b(mol)\\ n_{khí} = a + b = \dfrac{15,68}{22,4} = 0,7(mol)\\ m_{khí} = 28a + 44b = 27,6(gam)\\ \Rightarrow a = 0,2 ; b = 0,5\\ \%m_{CO} = \dfrac{0,2.28}{27,6}.100\% = 20,29\%\\ \%m_{CO_2} = 100\% - 20,29\% = 79,71\%\)
Đúng 1
Bình luận (1)
1 .Cho 15,68 lít hỗn hợp gồm hai khí CO và CO2 ở đktc có khối lượng là 27,6 gam. Tính thành phần trăm theo khối lượng mỗi khí trong hỗn hợp.
Số mol hỗn hợp: nCO, CO2 = 15,68 /22,4 = 0,7
Gọi số mol CO và CO2 là x và y (x, y > 0)
Ta có PTĐS: x + y = 0,7 => x = 0,7 – y (1)
28x + 44y = 27,6 (2)
Thay x = 0,7 – y vào (2) giải ra ta được: x = 0,2; y = 0,5
mCO = 0,2.28 = 5,6 gam; mCO2 = 0,5.44 = 22 gam
%mCO2 = 79,7% ; % mCO = 20,3 %
Đúng 1
Bình luận (5)
Theo đầu bài có tỉ lệ:
\(\frac{M_{CaSO_4.nH_2O}}{m_{CaSO_4.nH_2O_{ }}}=\frac{M_{H_2O}}{m_{H_2O}}=\frac{136+18n}{19,11}=\frac{18n}{4}\)
Giải ra ta được n = 2
Vậy CTHH là : CaSO4 . 2H2O
Đúng 0
Bình luận (2)
Cho 15,68 lít hỗn hợp gồm hai khí CO và CO2 ở đktc có khối lượng là 27,6 gam. Tính thành phần trăm theo khối lượng mỗi khí trong hỗn hợp.
Số mol hỗn hợp: nCO, CO2 = 15,68 /22,4 = 0,7
Gọi số mol CO và CO2 là x và y (x, y > 0)
Ta có PTĐS: x + y = 0,7 => x = 0,7 – y (1)
28x + 44y = 27,6 (2)
Thay x = 0,7 – y vào (2) giải ra ta được: x = 0,2; y = 0,5
mCO = 0,2.28 = 5,6 gam; mCO2 = 0,5.44 = 22 gam
%mCO2 = 79,7% ; % mCO = 20,3 %
%mCO2=79.7%
%mCO=20.3$
Ở đktc 15,68 lít hỗn hợp khí N2 và khí CO2 có khối lượng là 24,4 g
a) Tính thành phần phần trăm theo thể tích mỗi khí?
b) Tính khối lượng mỗi khí trong hỗn hợp?
a) \(n_{N_2}+n_{CO_2}=\dfrac{15,68}{22,4}=0,7\left(mol\right)\)
Có: \(28.n_{N_2}+44.n_{CO_2}=24,4\)
=> \(\left\{{}\begin{matrix}n_{N_2}=0,4\left(mol\right)\\n_{CO_2}=0,3\left(mol\right)\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}\%V_{N_2}=\dfrac{0,4}{0,7}.100\%=57,143\%\\\%V_{CO_2}=\dfrac{0,3}{0,7}.100\%=42,857\%\end{matrix}\right.\)
b) \(\left\{{}\begin{matrix}m_{N_2}=0,4.28=11,2\left(g\right)\\m_{CO_2}=0,3.44=13,2\left(g\right)\end{matrix}\right.\)
Đúng 2
Bình luận (0)
15,68 lít hỗn hợp gồm hai khí CO và CO2 ở đktc có khối lượng là 27,6 gam. Tính thành phần trăm theo khối lượng mỗi khí trong hỗn hợp.
số mol của hỗn hợp là : 15,68 : 22,4 = 0,7(mol)
Gọi số mol CO và CO2 là x và y (x,y > 0)
Ta có :
PTĐS:
x + y = 0,7 => x = 0,7 – y (1)
28x + 44y = 27,6 (2)
Thay x = 0,7 – y vào (2)
giải ra ta được: x = 0,2; y = 0,5
mCO = 0,2.28 = 5,6 gam; mCO2 = 0,5.44 = 22 gam
%m = 79,7%; %m = 20,3% CO CO
Đúng 0
Bình luận (0)
Gọi x,y là số mol của CO và CO2 (x,y>0)
Theo đề bài,ta có:
nhh(đktc)=nCO+nCO2=x+y=15,68/22,4=0,7(mol)
=>x=0,7-y(1)
Lại có : mhh=mCO+mCO2=28x+44y=27,6(g)(2)
Thế (1) vào (2) ta được 28(0,7-y)+44y=27,6
<=>y=0,5(mol)
=>x=0,7-0,5=0,2(mol)
%mCO=(0,2x28)/27,6 x 100%=20,3%
%mCO2=(0,5x44)/27,6 x 100%=79,7%
Đúng 0
Bình luận (0)
Cho 27,6 gam hỗn hợp 2 kim loại Mg và Ag tác dụng với dung dịch HCl vừa đủ, sau phản ứng thấy thoát ra 5,6 lít khí ở đktc. Thành phần phần trăm theo khối lượng của mỗi kim loại trong hỗn hợp ban đầu lần lượt là: A. 21,74% và 78,26% B. 78,26% và 21,74% C. 88, 04% và 11,96% D. 11,96% và 88, 04%
Đọc tiếp
Cho 27,6 gam hỗn hợp 2 kim loại Mg và Ag tác dụng với dung dịch HCl vừa đủ, sau phản ứng thấy thoát ra 5,6 lít khí ở đktc. Thành phần phần trăm theo khối lượng của mỗi kim loại trong hỗn hợp ban đầu lần lượt là:
A. 21,74% và 78,26%
B. 78,26% và 21,74%
C. 88, 04% và 11,96%
D. 11,96% và 88, 04%
Đáp án A
Cho Mg và Ag tác dụng với HCl chỉ có Mg phản ứng.
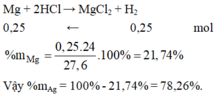
Đúng 0
Bình luận (0)
15lít hỗn hợp khí CO2 và CO ở điều kiện tiêu chuẩn có khối lượng 27,18.Hỏi:
A. bao nhiêu lít mỗi khí trong hỗn hợp đó B. tính phần trăm theo khối lượng mối khí C. tính tỉ khối của hỗn hợp so với không khíCho hỗn hợp khí X gồm CO2 và N2 (ở đktc) có tỉ khối đối với khí oxi là 1,225.
1. Tính thành phần % theo thể tích của mỗi khí trong hỗn hợp X.
2. Tính khối lương của 1 lít hỗn hợp khí X ở đktc.
1)
Coi \(n_X = 1(mol)\)
Gọi : \(n_{CO_2} = a(mol) ; n_{N_2} = b(mol)\)
Ta có :
\(n_X = a + b = 1(mol)\\ m_X = 44a + 28b = 1.1,225.32(gam)\\ \Rightarrow a = 0,7 ; b = 0,3\)
Vậy :
\(\%V_{CO_2} = \dfrac{0,7}{1}.100\% = 70\%\\ \%V_{N_2} = 100\% - 70\% = 30\%\)
2)
\(n_X = \dfrac{1}{22,4}(mol)\\ \Rightarrow m_X = n.M = \dfrac{1}{22,4}.1,225.32 = 1,75(gam)\)
Đúng 2
Bình luận (2)
Để xác định thành phần phần trăm khối lượng của hỗn hợp A gồm bột nhôm và bột magie, người ta thực hiện hai thí nghiệm sau: – Thí nghiệm 1: cho m gam hỗn hợp A tác dụng hết với dung dịch HCl loãng dư, thu được 5,6 lít khí ở đktc. – Thí nghiệm 2: cho m gam hỗn hợp A tác dụng với dung dịch NaOH dư, thu được 3,36 lít khí ở đktc. Tính phần trăm khối lượng của mỗi chất trong hỗn hợp A.
Đọc tiếp
Để xác định thành phần phần trăm khối lượng của hỗn hợp A gồm bột nhôm và bột magie, người ta thực hiện hai thí nghiệm sau:
– Thí nghiệm 1: cho m gam hỗn hợp A tác dụng hết với dung dịch HCl loãng dư, thu được 5,6 lít khí ở đktc.
– Thí nghiệm 2: cho m gam hỗn hợp A tác dụng với dung dịch NaOH dư, thu được 3,36 lít khí ở đktc. Tính phần trăm khối lượng của mỗi chất trong hỗn hợp A.
Gọi số mol của Al và Fe lần lượt là a và b
Ta có 1,5a + b = 0,25
1,5a = 0,15
=> a = 0,1 và b = 0,1
=> %Al = 32,53%
%Fe= 67,47%
Đúng 0
Bình luận (0)





















