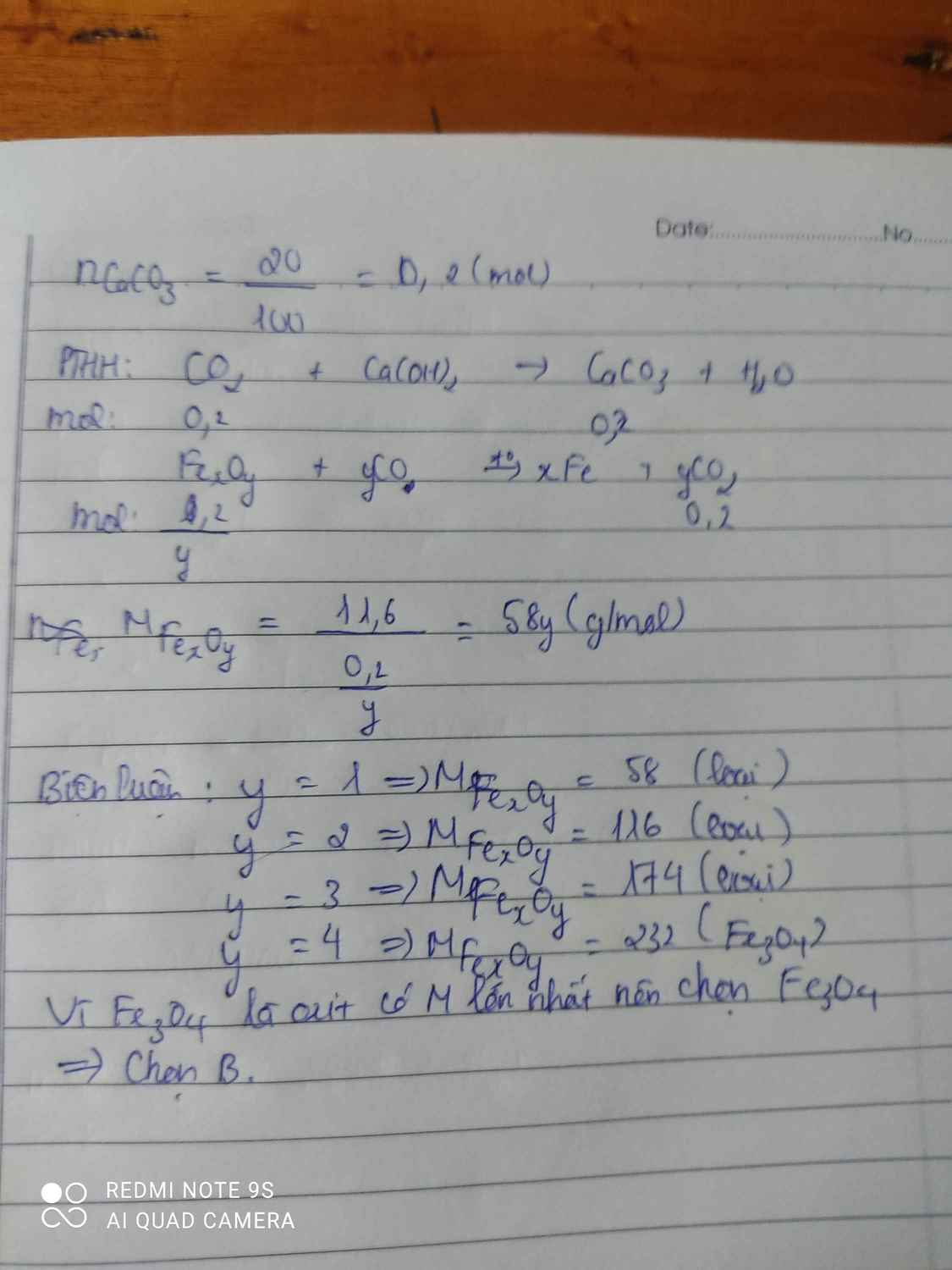khử hoàn toàn 8g oxit sắt bằng CO ở nhiệt độ cao. Sản phẩm khí dẫn vào nước vôi trong dư, tạo ra 15g kết tủa. Xác định CTPT của oxit sắt?

Những câu hỏi liên quan
Khử hoàn toàn 0,1 mol oxit sắt bằng khí CO ở nhiệt độ cao, rồi dẫn sản phẩm tạo thành vào dung dịch nước vôi trong dư, thấy tạo thành 30 gam kết tủa. Xác định công thức của oxit sắt.
A. Fe2O3
B. FeO
C. Fe3O4
D. Cả A và B
Đáp án A
Phản ứng:
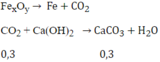
![]()
Cứ 0,1 mol có 0,3 mol nguyên tử O ⇒ y = 3 ⇒ x = 2
Công thức của oxit là Fe2O3
Đúng 0
Bình luận (0)
Khử hoàn toàn 11,6g oxit sắt bằng CO ở nhiệt độ cao. Sản phẩm khí dẫn vào dung dịch Ca(OH)2 dư, tạo ra 20g kết tủa. Công thức của oxit sắt là:
a FeO
b Fe3O4
c Fe2O3
d Không xác định được
Cách khác:
\(Đặt.CTTQ: Fe_xO_y\left(x,y:nguyên,dương\right)\\ y=n_{CO}=n_{CO_2}=n_{CaCO_3}=\dfrac{20}{100}=0,2\left(mol\right)\\ x=n_{Fe}=\dfrac{11,6-0,2.16}{2}=0,15\left(mol\right)\\ \Rightarrow x:y=0,15:0,2=3 :4\\ \Rightarrow x=3;y=4\\ \Rightarrow CTHH:Fe_3O_4\\ \Rightarrow B\)
Đúng 4
Bình luận (0)
vì Ca(OH)2 dư
=>CO2 dư ->n CO2= n CaCO3=0,2 mol
Bảo toàn O
=>n O (Oxit sắt ) = n CO2= 0,2 mol
->n Fe=\(\dfrac{11,6-0,2.16}{56}\)=0,15 mol
=>\(\dfrac{n_{Fe}}{n_O}\)=\(\dfrac{0,15}{0,2}=\dfrac{3}{4}\)
=>oxit là Fe3O4
Đúng 5
Bình luận (0)
khử hoàn toàn 16g một oxit sắt nguyên chất bằng khí CO ở nhiệt độ cao. Sau đó dẫn toàn bộ khí thu được qua bình đựng nước vôi trong dư, kết thúc phản ứng thu được 10g kết tủa. Xác định công thức oxit sắt
Khử hoàn toàn 16g 1 oxit sắt bằng khí Co ở nhiệt độ cao sau khi phản ứng kết thúc thấy khối lượng chất rắn còn lại là 11,2g.
a) Xác định CTHH của oxit đó.
b) chất khí sinh ra được dẫn vào dung dịch nước vôi trong lấy dư. Tính khối lượng chất kết tủa tạo thành
nFe = 11,2/56 = 0,2 mol , Gọi CT Oxit sắt là Fe2OnII
PTPƯ: Fe2On + nCO ---> 2Fe + nCO2
0,2 mol Fe -----> 0,1 mol Fe2On
MFe2On =16/0,1= 160 g/mol
⇒ 112 + 16n = 160 ⇒ 16n =48 ⇒n=3
⇒ CTHH: Fe2O3
Đúng 1
Bình luận (0)
Câu 4: Khử hoàn toàn 4,64 gam hỗn hợp các oxit của sắt bằng nhiệt độ cao. Khí sinh ra sau phản ứng được dẫn vào bình đựng nước vôi trong dư thu được 8g kết tủa. Khối lượng sắt sau phản ứng?
Theo gt ta có: $n_{CaCO_3}=n_{CO_2}=0,08(mol)$ (Bảo toàn nguyên tố C)
$Fe_xO_y+yCO\rightarrow xFe+yCO_2$
Nhận thấy $n_{O}=n_{CO_2}=0,08(mol)$
Do đó $m_{Fe}=m_{oxit}-m_{O}=3,12(g)$
Đúng 2
Bình luận (0)
Khử hoàn toàn 12 gam bột một loại oxit sắt bằng khí CO dư, sau khi phản ứng kết thúc, toàn bộ khí thoát ra được dẫn vào dung dịch nước vôi trong dư thu được 22,5 gam kết tủa. Xác định công thức của oxit sắt
Xem chi tiết
Oxit sắt : FexOy
\(CO_2 + Ca(OH)_2 \to CaCO_3 + H_2O\\ n_{CO_2} = n_{CaCO_3} =\dfrac{22,5}{100} = 0,225(mol)\\ Fe_xO_y + yCO \xrightarrow{t^o} xFe + yCO_2\\ n_{oxit} = \dfrac{n_{CO_2}}{y} = \dfrac{0,225}{y}(mol)\\ \Rightarrow \dfrac{0,225}{y}(56x + 16y) = 12\\ \Rightarrow \dfrac{x}{y} = \dfrac{2}{3}\)
Vậy CTHH của oxit : Fe2O3
Đúng 4
Bình luận (1)
Gọi oxit sắt là: FexOy.
PT: FexOy + yCO → xFe + yCO2 (1)
CO2 + Ca(OH)2 → CaCO3 + H2O (2)
Ta có: nCaCO3=22,5/100=0,225(mol)
Theo PT(2), ta có: nCO2=nCaCO3=0,225(mol)
Ta có: noxit sắt=0,225 . 1/y=0,225/y
=> (0,225/y)(56x + 16y)=12
Xét PT trên, ta có: x/y=2/3
=> x=2, y=3.
=> CTHH của oxit sắt là: Fe2O3.
Đúng 1
Bình luận (0)
. Khử hoàn toàn 16 gam một oxit sắt bằng khí CO ở nhiệt độ cao. Sau khi phản ứng kết thúc, thấy khối lượng chất rắn giảm 4,8 gam. Dẫn toàn bộ chất khí sinh ra vào bình đựng dung dịch Ca(OH)2 dư thu được m gam kết tủa trắng.a) Xác định CTPT của oxit sắt và tính m.b) Tính thể tích khí CO (đktc) đã dùng cho phản ứng khử nói trên, biết rằng người ta đã dùng dư khí CO 10% so với lý thuyết.
Đọc tiếp
. Khử hoàn toàn 16 gam một oxit sắt bằng khí CO ở nhiệt độ cao. Sau khi phản ứng kết thúc, thấy khối lượng chất rắn giảm 4,8 gam. Dẫn toàn bộ chất khí sinh ra vào bình đựng dung dịch Ca(OH)2 dư thu được m gam kết tủa trắng.
a) Xác định CTPT của oxit sắt và tính m.
b) Tính thể tích khí CO (đktc) đã dùng cho phản ứng khử nói trên, biết rằng người ta đã dùng dư khí CO 10% so với lý thuyết.
a)
CTHH: FexOy
\(n_{Fe_xO_y}=\dfrac{16}{56x+16y}\left(mol\right)\)
PTHH: FexOy + yCO --to--> xFe + yCO2
\(\dfrac{16}{56x+16y}\)--------->\(\dfrac{16x}{56x+16y}\)
=> \(\dfrac{16x}{56x+16y}.56=16-4,8=11,2\)
=> \(\dfrac{x}{y}=\dfrac{2}{3}\Rightarrow Fe_2O_3\)
\(n_{Fe_2O_3}=\dfrac{16}{160}=0,1\left(mol\right)\)
PTHH: Fe2O3 + 3CO --to--> 2Fe + 3CO2
0,1------>0,3--------------->0,3
Ca(OH)2 + CO2 --> CaCO3 + H2O
0,3----->0,3
=> \(m_{CaCO_3}=0,3.100=30\left(g\right)\)
b) nCO (thực tế) = 0,3.110% = 0,33(mol)
=> VCO = 0,33.22,4 = 7,392(l)
Đúng 6
Bình luận (0)
Khử hoàn toàn 4,06 gam một oxit sắt bằng khí CO dư ở nhiệt độ cao thành kim loại . Dẫn toàn bộ khí sinh ra vào bình đựng dd ca(oh)2 dư . Thấy tạo thành 7(g) kết rủa a) xác định công thức oxit sắt B) cho 4,06 g oxit sắt trên tác dụng hoàn toàn với dd H2SO4 đặc nóng
`a)`
Oxit: `Fe_xO_y`
`Fe_xO_y+yCO` $\xrightarrow{t^o}$ `xFe+yCO_2`
`CO_2+Ca(OH)_2->CaCO_3+H_2O`
Theo PT: `n_{CO_2}=n_{CaCO_3}=7/{100}=0,07(mol)`
`->n_{Fe_xO_y}={n_{CO_2}}/y={0,07}/y(mol)`
`->M_{Fe_xO_y}={4,06}/{{0,07}/y}=58y`
`->56x+16y=58y`
`->x/y={42}/{56}=3/4`
`->` Oxit: `Fe_3O_4`
`b)`
`n_{Fe_3O_4}={4,06}/{232}=0,0175(mol)`
`2Fe_3O_4+10H_2SO_4->3Fe_2(SO_4)_3+SO_2+10H_2O`
Đề thiếu.
Đúng 1
Bình luận (0)
a)Cho 0,3mol FexOy tham gia phản ứng nhiệt nhôm thấy tạo ra 0,4mol Al2O3. Xác định công thức oxit sắt?
b)Đốt cháy ko hoàn toàn 1 lượng sắt đã dùng hết 2,24 lít O2 ở đktc, thu đc hỗn hợp A gồm các oxit sắt và sắt dư. Khử hoàn toàn A bằng khí CO dư, khí đi ra sau pứ đc dãn vào bình đựng nước vôi trong dư. Tính khối lượng kết tủa thu đc