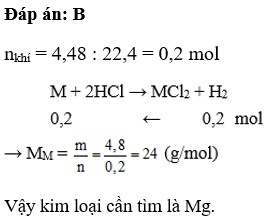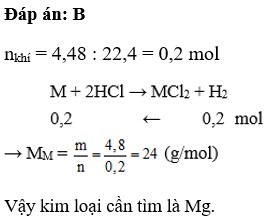Cho 4,8g kim loại M có hóa trị II vào dung dich HCl dư, thấy thoát ra 4.48 lít khí Hydro(ở đktc). Vậy kim loại M là
A. Ca B. Mg C. Fe D. Ba

Những câu hỏi liên quan
Cho 4,8 gam kim loại M có hóa trị II vào dung dịch HCl dư , thấy thoát ra 4,48 lít khí hiđro (ở đktc). Vậy kim loại M là
A. Ca
B. Mg
C. Fe
D. Ba
Cho 16,2 gam kim loại M có hóa trị n tác dụng với 0,15 mol O2. Chất rắn thu được sau phản ứng đem hòa tan vào dung dịch HCl dư thấy thoát ra 13,44 lít khí H2 đktc. Kim loại M là kim loại nào sau đây?
A. Fe.
B. Al.
C. Ca.
D. Mg.
Đáp án B.
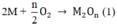
Chất rắn sau phản ứng hòa tan trong HCl thấy có khí thoát ra chứng ở có M dư
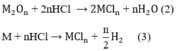
Số mol H2: 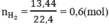
Theo phương trình (1)
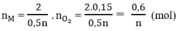
Theo phương trình (3)
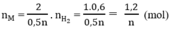
Tổng số mol M là 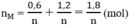
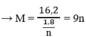
⇒ Giá trị thỏa mãn là n = 3, M = 27 M : Al
Đúng 1
Bình luận (0)
Cho 4,8g kim loại A hoá trị II vào dung dịch HCl dư thấy thoát ra 4,48g khí H2 ở đktc .Xác định kim loại A
Xem thêm câu trả lời
Cho 16,2 gam kim loại M có hóa trị n tác dụng với 0,15 mol O2. Chất rắn thu được sau phản ứng đem hòa tan vào dung dịch HCl dư thấy thoát ra 13,44 lít H2 (đktc). Kim loại M là
A. Fe
B. Al
C. Ca
D. Mg
Cho 16,2 gam kim loại M có hóa trị n tác dụng với 0,15 mol O2. Chất rắn thu được sau phản ứng đem hòa tan vào dung dịch HCl dư thấy thoát ra 13,44 lít H2 (đktc). Kim loại M là
A. Fe
B. Al
C. Ca
D. Mg
Đúng 0
Bình luận (0)
1) Cho 1,2 gam kim loại x có hóa trị II tác dụng dung dịch axit clo Hidric( dư), thoát ra 0,672 lít khí (đktc). kim loại X là?a) Zn65b) Mg24c) Ca40d) Fe56Tại sao chọn đáp án này?2) Cho 47,5 gam muối clorua của kim loại X có hóa trị II tác dụng với dung dịch Natri HIdroxit (dư) thu được 29 gam kết tủa trắng. Kim loại X là:a) Zn65b) Mg24c) Ca40d) Fe56Tại sao chọn đáp án này?3) Cho sơ đồ phản ứng hóa học: Cu(NO3)2- CuO+O2+NO2. Số mol Cu(NO3)2 cần dùng để điều chế 0,15 mol O2 là:a) 0,2 molb) 0,3 mo...
Đọc tiếp
1) Cho 1,2 gam kim loại x có hóa trị II tác dụng dung dịch axit clo Hidric( dư), thoát ra 0,672 lít khí (đktc). kim loại X là?
a) Zn=65
b) Mg=24
c) Ca=40
d) Fe=56
Tại sao chọn đáp án này?
2) Cho 47,5 gam muối clorua của kim loại X có hóa trị II tác dụng với dung dịch Natri HIdroxit (dư) thu được 29 gam kết tủa trắng. Kim loại X là:
a) Zn=65
b) Mg=24
c) Ca=40
d) Fe=56
Tại sao chọn đáp án này?
3) Cho sơ đồ phản ứng hóa học: Cu(NO3)2-> CuO+O2+NO2. Số mol Cu(NO3)2 cần dùng để điều chế 0,15 mol O2 là:
a) 0,2 mol
b) 0,3 mol
c) 0,1 mol
d) 0,05 mol
Tại sao chọn đáp án này?
1.
\(n_{H_2}=\dfrac{0.672}{22.4}=0.03\left(mol\right)\)
\(X+2HCl\rightarrow XCl_2+H_2\)
\(0.03.........................0.03\)
\(M_X=\dfrac{1.2}{0.03}=40\)
\(X:Ca\)
2.
\(CT:XCl_2\)
\(XCl_2+2NaOH\rightarrow X\left(OH\right)_2+2NaCl\)
\(X+71.........................X+34\)
\(47.5.............................29\)
\(29\cdot\left(X+71\right)=47.5\cdot\left(X+34\right)\)
\(\Rightarrow X=24\)
\(X:Mg\)
3.
\(2Cu\left(NO_3\right)_2\underrightarrow{^{^{t^0}}}2CuO+4NO_2+O_2\)
\(0.3..........................................0.15\)
\(n=0.3\)
Đúng 1
Bình luận (1)
Cho 2g hỗn hợp gồm Fe và một kim loại Z hóa trị II vào dung dịch HCl dư thì thu được 1,12 lít khí (đktc). Xác định kim loại Z biết rằng 500ml dung dịch HCl hòa tan dư 4,8g kim loại đó
Sửa đề : Xác định kim loại Z biết rằng 500ml dung dịch HCl 1M hòa tan dư 4,8g kim loại đó
nH2=0,05 mol
PTHH:
Fe+2HCl→FeCl2+H2↑
Z + 2HCl →ZCl2+H2↑
Đặt công thức chung của hỗn hợp là N
N + 2HCl → NCl2 + H2
0,05______________0,05
⇒MN=\(\dfrac{2}{0,05}\)=40
Vì MFe =56>40
⇒MZ <40 (1)
Ta có : nHCl<0,5.1=0,5 mol
Z + 2HCl →ZCl2+H2↑
=> nZ < 0,25
=> MZ >\(\dfrac{4,8}{0,25}=19,2\)(2)
Từ (1), (2), ta có 19,2<MZ <40
Mà Z hóa trị II
⇒Z là Magie
Đúng 1
Bình luận (1)
Cho 12,4 gam hỗn hợp gồm 2 kim loại là A (hóa trị II) và đồng phản ứng với lượng dư dung dịch HCl, sau phản ứng thấy trong dung dịch có 6,4 gam chất rắn không tan và thoát ra 5,6 lít khí không màu ở đktc. Xác định tên kim loại A giup em a
Đọc tiếp
Cho 12,4 gam hỗn hợp gồm 2 kim loại là A (hóa trị II) và đồng phản ứng với lượng dư dung dịch HCl, sau phản ứng thấy trong dung dịch có 6,4 gam chất rắn không tan và thoát ra 5,6 lít khí không màu ở đktc. Xác định tên kim loại A
giup em a
Câu 1. Cho 2g hỗn hợp 2 kim loại Fe là kim loại hóa trị II vào dung dịch HCl dư thì thu được 1,12l khí H2(ĐKTC). Mặt khác nếu hòa tan 4,8g kim loại hóa trị II đó thì cần chưa tới 500ml dung dịch HCl 1M. Xác định kim loại hóa trị II.
Giúp MK với!!!
Hòa tan hoàn toàn 0,5 gam Fe và một kim loại hóa trị II trong dung dịch HCl thu được 1,12 lít khí H2 đktc. Kim loại hóa trị II đó là kim loại nào sau đây.
A. Mg.
B. Ca.
C. Zn.
D. Be.
Đáp án D.
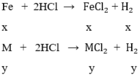
gọi x, y lần lượt là số mol của Fe và M trong hỗn hợp
số mol H2 là 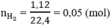
theo bài ra ta có hệ phương trình
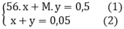
từ (2) → x= 0,05 – y
thay vào (1) ta được 56(0,05 – y) + My = 0,5
⇔ 2,8 – 56y + My = 0,5
2,3 = 56y – My
→ y = 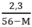
Ta có 0 < y < 0,05
y > 0 ↔ 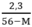 > 0 → 56 – M > 0 ⇒ M < 56
> 0 → 56 – M > 0 ⇒ M < 56
y < 0,05 ↔ 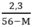 < 0,05 → 2,3 < 0,05(56 – M) → M < 10
< 0,05 → 2,3 < 0,05(56 – M) → M < 10
Trong các kim loại hóa trị II chỉ có Be thỏa mãn do đó M là Be
Đúng 0
Bình luận (0)