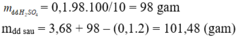Cho hỗn hợp 10g Al và Cu tác dụng vừa đủ với dung dịch H2SO4 thì thu được 6,72 lít khí H2. Khối lượng Cu và Al lần lượt là bao nhiêu?

Những câu hỏi liên quan
Cho 33,2g hỗn hợp X gồm Cu, Mg, Al tác dụng vừa đủ với dung dịch H2SO4 loãng thu được 22,4 lít khí ở đktc và chất rắn không tan B. Cho B hoà tan hoàn toàn vào dung dịch H2SO4 đặc, nóng dư thu được 4,48 lít khí SO2(đktc). Khối lượng mỗi kim loại trong hỗn hợp X lần lượt là: A. 13,8;7,6;11,8 B. 11,8;9,6;11,8 C. 12,8;9,6;10,8 D. kết quả khác
Đọc tiếp
Cho 33,2g hỗn hợp X gồm Cu, Mg, Al tác dụng vừa đủ với dung dịch H2SO4 loãng thu được 22,4 lít khí ở đktc và chất rắn không tan B. Cho B hoà tan hoàn toàn vào dung dịch H2SO4 đặc, nóng dư thu được 4,48 lít khí SO2(đktc). Khối lượng mỗi kim loại trong hỗn hợp X lần lượt là:
A. 13,8;7,6;11,8
B. 11,8;9,6;11,8
C. 12,8;9,6;10,8
D. kết quả khác
Đáp án C.
Kim loại không phản ứng với H2SO4 loãng là Cu.
Gọi nCu = x, nMg = y, nAl = z
Ta có:
64x + 24y + 27z = 33,2 (1)
Bảo toàn e:
2nMg + 3nAl = 2nH2
=> 2y + 3z = 2.1 (2)
2nCu = 2nSO2 => x = 0.2 (mol) (3)
Từ 1, 2, 3 => x = 0,2; y = z = 0,4 (mol)
mCu = 0,2.64 = 12,8 (g)
mMg = 0,4.24 = 9,6 (g)
mAl = 10,8 (g)
Đúng 0
Bình luận (0)
Cho hỗn hợp A có khối lượng là 32,8 gồm ( Al, Fe, Cu) tác dụng với dung dịch NaOH thì thu được 6,72 lít khí H2 thoát ra ở đktc. Nếu đem hỗn hợp trên tác dụng với dung dịch HCl thì sinh ra 10,08 lít khí H2 thoát ra ở đktc. Tính % khối lượng mỗi kim loại trong hỗn hợp.
2Al + 2H2O + 2NaOH→ 3H2 + 2NaAlO2
0,2mol 0,3mol
mAl=0,2.27=5,4g
2Al + 6HCl→ 2AlCl3+ 3H2
0,2mol 0,3mol
Fe + 2HCl→ FeCl2+ H2
0,15mol 0,45-0,3 mol
mFe=0,15.56=8,4g
mCu=32,8-(6,4+8,4)=18g
%mFe=\(\frac{8,4}{32,8}.100=25,6\%\)
%mCu=\(\frac{18}{32,8}.100=54,8\%\)
%mAl=19,6%
Đúng 1
Bình luận (0)
Cho 33,2 g hỗn hợp X gồm Cu, Mg, Al tác dụng vừa đủ với dung dịch HCl thu được V lít khí ở đktc và chất rắn không tan Y. Cho Y hoà tan hoàn toàn vào dung dịch H2SO4 đặc, nóng dư thu được 4,48 lít khí SO2 (đktc). Phần trăm khối lượng của Cu trong hỗn hợp X là A. 57,83%. B. 33,33%. C. 19,28%. D. 38,55%.
Đọc tiếp
Cho 33,2 g hỗn hợp X gồm Cu, Mg, Al tác dụng vừa đủ với dung dịch HCl thu được V lít khí ở đktc và chất rắn không tan Y. Cho Y hoà tan hoàn toàn vào dung dịch H2SO4 đặc, nóng dư thu được 4,48 lít khí SO2 (đktc). Phần trăm khối lượng của Cu trong hỗn hợp X là
A. 57,83%.
B. 33,33%.
C. 19,28%.
D. 38,55%.
Cho 20 gam hỗn hợp Cu và Al phản ứng với dung dịch H 2 S O 4 loãng, dư thấy thu được 13,44 lít khí (đktc). % theo khối lượng Al và Cu trong hỗn hợp lần lượt là
A. 44% và 66%.
B. 54% và 46%.
C. 50% và 50%.
D. 94% và 16%.
Cho 24,6 gam hỗn hợp Al và Cu tác dụng vừa đủ với dung dịch HNO3 loãng 25% thì thu được 8,96
lít khí NO duy nhất thoát ra (ở đktc) và ddA.
a) Tính % khối lượng của Al và Cu trong hỗn hợp.
b) Tính C % từng chất trong dung dịch A thu được sau phản ứng biết axit vừa đủ.
c. Lấy 1/2 dung dịch A cô cạn thu được m1 gam chất rắn, đun nóng chất rắn tới khối lượng không đổi thu
được m2 gam. Hỏi khối lượng m2 so với m1 tăng hay giảm bao nhiêu gam ?
Đọc tiếp
Cho 24,6 gam hỗn hợp Al và Cu tác dụng vừa đủ với dung dịch HNO3 loãng 25% thì thu được 8,96 lít khí NO duy nhất thoát ra (ở đktc) và ddA. a) Tính % khối lượng của Al và Cu trong hỗn hợp. b) Tính C % từng chất trong dung dịch A thu được sau phản ứng biết axit vừa đủ. c. Lấy 1/2 dung dịch A cô cạn thu được m1 gam chất rắn, đun nóng chất rắn tới khối lượng không đổi thu được m2 gam. Hỏi khối lượng m2 so với m1 tăng hay giảm bao nhiêu gam ?
Giúp mình với
Bài 1: Cho 10g hỗn hợp hai kim loại: Al và Cu tác dụng với dd H2SO4 20%, thu được 6,72 lít khí H2 (ở đktc).
Viết PT phản ứng.
Tính khối lượng các chất có trong hỗn hợp.
Tính thành phần tram khối lượng mỗi kim loại trong hỗn hợp.
Tính khối lượng dd H2SO4 cần dùng.
\(n_{H_2}=\dfrac{6,72}{22,4}=0,3(mol)\\ 2Al+3H_2SO_4\to Al_2(SO_4)_3+3H_2\\ \Rightarrow n_{Al}=0,2(mol)\Rightarrow m_{Al}=0,2.27=5,4(g)\\ \Rightarrow m_{Cu}=10-5,4=4,6(g)\\ \Rightarrow \%_{Al}=\dfrac{5,4}{10}.100\%=54\%\\ \Rightarrow \%_{Cu}=100\%-54\%=46\%\\ n_{H_2SO_4}=0,3(mol)\Rightarrow m_{dd_{H_2SO_4}}=\dfrac{0,3.98}{20\%}=147(g)\)
Đúng 2
Bình luận (0)
Cho 10g hỗn hợp hai kim loại: Al và Cu tác dụng với dd H2SO4 20%, thu được 6,72 lít khí H2 (ở đktc).
a. Viết PT phản ứng.
b. Tính khối lượng các chất có trong hỗn hợp.
c. Tính thành phần tram khối lượng mỗi kim loại trong hỗn hợp.
d. Tính khối lượng dd H2SO4 cần dùng.
a. PTHH:
2Al + 3H2SO4 ---> Al2(SO4)3 + 3H2
Cu + H2SO4 ---x--->
b. Theo PT: \(n_{Al}=\dfrac{2}{3}.n_{H_2}=\dfrac{2}{3}.\dfrac{6,72}{22,4}=0,2\left(mol\right)\)
=> \(m_{Al}=0,2.27=5,4\left(g\right)\)
=> \(m_{Cu}=10-5,4=4,6\left(g\right)\)
c. \(\%_{m_{Al}}=\dfrac{5,4}{10}.100\%=54\%\)
\(\%_{m_{Cu}}=100\%-54\%=46\%\)
d. Theo PT: \(n_{H_2SO_4}=n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
=> \(m_{H_2SO_4}=0,3.98=29,4\left(g\right)\)
Ta có: \(C_{\%_{H_2SO_4}}=\dfrac{29,4}{m_{dd_{H_2SO_4}}}.100\%=20\%\)
=> \(m_{dd_{H_2SO_4}}=147\left(g\right)\)
Đúng 1
Bình luận (0)
Câu 5: Cho 65,4 gam hỗn hợp Al và Cu tác dụng vừa đủ với dung dịch HNO3 loãng thì thu được 31,36 lít khí NO thoát ra (đktc). % khối lượng của Cu trong hỗn hợp là . 17,42% B. 41,28 % C. 58,72% D. 50%.
\(Al\rightarrow Al^{3+}+3e\\ Cu\rightarrow Cu^{2+}+2e\\ N^{+5}+3e\rightarrow N^{+2}\\ Đặt:\left\{{}\begin{matrix}n_{Al}=x\left(mol\right)\\n_{Cu}=y\left(mol\right)\end{matrix}\right.\\ n_{NO}=\dfrac{31,36}{22,4}=1,4\left(mol\right)\\ BTe:3x+2y=1,4.3\\ Mặtkhác:27x+64y=65,4\\ \Rightarrow\left\{{}\begin{matrix}x=1\\y=0,6\end{matrix}\right.\\ \Rightarrow\%m_{Cu}=\dfrac{0,6.64}{65,4}.100=58,72\%\\ \Rightarrow ChọnC\)
Đúng 2
Bình luận (0)
Cho 3,68 gam hỗn hợp gồm Al và Zn tác dụng với một lượng vừa đủ dung dịch H2SO4 10%, thu được 2,24 lít khí H2 (đktc).Khối lượng dung dịch thu được sau phản ứng là A. 97,80 gam B. 101,48 gam C. 88,20 gam D. 101,68 gam
Đọc tiếp
Cho 3,68 gam hỗn hợp gồm Al và Zn tác dụng với một lượng vừa đủ dung dịch H2SO4 10%, thu được 2,24 lít khí H2 (đktc).Khối lượng dung dịch thu được sau phản ứng là
A. 97,80 gam
B. 101,48 gam
C. 88,20 gam
D. 101,68 gam