Trong phòng thí nghiệm điều chế oxi người ta sử dụng cụ và hóa chất nào?Tại sao ở miệng ống nghiệm lại có một miếng bông? Nếu các chất có khối lượng như nhau em chọn chất nào để điều chế khí oxi nhiều nhất?

Những câu hỏi liên quan
trong phòng thí nghiệm ngta thường nung KClO3 hoặc KMnO4 để điều chế khí oxi sử dụng cho các thí nghiệm khác, nếu ta sử dụng cùng số mol hai chất này để điều chế khí oxi thì trường hợp nào sẽ thu được khối lượng khí oxi là nhiều nhất? giải thích.
\(2KMnO_4\underrightarrow{^{t^0}}K_2MnO_4+MnO_2+O_2\)
\(\dfrac{a}{158}.............................\dfrac{a}{79}\)
\(2KClO_3\underrightarrow{^{t^0}}2KCl+3O_2\)
\(\dfrac{a}{122.5}............\dfrac{3a}{245}\)
\(TC:\)
\(\dfrac{a}{79}>\dfrac{3a}{245}\)
=> Lượng Cl2 điều chế từ KMnO4 lớn nhất.
Đúng 2
Bình luận (0)
Để điều chế cùng một lượng khí oxi trong phòng thí nghiệm, ta nên sử dụng nguyên liệu nào sau đây để khối lượng hóa chất cần dùng là nhỏ nhất?
bạn không nói rõ là nguyên liệu nào thì sao chọn được. Nhưng nếu so sánh giữa KMnO4,KClO3,KNO3 và H2O2 thì chọn H2O2 nhé
Đúng 0
Bình luận (2)
Bằng kiến thức hóa học, hãy cho biết một chất nào hoặc một cặp chất nào có thể tác dụng với nhau để : a) điều chế hiđro (H²) trong phòng thí nghiệm ? b) tạo thành dung dịch làm quỳ tím hóa đỏ ? c) điều chết khí oxi (O²) trong phòng thí nghiệm? d) chỉ sinh ra oxit ? Viết các phương trình phản ứng hóa học xảy ra và ghi rõ điều kiện ( nếu có ) .
\(a,Zn+H_2SO_4\rightarrow ZnSO_4+H_2\uparrow\\ b,CO_2+H_2O\rightarrow H_2CO_3\\ c,2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\\ C+O_2\underrightarrow{t^o}CO_2\)
Đúng 6
Bình luận (0)
Cho dung dịch axit sunfuric loãng, nhôm và các dụng cu thí nghiệm như hình vẽ. Hãy chọn câu trả lời đúng trong các câu sau: A. Có thể dùng các hóa chất và dụng cụ đã cho để điều chế và thu khí oxi. B. Có thể dùng các hóa chất và dụng cụ đã cho để điều chế và thu không khí. C. Có thể dùng các hóa chất và dụng cụ đã cho để điều chế và thu khí hiđro. D. Có thể dùng để điều chế hidro nhưng không thu được khí hiđro.
Đọc tiếp
Cho dung dịch axit sunfuric loãng, nhôm và các dụng cu thí nghiệm như hình vẽ. Hãy chọn câu trả lời đúng trong các câu sau:
A. Có thể dùng các hóa chất và dụng cụ đã cho để điều chế và thu khí oxi.
B. Có thể dùng các hóa chất và dụng cụ đã cho để điều chế và thu không khí.
C. Có thể dùng các hóa chất và dụng cụ đã cho để điều chế và thu khí hiđro.
D. Có thể dùng để điều chế hidro nhưng không thu được khí hiđro.
Câu trả lời đúng là C.
PT: 2Al + 3H2SO4 → Al2(SO4)3 + 3H2
Từ phản ứng này ⇒ có thể điều chế khí H2
Khí H2 nhẹ hơn không khí nên úp ngược ống nghiệm sẽ thu được khí H2
Đúng 0
Bình luận (0)
Cho hình vẽ sau: a. Nếu khí Y là khí oxi thì hình nào trên đây mô tả đúng sự điều chế oxi trong phòng thí nghiệm? Giải thích sự lựa chọn này. b. Viết hai phương trình hóa học điều chế khí oxi trong phòng thí nghiệm từ hai chất rắn X khác nhau.
Đọc tiếp
Cho hình vẽ sau:
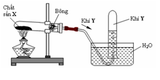
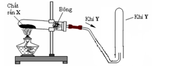
a. Nếu khí Y là khí oxi thì hình nào trên đây mô tả đúng sự điều chế oxi trong phòng thí nghiệm? Giải thích sự lựa chọn này.
b. Viết hai phương trình hóa học điều chế khí oxi trong phòng thí nghiệm từ hai chất rắn X khác nhau.
a. Khí O2 ít tan trong nước và nặng hơn không khí nên cách 1b không được (khi đó không khí sẽ xua hết khí O2 ra ngoài), trong phòng thí nghiệm người ta sử dụng cách 1a
b. Điều chế khí O2 người ta nhiệt phân các hợp chất giàu oxi: KMnO4; KClO3
Đúng 0
Bình luận (0)
Trong phòng thí nghiệm có các hóa chất KClO3 , MnO2 và dụng cụ cần thiết
a, Viết phương trình hóa học của phản ứng điều chế khí oxi
b, Hãy vẽ hình mô tả thí nghiệm điều chế và thu khí oxi bằng cách đẩy không khí
a) 2KClO3 -> 2KCl + 3O2
b) MnO2 + 4HCl -> MnCl2 + Cl2 + 2H2O
b) SGK
Đúng 0
Bình luận (1)
Trong phòng thí nghiệm có các hợp chất KClO3, KNO3, HgO. Muốn điều chế 3,36 lít khí oxi(đktc) theo em nên cho chất nào để tiết kiệm hóa chất nhất ???
nO2 = 3,36/22,4 = 0,15 (mol)
PTHH:
2KClO3 -> (t°) 2KCl + O2
0,1 <------------------------ 0,15
2KNO3 -> (t°) 2KNO2 + O2
0,3 <--------------------------- 0,15
2HgO -> (t°) 2Hg + O2
0,3 <---------------------- 0,15
So sánh: 0,1 < 0,3 = 0,3
=> Dùng KClO3 thì sẽ tiết kiệm nhất
Đúng 2
Bình luận (0)
PTHH
2KClO3 -to-> 2KCl + 3O2
0,1--------------------------0,15
2KNO3 -to-> 2KNO2 + O2
0,3-----------------------------0,15
2HgO -to-> 2Hg + O2
0,3---------------------0,15
ta cho mỗi khí ở ccas pt là như nhau
n O2=\(\dfrac{3,36}{22,4}\)=0,15 mol
=> ta suy ra khối lg thấy KClO3 là tiết kiệm nhất
Đúng 2
Bình luận (1)
Có những chất sau: KMnO4, MnO2, K2Cr2O7 và dung dịch HCl. a) Nếu các chất oxi hóa có khối lượng bằng nhau thì chọn chất nào có thể điều chế được lượng khí clo nhiều hơn? b) Nếu chất oxi hóa có số mol bằng nhau thì chọn chất nào có thể điều chế được lượng khí clo nhiều hơn? Hãy trả lời bằng cách tính toán trên cơ sở của các phương trình phản ứng.
Đọc tiếp
Có những chất sau: KMnO4, MnO2, K2Cr2O7 và dung dịch HCl.
a) Nếu các chất oxi hóa có khối lượng bằng nhau thì chọn chất nào có thể điều chế được lượng khí clo nhiều hơn?
b) Nếu chất oxi hóa có số mol bằng nhau thì chọn chất nào có thể điều chế được lượng khí clo nhiều hơn?
Hãy trả lời bằng cách tính toán trên cơ sở của các phương trình phản ứng.
a) Giả sử lấy lượng mỗi chất là a gam
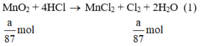
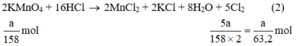
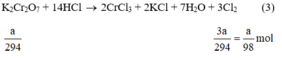
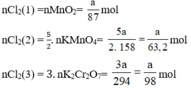
Ta có: 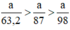
Lượng Cl2 điều chế được từ pt (2) nhiều nhất.
Vậy dùng KMnO4 điều chế được nhiều Cl2 hơn.
b) Nếu lấy số mol các chất bằng a mol
Theo (1) nCl2(1) = nMnO2 = a mol
Theo (2) nCl2(2) = 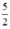 . nKMnO4 = 2,5a mol
. nKMnO4 = 2,5a mol
Theo (3) nCl2(3) = 3. nK2Cr2O7 = 3a mol
Ta có: 3a > 2,5a > a.
⇒ lượng Cl2 điều chế được từ pt (3) nhiều nhất.
Vậy dùng K2Cr2O7 được nhiều Cl2 hơn.
Đúng 0
Bình luận (0)
trong phòng thí nghiệm người ta điều chế oxi bằng cách nhiệt phân kmno4 hoặc kclo3.hỏi sử dụng khối lượng kmno4 và kclo3 bằng nhau thì cái nào thu khí oxi nhiều hơn
Hm....
KClO3 thu đc nhiều hơn




















