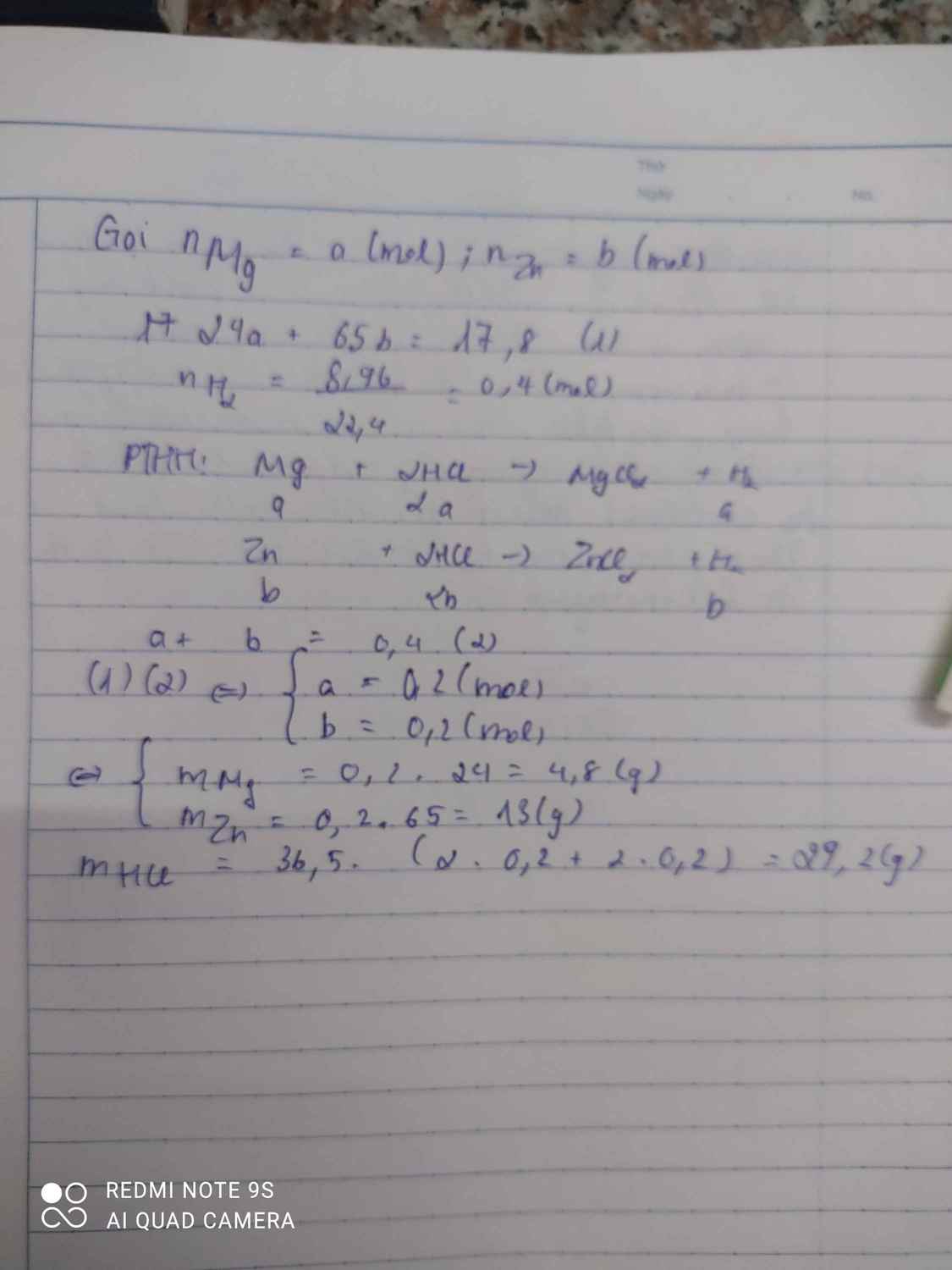cho a gam hỗn hợp gồm 2 kim loại A Và B tác dụng hết với dd HCL . sau khi phản ứng kết thúc , người ta thu được 67 gam muối và 8,96 lít H2 ĐKTC . viết PTHH , Tính A

Những câu hỏi liên quan
1/ Cho a gam hỗn hợp gồm 2 kim loại A và B (chưa rõ hóa trị) tác dụng hết với dung dịch HCl (Cả A và B đều phản ứng). Sau khi phản ứng kết thúc, người ta chỉ thu được 67 gam muối và 8,96 lít H2 (đktc)a. Viết các PTHHb. Tính a ?2/ Dùng khí CO để khử hoàn toàn 20g 1 hỗn hợp Y gồm CuO và Fe2O3 ở nhiệt độ cao. Sau phản ứng, thu được chất rắn chỉ là các kim loại, lượng kim loại này cho phản ứng với dung dịch H2SO4 loãn (lấy dư) thì thấy có 3,2g một kim loại màu đỏ không tana. Tính thành phần % khối l...
Đọc tiếp
1/ Cho a gam hỗn hợp gồm 2 kim loại A và B (chưa rõ hóa trị) tác dụng hết với dung dịch HCl (Cả A và B đều phản ứng). Sau khi phản ứng kết thúc, người ta chỉ thu được 67 gam muối và 8,96 lít H2 (đktc)
a. Viết các PTHH
b. Tính a ?
2/ Dùng khí CO để khử hoàn toàn 20g 1 hỗn hợp Y gồm CuO và Fe2O3 ở nhiệt độ cao. Sau phản ứng, thu được chất rắn chỉ là các kim loại, lượng kim loại này cho phản ứng với dung dịch H2SO4 loãn (lấy dư) thì thấy có 3,2g một kim loại màu đỏ không tan
a. Tính thành phần % khối lượng các chất có trong hỗn hợp Y
b. Nếu dùng khí sản phẩm ở các phản ứng khử Y, cho đi qua dung dịch Ca(OH)2 dư thì thu được bao nhiêu gam kết tủa. Biế hiệu suất của phản ứng này chỉ đạt 80%
Câu 1:
a) PTHH: \(2A+2xHCl\rightarrow2ACl_x+xH_2\uparrow\)
\(2B+2yHCl\rightarrow2BCl_y+yH_2\uparrow\)
b) Ta có: \(n_{H_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\) \(\Rightarrow m_{H_2}=0,4\cdot2=0,8\left(g\right)\)
Theo các PTHH: \(n_{HCl}=2n_{H_2}=0,8\left(mol\right)\) \(\Rightarrow m_{HCl}=0,8\cdot36,5=29,2\left(g\right)\)
Bảo toàn khối lượng: \(a=m_{KL}=m_{muối}+m_{H_2}-m_{HCl}=38,6\left(g\right)\)
Đúng 1
Bình luận (0)
hòa tan hết một gam hồn hợp gồm 2 kim loại A và B (chưa rõ hóa trị) vào dd HCI. Sau khi phản ứng kết thúc thu được m gam muối clorua và 8,96 lít H2 ( dktc )
a) Viết pthh
b) Tính a (biết a = 57,61 %m)
Cho 7,8 gam hỗn hợp hai kim loại là Mg và Al tác dụng với dung dịch H 2 SO 4 loãng, dư. Khi phản ứng kết thúc, người ta thu được 8,96 lít khí (đktc). Viết PTHH của các phản ứng đã xảy ra.
Các PTHH :
Mg + H 2 SO 4 → Mg SO 4 + H 2 (1)
2Al + 3 H 2 SO 4 → Al 2 SO 4 3 + 3 H 2 (2)
Đúng 0
Bình luận (0)
Cho 13,8 gam hỗn hợp X gồm kim loại kiềm R và Ca tác dụng hết với nước thu được 5,6 lít H2 (đktc) và dung dịch Y. Mặt khác, cho 8,58 gam kim loại R phản ứng hết với lượng dư dung dịch HCl thì thể tích khí H2 thoát ra lớn hơn 2,24 lít (đktc). 1. Tìm kim loại R? 2. Cho 15 lít hỗn hợp khí Z gồm N2 và CO2 (đktc) vào dung dịch Y. Sau khi phản ứng kết thúc thu được 8,5 gam kết tủa. Tính thành phần phần trăm về thể tích của mỗi khí trong hỗn hợp Z?
Đọc tiếp
Cho 13,8 gam hỗn hợp X gồm kim loại kiềm R và Ca tác dụng hết với nước thu được 5,6 lít H2 (đktc) và dung dịch Y. Mặt khác, cho 8,58 gam kim loại R phản ứng hết với lượng dư dung dịch HCl thì thể tích khí H2 thoát ra lớn hơn 2,24 lít (đktc).
1. Tìm kim loại R?
2. Cho 15 lít hỗn hợp khí Z gồm N2 và CO2 (đktc) vào dung dịch Y. Sau khi phản ứng kết thúc thu được 8,5 gam kết tủa. Tính thành phần phần trăm về thể tích của mỗi khí trong hỗn hợp Z?
1.
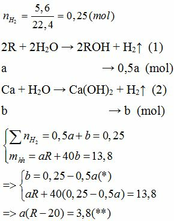
Vì b > 0, từ (*) => a < 0,25/0,5 = 0,5 thế vào (**)
=> R – 20 > 7,6
=> R > 27,6 (***)
Khi cho 8,58 gam R tác dụng với lượng dư HCl thì lượng H2 thoát ra lớn hơn 2,24 (lít)
2R + 2HCl → 2RCl + H2↑ (3)
Theo PTHH (3):
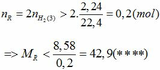
Từ (***) và (****) => 27, 6 < MR < 42,9
Vậy MR = 39 (K) thỏa mãn
2.
Ta có:
=> nKOH = nK = 0,2 (mol)
nCa(OH)2 = nCa = 0,15 (mol)
∑ nOH- = nKOH + 2nCa(OH)2 = 0,2 + 2.0,15 = 0,5 (mol)
Khi cho hỗn hợp Z ( N2, CO2) vào hỗn hợp Y chỉ có CO2 phản ứng
CO2 + OH- → HCO3- (3)
CO2 + 2OH- → CO32- + H2O (4)
CO32- + Ca2+ → CaCO3↓ (5)
nCaCO3 = 8,5/100 = 0,085 (mol) => nCO32-(5) = nCaCO3 = 0,085 (mol)
Ta thấy nCaCO3 < nCa2+ => phương trình (5) Ca2+ dư, CO32- phản ứng hết
TH1: CO2 tác dụng với OH- chỉ xảy ra phản ứng (4)
Theo (4) => nCO2 = nCO32-(4) = nCaCO3 = 0,085 (mol)
=> VCO2(đktc) = 0,085.22,4 = 1,904 (lít)
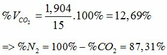
TH2: CO2 tác dụng với OH- xảy ra cả phương trình (3) và (4)
Theo (4): nCO2 = nCO32- = 0,085 (mol)
nOH- (4) = 2nCO32- = 2. 0,085 = 0,17 (mol)
=> nOH- (3)= ∑ nOH- - nOH-(4) = 0,5 – 0,17 = 0,33 (mol)
Theo PTHH (3): nCO2(3) = nOH- = 0,33 (mol)
=> ∑ nCO2(3+4) = 0,085 + 0,33 = 0,415 (mol)
=> VCO2 (ĐKTC) = 0,415.22,4 = 9,296 (lít)
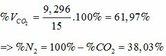
Đúng 0
Bình luận (0)
BT4.cho hỗn hợp A gồm 17,8 gam Mg và Zn tác dụng vs dung dịch HCl dư . sau phản ứng thu đc 8,96 lít H2 (đktc)
a) viết PTHH của phản ứng xảy ra .
b) tính khối lượng mỗi kim loại trong hỗn hợp A.
c)tính khối lượng HCl tối thiểu cần dùng .
lm giúp mik vsssssssss
Mg+2HCl->MgCl2+H2
x------------------------x
Zn+2HCl->ZnCl2+H2
y-------------------------y
Ta có :
\(\left\{{}\begin{matrix}24x+65y=17,8\\x+y=\dfrac{8,96}{22,4}\end{matrix}\right.\)
=>x=0,2 mol, y=0,2 mol
=>mMg=0,2.24=4,8g
=>m Zn=0,2.65=13g
=>m HCl=0,8.36,5=29,2g
Đúng 4
Bình luận (0)
Cho a gam hỗn hợp gồm 2 kim loại A và B (chưa rõ hoá trị) tác dụng hết với dd HCl (cả A và B đều phản ứng). Sau khi phản ứng kết thúc, người ta chỉ thu được 67 gam muối và 8,96lít H2 (ĐKTC).
a. Viết các phương trình hoá học ?
b. Tính a ?
a) gọi hóa trị của kim loại A là x , của kim loại B là y
PTHH:
2A + 2xHCl \(\rightarrow\) 2AClx + xH2 (1)
2B + 2yHCl \(\rightarrow\) 2BCly + yH2 (2)
b) nH2 = V/22,4 = 8,96/22,4 = 0,4(mol) => mH2 = 0,4 x 2 = 0,8(g)
Theo PT(1)(2) => nHCl = 2nH2 = 2 . 0,4 = 0,8(mol)
=> mHCl = 0,8 x 36,5 =29,2(g)
Theo ĐLBTKL :
mhỗn hợp 2 kim loại + mHCl = m2 muối + mH2
=> a + 29,2 = 67 + 0,8 => a =38,6(g)
Đúng 0
Bình luận (5)
Cho 7,8 gam hỗn hợp hai kim loại Mg và Al tác dụng với dung dịch H2SO4 loãng dư. Khi phản ứng kết thúc người ta thu được 8,96 lít khí (đktc).
a. Viết các phương trình hoá học xảy ra
b. Tính khối lượng mỗi kim loại trong hỗn hợp ban đầu.
c. Tính thể tích dung dịch H2SO4 2 M đã tham gia phản ứng
a)
2Al + 3H2SO4 → Al2(SO4)3 +3H2
Mg + H2SO4 → MgSO4 + H2
b. n H2 = 8,96/22,4 =0,4 mol
Gọi x và y là số mol của Al và Mg ta có hệ
27x+ 24y = 7,8 (1)
1,5x+ y = 0,4 (2)
Từ 1 và 2 => x = 0,2 ; y = 0,1
Khối lượng của Al và Mg là:
mAg = 0,2.27=5,4(gam)
mMg = 7,8 – 5,4 = 2,4(gam)
c. Theo phương trình số mol của H2SO4 là : 0,3 + 0,1 = 0,4(mol)
Thể tích dung dịch H2SO4 2M đã tham gia phản ứng là:
V = 0,4/2=0,2 lít
Đúng 3
Bình luận (1)
Gọi nMg = a (mol); nAl = b (mol)
=> 24a + 27b = 7,8 (1)
nH2 = 8,96/22,4 = 0,4 (mol)
PTHH:
Mg + H2SO4 -> MgSO4 + H2
a ---> a ---> a ---> a
2Al + 3H2SO4 -> 2Al2(SO4)3 + 3H2
b ---> 1,5b ---> b ---> 1,5b
=> a + 1,5b = 0,4 (2)
(1)(2) => a = 0,1 (mol); b = 0,2 (mol)
mMg = 0,1 . 24 = 2,4 (g)
mAl = 0,2 . 27 = 5,4 (g)
nH2SO4 = 0,1 + 0,3 . 1,5 = 0,4 (mol)
VddH2SO4 = 0,3/2 = 0,2 (l)
Đúng 4
Bình luận (7)
a.b.\(n_{H_2}=\dfrac{8,96}{22,4}=0,4mol\)
Gọi \(\left\{{}\begin{matrix}n_{Mg}=x\\n_{Al}=y\end{matrix}\right.\)
\(Mg+H_2SO_4\left(l\right)\rightarrow MgSO_4+H_2\)
x x ( mol )
\(2Al+3H_2SO_4\left(l\right)\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
y 3/2y ( mol )
Ta có:
\(\left\{{}\begin{matrix}24x+27y=7,8\\x+\dfrac{3}{2}y=0,4\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}x=0,1\\y=0,2\end{matrix}\right.\)
\(\Rightarrow m_{Mg}=0,1.24=2,4g\)
\(\Rightarrow m_{Al}=0,2.27=5,4g\)
c.\(Mg+H_2SO_4\left(l\right)\rightarrow MgSO_4+H_2\)
0,1 0,1 ( mol )
\(2Al+3H_2SO_4\left(l\right)\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
0,2 0,3 ( mol )
\(V=\dfrac{n}{C_{M\left(H_2SO_4\right)}}=\dfrac{0,1+0,3}{2}=0,2l\)
Đúng 3
Bình luận (1)
Xem thêm câu trả lời
Cho 17,7 gam hỗn hợp 2 kim loại gồm kẽm và sắt tác dụng với hcl , thu được 6,72 lít khí h2(đktc).
a) viết pthh.
b) tính khối lượng mỗi kim loại có trong hỗn hợp.
c) tính khối lượng muối clorua thu được
Xem chi tiết
a)
Zn + 2HCl → ZnCl2 + H2
Fe + 2HCl → FeCl2 + H2
b) Gọi số mol Zn và Fe có trong 17,7 gam hỗn hợp là x và y mol. nH2 = \(\dfrac{6,72}{22,4}\)=0,3 mol
Theo tỉ lệ phản ứng ta có \(\left\{{}\begin{matrix}x+y=0,3\\65x+56y=17,7\end{matrix}\right.\)=> x = 0,1 và y = 0,2
=> mZn = 0,1.65 = 6,5 gam và mFe= 0,2.56 = 11,2 gam
c) nHCl = 2nH2 = 0,3.2 = 0,6 mol
Áp dụng ĐLBT khối lượng => m muối clorua = mKl + mHCl - mH2
<=> m muối = 17,7 + 0,6.36,5 - 0,3.2 = 28,05 gam
Đúng 2
Bình luận (0)
cho 1,66 gam hỗn hợp gồm 2 kim loại Fe và Al tác dụng với dd HCL dư, sau phản ứng thu được 11,2 lít khí (dktc)
a, viết PTHH
b,tính khối lượng của kim loại trong hỗn hợp ban đầu
a) Fe +2 HCl -> FeCl2 + H2
x____2x______x____x(mol)
2 Al + 6 HCl -> 2 AlCl3 + 3 H2
y____3y______y________1,5y(mol)
b) nH2= 0,05(mol)
Ta có hpt:
\(\left\{{}\begin{matrix}56x+27y=1,66\\x+1,5y=0,05\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,02\\y=0,02\end{matrix}\right.\)
=> mFe=0,02.56= 1,12(g)
mAl=0,02.27=0,54(g)
Đúng 2
Bình luận (0)