mấy bn cứu mình với ạ
một ngtu có 9 electron ở lớp vỏ . Tổng số hạt trog ngtu là 28 . Tính số p, n và vẽ sơ đồ
ngtu có 9 electon ở lớp vỏ . Tổng số hạt trog ngtu là 28 . Tính số p,e,n
mình hỏi mà bài mà k ai trả lwoif giúp mình hết
Có: số p = số e
Vậy p = 9
Có: n + p + e = 28
Mà p = e = 9
\(\rightarrow n=28-9.2=10\)
Có thể vẽ sơ đồ đơn giản gồm vòng tròn con là hạt nhân, mỗi vòng cung nhỏ là một lớp với số electron của lớp ghi ở chân. Thí dụ sơ đồ đơn giản của nguyên tử sillic trong bài tập 4.3 như sau:
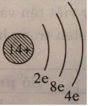
Biết rằng, trong nguyên tử các electron có ở lớp 1 (tính từ hạt nhân) tối đa là 2e, ở lớp 2 tối đa là 8e, ở lớp 3 tạm thời cũng là 8e, nếu còn electron sẽ ở lớp 4.
Mấy nguyên tử có số electron ở lớp ngoài cùng bằng 5, mấy nguyên tử có số electron ở lớp ngoài cùng bằng 7 ?
- Hai nguyên tử có số eletron lớp ngoài cùng là 5.
- Hai nguyên tử có số electron ngoài cùng 7.
Có thể vẽ sơ đồ đơn giản gồm vòng tròn con là hạt nhân, mỗi vòng cung nhỏ là một lớp với số electron của lớp ghi ở chân. Thí dụ sơ đồ đơn giản của nguyên tử sillic trong bài tập 4.3 như sau:
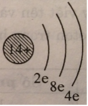
Biết rằng, trong nguyên tử các electron có ở lớp 1 (tính từ hạt nhân) tối đa là 2e, ở lớp 2 tối đa là 8e, ở lớp 3 tạm thời cũng là 8e, nếu còn electron sẽ ở lớp 4.
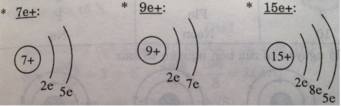
Vẽ sơ đồ đơn giản của năm nguyên tử mà trong hạt nhân có số proton bằng 7, 9, 15, 17, 19.
Nguyên tử có hạt nhân có số proton lần lượt à 7e+; 9e+; 15e+; 17e+; 19e+.

tổng số hạt p,n,e có trong một loại ngtu của ngto X là 54 trong đó tổng số hạt mang điện nhiều hơn số hạt ko mang điện là 1,7 lần. Xac định số hiệu ngtu số khối và viết kí hiệu ngtu X
2P+N=54
2P=1,7N
Giải hệ ta được: P=17(Cl), N=20
A=P+N=37
ta có : 2e +n =54
mặt khác : 2e =1.7*n
suy ra --> 1.7n +n =54
--> n =20
--> e = p = 20.1.7 =17
Vậy X là clo
Hợp chất MX2 đc cấu tạo từ ion M+và X-. Trong phân tử MX2, có tổng số hạt p,n,e là 116, tổng số hạt trong ngtu M nhiều hơn tổng số hạt trong ngtu X là 32. số khối của M lớn hơn số khối của X là 21. Xác định công thức của phân tử MX2
bài 15: ngtu R có tổng số hạt các loại =34, trong hạt nhân ngtu, số hạt mang điện =91,67% số hạt không mang điện. tìm Z. giúp tui với
Cho tổng số hạt p,n,e trong nguyên tử X là 36 .số hạt không mang điện chiếm 1/3 tổng số hạt .Tính số hạt p,n,etrong nguyên tử đó. Vẽ sơ đồ cấu tạo nguyên tử X?cho biết số lớp electron và hạt electron lớp ngoài cùng?
Số hạt không mang điện là:
\(\dfrac{1}{3}.36=12\left(hạt\right)\)
\(\Rightarrow p=e=\dfrac{36-12}{2}=12\left(hạt\right)\)
(Bn tự vẽ hình nhé.)
Một nguyên tử X có 2 lớp electron, biết lớp ngoài cùng có 4 electron. Trong nguyên tử X, số hạt mang điện hơn số hạt ko mang điện 6 hạt.
a)xác định số hạt proton, electron, nơtron, NTK (đvC) và kí hiệu hóa học của X
b) Vẽ sơ đồ phân bố lớp vỏ electron vủa nguyên tử X, tính khối lượng nuyên tử X theo đơn vị gam
c) Biết rằng 8 nguyên tử X nặng bằng 3 nguyên tử Y; 2 nguyên tử Y nặng bằng 4 nguyên tử Z. Xác định phân tử khối của các hợp chất XY2; XZ2 và YZ3
a)
X có 6 electron
=> pX = eX = 6
nX = 2pX - 6 = 6
X là Cacbon(C), có NTK = 12 (đvC)
b)

Khối lượng của 1 nguyên tử C = 1,9926.10-23 (g)
c)
\(NTK_Y=\dfrac{8.12}{3}=32\left(đvC\right)\)
PTKXY2 = 12 + 32.2 = 76 (đvC)
\(NTK_Z=\dfrac{2.32}{4}=16\left(đvC\right)\)
PTKXZ2 = 12 + 16.2 = 44 (đvC)
PTKYZ3 = 32 + 16.3 = 80 (đvC)
ta có lớp ngoài có 4 lớp => tổng số e là : 4+2=6 hạt
=> p=e=6
2p - n = 6
<=> 12 - n = 6
<=> n=6
=> X là Cacbon : C
c) ta lại có : 8X = 3Y => 48 = 3Y => Y = 16 => Y là S
có : 2Y = 4Z => 32 = 4Z = Z= 8 => Z là O
=> CTHH : XY2 : CS2 , XZ2 : CO2 , YZ3 : SO3
ta có lớp ngoài có 4 lớp => tổng số e là : 4+2=6 hạt
=> p=e=6
2p - n = 6
<=> 12 - n = 6
<=> n=6
=> X là Cacbon : C
c) ta lại có : 8X = 3Y => 48 = 3Y => Y = 16 => Y là S
có : 2Y = 4Z => 32 = 4Z = Z= 8 => Z là O đơn giản cũng hỏi
tổng số hạt proton, electron, notron trong 2 ngtu kim loại A,B là 94 trong đó tổng số hạt mang điện nhiều hơn tổng số hạt khong mang điện là 30. Số hạt mang điện của ngtu A nhiều hơn số hạt mang điện của ngtu B là 14. Xác định 2 kim loại A,B
giúp mik vs ![]()
Theo đề ta có: p + n+ e =94 (1)
p +n -e = 30 (2)
Cộng 1 và 2
2(p+n)= 124
=> p+n =62 (3)
lại có: p-n =14 (4)
Cộng 3 và 4:
2p=76
=> p=39
=> n= 28
vậy A là Kali
B là Silic
Mình cũng không chắc nữa
Gọi số hạt của kim loại A là p1 , n1 ,e1
số hạt của kim loại B là p2 , n2 , e2
Vì tổng số hạt của 2 nguyên tử A và B là 94
=> p1 + n1 + e1 + p2 + n2 + e2 = 94 (*)
mà số hạt mang điện nhiều hơn số hạt không mang điện là 30
=> (p1 + e1 + p2 + e2) - (n1 + n2) = 30 (**)
Cộng ( *) và (**) ta được :
2p1 + 2e1 + 2p2 + 2e2 = 124
=> 4p1 + 4p2 = 124 (vì số p = số e )
=> p1 + p2 = 31 (***)
mà số hạt mang điện của nguyên tử A nhiều hơn số hạt mang điện của nguyên tử B là 14
=> p1 + e1 - (p2 + e2) = 14
=> 2p1 - 2p2 = 14 (vì số p =số e )
=> p1 - p2 = 7 (****)
Từ (***) và (****) có :
\(\left\{{}\begin{matrix}p_1+p_2=31\\p_1-p_2=7\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}p_1=19\\p_2=12\end{matrix}\right.\)
Tra bảng thấy A là Kali (K) có số proton = 19
B là Magie (Mg) có số proton = 12
Để xác định số hạt proton trong hai kim loại A và B, ta cần giải hệ các phương trình dựa trên các điều kiện đã cho.
Gọi \( p_A, n_A, e_A \) lần lượt là số proton, neutron và electron của nguyên tử A. Tương tự, gọi \( p_B, n_B, e_B \) là số proton, neutron và electron của nguyên tử B.
### Bước 1: Thiết lập phương trình
1. Tổng số hạt proton, neutron và electron trong hai nguyên tử A và B là 94:
\[ p_A + n_A + e_A + p_B + n_B + e_B = 94 \]
2. Tổng số hạt mang điện nhiều hơn tổng số hạt không mang điện là 30:
\[ (p_A + e_A + p_B + e_B) - (n_A + n_B) = 30 \]
3. Số hạt mang điện của nguyên tử A nhiều hơn số hạt mang điện của nguyên tử B là 14:
\[ (p_A + e_A) - (p_B + e_B) = 14 \]
Bước 2: Đơn giản hóa phương trình
Vì nguyên tử trung hòa về điện tích, số proton bằng số electron:
\[ p_A = e_A \]
\[ p_B = e_B \]
Do đó, ta có:
\[ 2p_A + n_A + 2p_B + n_B = 94 \quad \text{(1)} \]
\[ 2p_A + 2p_B - (n_A + n_B) = 30 \quad \text{(2)} \]
\[ 2p_A - 2p_B = 14 \quad \text{(3)} \]
### Bước 3: Giải hệ phương trình
Từ phương trình (3):
\[ p_A - p_B = 7 \]
\[ p_A = p_B + 7 \quad \text{(4)} \]
Thay phương trình (4) vào phương trình (1) và (2):
Từ phương trình (1):
\[ 2(p_B + 7) + n_A + 2p_B + n_B = 94 \]
\[ 2p_B + 14 + n_A + 2p_B + n_B = 94 \]
\[ 4p_B + n_A + n_B = 80 \quad \text{(5)} \]
Từ phương trình (2):
\[ 2(p_B + 7) + 2p_B - (n_A + n_B) = 30 \]
\[ 2p_B + 14 + 2p_B - n_A - n_B = 30 \]
\[ 4p_B - n_A - n_B = 16 \quad \text{(6)} \]
Cộng phương trình (5) và (6):
\[ (4p_B + n_A + n_B) + (4p_B - n_A - n_B) = 80 + 16 \]
\[ 8p_B = 96 \]
\[ p_B = 12 \]
Từ phương trình (4):
\[ p_A = p_B + 7 \]
\[ p_A = 12 + 7 \]
\[ p_A = 19 \
Bước 4: Tính số neutron
Thay các giá trị \( p_A \) và \( p_B \) vào phương trình (5):
\[ 4p_B + n_A + n_B = 80 \]
\[ 4 \times 12 + n_A + n_B = 80 \]
\[ 48 + n_A + n_B = 80 \]
\[ n_A + n_B = 32 \]
Thay vào phương trình (6):
\[ 4p_B - n_A - n_B = 16 \]
\[ 4 \times 12 - n_A - n_B = 16 \]
\[ 48 - n_A - n_B = 16 \]
\[ 32 = n_A + n_B \]
Xác định nguyên tố:
- Nguyên tử A có \( p_A = 19 \): Đó là Kali (K).
- Nguyên tử B có \( p_B = 12 \): Đó là Magie (Mg).
Vậy số proton trong nguyên tử A là 19 và trong nguyên tử B là 12. Nguyên tố A là Kali (K) và nguyên tố B là Magie (Mg).