một hỗn hợp khí B gồm : CH4 ;H2;CÓ . trong hỗn hợp, khí H2 chiếm 60% về thể tích và 12% về khối lượng
a) xác định % thể tích và % khối lượng mối khí trong B
b) tính tỉ khối của khí B so với khí H2
Có một hỗn hợp khí gồm CO2 và CH4. Hãy trình bày phương pháp hóa học để:
a) Thu được khí CH4
b) Thu được khí CO2
Dẫn 3g hỗn hợp gồm CH4,C2H4 qua bình Br dư thấy 2,24l có một khí thoát khỏi bình a,PTHH b,Xác định % khối lượng mỗi khí trong hỗn hợp
\(PTHH:C_2H_4+Br_2\rightarrow C_2H_4Br_2\\ n_{CH_4}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\\ \%m_{CH_4}=\dfrac{0,1.16}{3}.100\%=53,33\%\\ \%m_{C_2H_4}=100\%-53,33\%=46,67\%\)
\(V_{khí.thoát.ra}=V_{CH_4}=2,24l\)
\(n_{CH_4}=\dfrac{2,24}{22,4}=0,1mol\)
\(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
\(m_{CH_4}=0,1.16=1,6g\)
\(\left\{{}\begin{matrix}\%m_{CH_4}=\dfrac{1,6}{3}.100=53,33\%\\\%m_{C_2H_4}=100\%-53,33\%=46,67\%\end{matrix}\right.\)
Hỗn hợp khí A gồm C2H2, CH4 và H2. Dẫn m gam hỗn hợp A vào bình kín chứa chất xúc tác Ni, rồi đun nóng. Sau một thời gian thu được hỗn hợp khí B gồm CH4, C2H4, C2H6, C2H2 và H2. Dẫn toàn bộ lượng khí B vào dung dịch brom ( dư) thấy khối lượng bình đựng brom tăng 4,1 gam và thoát ra hỗn hợp khí D. Đốt cháy hoàn toàn D cần dùng 9,52 lít khí O2 (đktc), thu được sản phẩm cháy gồm CO2 và 8,1 gam H2O.
Viết các phương trình phản ứng xảy ra và tính m.
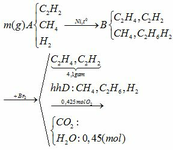
C2H2 + H2 C2H4
C2H2 + H2 C2H6
Khi cho hỗn hợp B qua dd nước Br2 chỉ có C2H4 và C2H2 phản ứng C2H2 +2Br2 → C2H2Br4
C2H4 + Br2 → C2H4Br2
=> khối lượng bình Br2 tăng chính bằng khối lượng của C2H2 và C2H4
mC2H2 + mC2H4 = 4,1 (g)
Hỗn hợp khí D đi ra là CH4, C2H6 và H2
CH4 + 2O2 → t ∘ CO2 + 2H2O
C2H6 + O2 → t ∘ 2CO2 + 3H2O
2H2 + O2 → t ∘ 2H2O
Bảo toàn nguyên tố O cho quá trình đốt cháy hh D ta có:
2nCO2 = 2nO2 – nH2O => nCO2 = ( 0,425. 2– 0,45)/2 = 0,2 (mol)
Bảo toàn khối lượng : mhh D = mCO2 + mH2O – mO2 = 0,2.44 + 0,45.18 – 0,425.32 = 3,3 (g)
Bảo toàn khối lương: mA = (mC2H2 + mC2H4) + mhh D = 4,1 + 3,3 = 7,4 (g)
Một hỗn hợp X gồm 8,8 gam CO2 và 19,2 gam SO2. Tính tỉ khối của X đối với:
a, Khí hydrogen.
b, Hỗn hợp khí Y gồm: 0,1 mol CH4 và 0,4 mol N2
Hỗn hợp B gồm 2 khí N2O và O2 có tỉ khối với CH4 là 2,5 . Tính V mỗi khí có trong 12g hỗn hợp B ở đktc?
Gọi số mol N2O, O2 trong 12g hỗn hợp B là a, b
=> 44a + 32b = 12 (1)
Có \(M=\dfrac{44a+32b}{a+b}=2,5.16=40\)
=> \(\dfrac{a}{b}=\dfrac{2}{1}\) (2)
(1)(2) => a = 0,2 ; b = 0,1
=> \(\left\{{}\begin{matrix}V_{N_2O}=0,2.22,4=4,48\left(l\right)\\V_{O_2}=0,1.22,4=2,24\left(l\right)\end{matrix}\right.\)
Một lít hỗn hợp gồm hai chất khí C3H8 và CH4 có thể tích bằng nhau. Xác định khối lượng của hỗn hợp??
Một hỗn hợp khí M gồm ankin X và H2 có tỉ khối hơi so với CH4 là 0,6. Nung nóng hỗn hợp M với bột Ni để phản ứng xảy ra hoàn toàn thu được hỗn hợp khí N có tỉ khối hơi so với CH4 là 1,0. Ankin X là
A. axetilen.
B. metylaxetilen.
C. etylaxetilen.
D. propylaxetilen.
Đáp án B
hhM gồm CnH2n - 2 và H2 có dM/CH4 = 0,6.
Nung M với Ni → hhN có N/CH4 = 1.
• Ta có hhN có M = 16 → H2 dư.
Đặt nCnH2n - 2 x mol và H2 y mol.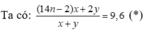
Vì phản ứng xảy ra hoàn toàn → hhN gồm CnH2n + 2 x mol và H2 dư (y - 2x) mol.![]()
Từ (*), (**) → y = 4x → n = 3 → CH≡C-CH3 → metylaxetilen
hỗn hợp khí x gồm NO,NxO và CH4 trong đó NO chiếm 30% về thể tích,NxOchiếm 30% còn lại là CH4 .trong hỗn hợp CH4 chiếm 22,377% về khối lượng
a, xác định công thức hóa học của NxO
b tính tỉ khối của X so với không khí
Không mất tính tổng quát quy ước
nNO=3;nNxO=3;nCH4=4
Ta có:
Đốt cháy hoàn toàn 8,96 L hỗn hợp khí (đo ở đktc) gồm CH4 và C2H4 cần phải dùng 28,8 g khí Oxi khối lượng mỗi khí có trong hỗn hợp là A.4,8 g CH4; 2,8 g C2H4. B.48 g CH4;28 g C2H4 C.4,8 g C2H4;2,8 g CH4. D.48 g C2H4;2,8 g CH4
Mn giúp vs
hỗn hợp B gồm 2 khí N2O và O2 có tỉ khối đối với khí metan CH4 là 2,5 . tính phần trăm thể tích của mỗi khí trong hỗn hợp B. ( đề hsg hóa)
`d_[B//CH_4]=[\overline{M_B}]/16=2,5`
`=>\overline{M_B}=40`
`=>[n_[N_2 O]]/[n_[O_2]]=|[40-32]/[40-44]|=2`
Vì phần trăm của thể tích mỗi khí trog hỗn hợp `B` bằng phần trăm của số mol mỗi khí trong hỗn hợp `B`
`=>%V_[N_2 O]=2/[2+1] .100~~66,67%`
`=>%V_[O_2]~~100-66,67~~33,33%`