Người ta xác định được rằng , trong 1 hợp chất vs nguyên tử Hiđro, nguyên tử Silic chiếm 87,5% về khối lượng. Viết CTHH , tính PTK của chất đó

Những câu hỏi liên quan
Bài 1:Người ta sác định được rằng , nguyên tố Si chiếm 87,5%về khối lượng trong đó hợp chất của nguyên tố Ha) viết CTHH và tính PTK của hợp chấtb)Xác định hóa trị của Si trong hợp chấtBài 2:Blà hợp chất của nguyên tố Y và H.Tỉ lệ số nguyên tử trong phân tử hợp chất B là Y:B1:3, trong đó nguyên tố Y chiếm 82,35% về khối lượng a)XĐ tên củaYb)tính PTK của B.Nếu phân tử chỉ có 1 nguyên tử Yc)CTHH của B
Đọc tiếp
Bài 1:Người ta sác định được rằng , nguyên tố Si chiếm 87,5%về khối lượng trong đó hợp chất của nguyên tố H
a) viết CTHH và tính PTK của hợp chất
b)Xác định hóa trị của Si trong hợp chất
Bài 2:Blà hợp chất của nguyên tố Y và H.Tỉ lệ số nguyên tử trong phân tử hợp chất B là Y:B=1:3, trong đó nguyên tố Y chiếm 82,35% về khối lượng
a)XĐ tên củaY
b)tính PTK của B.Nếu phân tử chỉ có 1 nguyên tử Y
c)CTHH của B
Người ta xác định được rằng nguyên tố silic(Si) chiếm 87,5% về khối lượng trong hợp chất với nguyên tố hidro. Viết công thức hóa học và tính phân tử khối của hợp chất.
Gọi công thức của hợp chất là S i x H y .
Theo đề bài ta có:
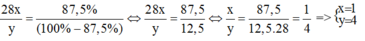
CTHH của hợp chất là S i H 4 .
Phân tử khối là: 28 + 4.1 = 32 ( đvC)
Đúng 0
Bình luận (0)
Câu 16: (M4) Người ta xác định được rằng nguyên tố silic (Si) chiếm 87,5% về khối lượng tronghợp chất với nguyên tố hidro.a) Viết công thức hóa học và tính phân tử khối của hợp chất.b) Xác định hóa trị của silic trong hợp chất.Câu 17: (M4) Phân tích mẫu hợp chất tạo bởi hai nguyên tố là sắt và oxi. Kết quả cho thấy cứ 7phần khối lượng sắt có tương ứng 3 phần khối lượng oxi.a) Viết công thức hóa học và tính phân tử khối của hợp chất.b) Xác định hóa trị của sắt trong hợp chất.Câu 18: (M4) Cho biết...
Đọc tiếp
Câu 16: (M4) Người ta xác định được rằng nguyên tố silic (Si) chiếm 87,5% về khối lượng trong
hợp chất với nguyên tố hidro.
a) Viết công thức hóa học và tính phân tử khối của hợp chất.
b) Xác định hóa trị của silic trong hợp chất.
Câu 17: (M4) Phân tích mẫu hợp chất tạo bởi hai nguyên tố là sắt và oxi. Kết quả cho thấy cứ 7
phần khối lượng sắt có tương ứng 3 phần khối lượng oxi.
a) Viết công thức hóa học và tính phân tử khối của hợp chất.
b) Xác định hóa trị của sắt trong hợp chất.
Câu 18: (M4) Cho biết X và Y tạo được các hợp chất như sau: X3(SO4)3 và H3Y.
Hãy viết công thức hóa học của hợp chất tạo bởi X và Y.
Câu 19: (M4) Một hợp chất của nguyên tố T hóa trị III với nguyên tố oxi, trong đó T chiếm 53%
về khối lượng.
a) Xác định nguyên tử khối và tên của T.
b) Viết công thức hóa học và tính phân tử khối của hợp chất.
Câu 20: (M4) Hợp chất A bởi hidro và nhóm nguyên tử ( XOy ) hóa trị III. Biết rằng phân tử A
nặng bằng phân tử khối của H2SO4 và nguyên tố oxi chiếm 61,31% về khối lượng của A.
a) Xác định chỉ số y và nguyên tử khối của nguyên tố X.
b) Viết tên, kí hiệu hóa học của X và công thức hóa học của A.
mọi người cứ làm dần đi ạ em ko gấp lắm em cảm ơn
Câu 16 :
a) CTHH : $SiH_n$
Ta có : $\%Si = \dfrac{28}{28 + n}.100\% = 87,5\% \Rightarrow n = 4$
Vậy CTHH là $SiH_4$
$PTK = 32(đvC)$
b) Si có hóa trị IV trong hợp chất
Câu 17 :
a) Gọi CTHH là $Fe_xO_y$
Ta có : $\dfrac{56x}{7} = \dfrac{16y}{3} \Rightarrow \dfrac{x}{y} = \dfrac{2}{3}$
Vậy oxit là $Fe_2O_3$
PTK = 160 đvC
b) Fe có hóa trị III trong hợp chất
Đúng 3
Bình luận (0)
Câu 18 :
$X_2(SO_4)_3 \Rightarrow $ X có hóa trị III
$H_3Y \Rightarrow $ Y có hóa trị III
Theo quy tắc hóa trị, CTHH cần tìm là XY
Câu 19 :
a) CTHH : $T_2O_3$
$\%T = \dfrac{2T}{2T + 16.3}.100\% = 53\%$
$\Rightarrow T = 27(Al)$
Vậy T là nhôm
b) CTHH là $Al_2O_3$
$PTK = 102(đvC)$
Câu 20 :
a) CTHH là $H_3XO_y$
Ta có : $M_A = 3 + X + 16y = 98(1)$
$\%O = \dfrac{16y}{98}.100\% = 61,31\%(2)$
Từ (1)(2) suy ra X = 31 ; y = 4
b)
X là Photphot, kí hiệu P
Đúng 3
Bình luận (0)
Người ta xác định được rằng , nguyên tố silic (Si) chiếm 87,5% về khối lượng trọng hợp chất với nguyến tố hiđro.
a) Viết CTHH và phân tử khối của hợp chất.
b) Xác định hóa trị của silic trong hợp chất
a, Gọi công thức của hợp chất Si và H là SixHy(x,y nguyên dương)
%H=100%-87,5%=12,5%
Ta có tỉ lệ:x:y=%Si/M(Si) : %H/M(H)
=87,5/28:12,5/1
=3,125:12.5
=1:4
=>CT:SiH4
PTK(SiH4)=28+4=32
b,Gọi hóa trị của Si là a(a nguyên dương)
Aps dụng quy tắc hóa trị: a*1=I*4
=>a=IV
=>hóa trị cuiar Silic trong hợp chất là 4
Đúng 0
Bình luận (2)
Ta có
a, Gọi CTHC là SixHy ( x ; y > 0 )
=> \(\dfrac{28x}{y}=\dfrac{87,5}{100-87,5}\)
=> \(\dfrac{x}{y}=\dfrac{87,5}{12,5\times28}\)
=> \(\dfrac{x}{y}=\dfrac{87,5}{350}=\dfrac{1}{4}\)
=> CTHC là SiH4
MSiH4 = 28 + 1 . 4 = 32 ( đvC )
b, Si có hóa trị IV
Đúng 1
Bình luận (2)
Người ta xác định được rằng nguyên tố silic(Si) chiếm 87,5% về khối lượng trong hợp chất với nguyên tố hidro. Xác định hóa trị của Silic trong hợp chất.
Hóa trị của Si trong hợp chất S i H 4 là IV.
Đúng 0
Bình luận (0)
Thành phần chính của cát, thuỷ tinh là hợp chất giữa Si và O. Trong hợp chất này, người ta xác định được rằng nguyên tố silic (Si) chiếm 46,67% về khối lượng. Viết công thức hoá học và tính khối lượng mol phân tử của hợp chất.
Gọi CTHH là $Si_xO_y$
$\%O = 100\% -46,67\% = 53,33\%$
Ta có :
\(\dfrac{28x}{46,67}=\dfrac{16y}{53,33}\Rightarrow\dfrac{x}{y}=0,5=\dfrac{1}{2}\)
Vậy CTHH cần tìm là $SiO_2$
$M_{SiO_2} = 60(đvC)$
Đúng 1
Bình luận (0)
%O=100-46,67=53,33%
=>Si:O=46,67.28\100:53,33.16\100=1:2
=>SiO2
M SiO2=28+16.2=60đvC
Đúng 0
Bình luận (0)
Một hợp chất gồm 2 nguyên tử X và 3 nguyên tử Oxi trong đó X chiếm 52,94% về khối lượng
a) Tính PTK của hợp chất
b) viết CTHH đúng của hợp chất
Do hợp chất gồm 2 nguyên tử X và 3 nguyên tử Oxi , mà trong đó X chiếm 52,94%
=> Khối lượng của Oxi chiếm :
100% - 52,94% = 47,06% (khối lượng hợp chất)
Mà khối lượng Oxi trong hợp chất là : 3*16 = 48 (đvC)
=> Khối lượng bằng đvC của hợp chất là :
48 : 47,06% = 102 (đvC)
=> Khối lượng bằng đvC của 2 nguyên tử X trong hợp chất là :
102 - 48 = 54 (đvC)
=> Khối lượng bằng đvC của 1 nguyên tử X là :
54 : 2 = 27 (đvC)
=> X là nguyên tố nhôm (Al)
Công thức hóa học đúng của hợp chất là Al2O3
Đúng 0
Bình luận (2)
Một hợp chất gồm 2 nguyên tử nguyên tố A liên kết với 1 nguyên tử nguyên tố B, và có phân tử khối nặng hơn phân tử khí Hiđro 31 lần.
a. Viết CTHH chung của hợp chất
b. Xác định A, B tìm CTHH của hợp chất biết PTK của A nhiều hơn PTK của B= 7 đvC
giúp mình với ạ:((
Ai giúp vs
Phân tử hợp chất gồm 2 nguyên tố R liên kết vs 1 nguyên tử oxi và nặng gấp 4 lần phân tử hidro
a)Tính PTK của hợp chất
b)Tìm tên và kí hiệu của nguyên tố R
c) Viết CTHH của hợp chất đó và tính % về khối lượng của nguyên tố R trong hợp chất
\(a.M_{hc}=47.M_{H_2}=94\left(đvC\right)\\ b.CTHHcủahợpchất:R_2O\\ Tacó:2.R+16=94\\ \Rightarrow R=39\left(Kali-K\right)\\ c.CTHH:K_2O\\ \%K=\dfrac{39.2}{94}.100=82,98\%\)
Đúng 2
Bình luận (0)
Xem lại đề chỗ "nặng gấp 4 lần phân tử hidro" nha em!
Đúng 0
Bình luận (1)


















