Phân tích mẫu hợp chất tạo bởi 2 nguyên tố là sắt và oxi. Kết quả cho thấy cứ 7 phần khối lượng sắt có tương ứng với 3 phần khối lượng oxi.
a) Viết công thức hóa học và tính phân tử khối của hợp chất.
b) Xác định hóa trị của sắt trong hợp chất.
Phân tích một mẫu hợp chất tạo bởi hai nguyên tố là sắt và oxi. Kết quả cho thấy cứ 7 phần khối lượng sắt có tương ứng với 3 phần khối lượng oxi. Viết công thức hóa học và tính phân tử khối của hợp chất.
Công thức chung của hợp chất F e x O y .
Theo đề bài ta có:
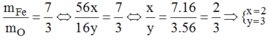
Vậy CTHH của hợp chất là F e 2 O 3 .
Phân tử khối là: 56.2 + 16.3 = 160 (đvC)
Phân tích một mẫu hợp chất tạo bởi hai nguyên tố là sắt và oxi. Kết quả cho thấy cứ 7 phần khối lượng sắt có tương ứng với 3 phần khối lượng oxi. Xác định hóa trị của sắt trong hợp chất.
Hợp chất Fe2O3. Gọi hóa trị của Fe là x
Theo quy tắc hóa trị ta có: x. 2 = 3.II ⇒ x = III
: Phân tích một mẫu hợp chất tạo bởi 2 nguyên tố là Fe và O. Kết quả cho thấy cứ 7 phần khối lượng Fe có tương ứng với 3 phần khối lượng oxi.
a. Viết công thức hóa trị của Fe trong hợp chất
b. Xác định hóa trị của Fe trong hợp chất
Vậy x=2, y=3
Công thức hóa học của hợp chất là 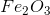
Phân tử khối bằng
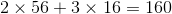
b) Hóa trị của Fe trong hợp chất là : III
Bài 3: Phân tích một mẫu hợp chất tạo bởi hai nguyên tố Fe và O. Kết quả cho thấy cứ 7 phần khối lượng Fe có tương ứng với 3 phần khối lượng O
a. Viết CTHH và tính PTK của hợp chất
b. Xác định hóa trị của Fe trong hợp chất.
CTHH : Fe2O3
hóa trị :
a . x = y.b
=> a .2 = 2.3
=> a = lll
Một hợp chất tạo bởi hai nguyên tố là nitơ và oxi. Kết quả cho thấy cứ 7 phần khối lượng nitơ có tương ứng 16 phần khối lượng oxi. CTHH của hợp chất là: A.NO2 B.NO C.N2O D.N2O3
Phân tích một mẩu hợp chất tạo bởi 2 nguyên tố S và O kết quả cho thấy cứ 2 phần khối lượng S ứng với 3 phần khối lượng O.
A) Viết công thức hoá học đơn giản, tính phân tử khối của hợp chất.
B) Xác định hoá trị của S trong hợp chất.
Ghi rõ cách làm luôn nha các bạn.
Phân tích mẫu hợp chất tạo bởi 2 nguyên tố sắt và oxi.Kết quả cho thấy thành phần phần trăn theo khối lượng của Fe trong hợp chất là 72,414%
a ) Viết CTHH và tính PTK của hợp chất
b ) Xác định hóa trị của sắt trong hợp chất .
a ) Đặt công thức hóa học của hợp chất có dạng chung là FexOy.Ta có :
\(\%m_{Fe}=\frac{56x}{56x+16y}\times100\%=72,414\%\Rightarrow\frac{x}{y}=\frac{3}{4}\Rightarrow x=3\) và \(y=4\)
\(\Rightarrow\) CTHH của hợp chất là : \(Fe_3O_4.\)
\(\Rightarrow\) PTK của \(Fe_3O_4\)là \(56\times3+4\times16=232\) đvC
b ) \(Fe_3O_4=FE^{II}O^{II}.Fe_2^{III}O_3^{II}\)
\(\Rightarrow\) Trong phân tử Fe3O4 thì Fe có hóa trị II và III .
Câu 1: Phân tích mẫu hợp chất tạo bởi hai nguyên tố là sắt và oxi. Kết quả cho thấy cứ 7 phần
khối lượng sắt có tương ứng 3 phần khối lượng oxi.
a) Viết công thức hóa học và tính phân tử khối của hợp chất.
b) Xác định hóa trị của sắt trong hợp chất.
Câu 2: Cho biết X và Y tạo được các hợp chất như sau: X2(SO4)3 và H3Y.
Hãy viết công thức hóa học của hợp chất tạo bởi X và Y.
Câu 2:
Áp dụng quy tắc hoá trị: X có hoá trị III (1)
Áp dụng quy tắc hoá trị: Y có hoá trị III (2)
Từ (1)(2), X và Y đều có hoá trị III nên CTHH là: XY
Câu 1: Ta có CTHC là FexOy
mà 56x . 7 = 16y . 3
=> \(\dfrac{56x}{16y}\) = \(\dfrac{3}{7}\)
=> \(\dfrac{x}{y}\) = \(\dfrac{6}{49}\)
=> x = \(\dfrac{6}{49}\)y
mà y là hóa trị của kim loại => 1 \(\le\) y \(\le\) 3
nếu y =1 => x = \(\dfrac{6}{49}\) ( loại )
nếu y = 2 => x = \(\dfrac{12}{49}\) ( loại )
nếu y = 3 => x = \(\dfrac{18}{49}\) ( loại )
Hình như đề sai rồi bạn ơi
Mình xin đổi lại đề của câu 1 là 3 phần khối lượng của Fe tương ứng với 7 phần khối lượng oxi
Hoặc khối lượng của oxi bằng \(\dfrac{3}{7}\)% Fe ( Nếu làm theo cách sửa đề này bạn phải chứng minh %mO2 = 30% và %mFe = 70% trong hỗn hợp )
Câu 1: Ta có CTHC là FexOy
mà 56x . 3 = 16y . 7
=> \(\dfrac{56x}{16y}\) = \(\dfrac{7}{3}\)
=> \(\dfrac{x}{y}\) = \(\dfrac{2}{3}\)
=> x = \(\dfrac{6}{49}\)y
=> CTHC là Fe2O3
Phân tích mẫu hợp chất tạo bởi hai nguyên tố là sắt và oxi . Kết quả cho thấy cứ 7 phần khối lượng sắt có 3 phần khối lượng oxi.
a) Viết CTHH và tính PTK của hợp chất
b) Xác định hóa trị Sắt trg hợp chất
Ta có gọi CTHC là FexOy
=> \(\dfrac{56x}{16y}=\dfrac{7}{3}\)
=> \(\dfrac{x}{y}=\dfrac{7\times16}{3\times56}\)
=> \(\dfrac{x}{y}=\dfrac{2}{3}\)
=> CTHC là Fe2O3