1 n tố X có 2 đồng vị với tỉ lệ số n tử là 27/23. Hạt nhân n tử X có 35p, trong n tử của đồng vị 1 có 44 nơ tron, số nơ tron trong n tử của đồng đồng vị 27 đồng vị 1 là 2n
Xác định NTK trung bình của X?
Nguyên tố X có 2 đồng vị với tỉ lệ số nguyên tử là 27/23 . Hạt nhân nguyên tử X có 35p . đồng vị thứ nhất có 44 nơtron . Tính nguyên tử khối trung bình của:
Nguyên tử khối của động vị thứ nhất là :
\(35+44=49.\)
Nguyên tử khối của dồng vị thứ 2 là :
\(79+2=81\)
Nguyên tử khối trung bình của x là :
\(\frac{\left(79.27+81.23\right)}{27+23}=79,92\)
Vậy ..................................
Nguyên tố R có ba đồng vị . Nếu cứ mỗi đồng vị lấy 1 nguyên tử thì
-Tổng số hạt trong 3 nguyên tử đó là 111
-Nguyên tử đồng vị I có sô proton bằng số nơ tron
-Số nơ tron của đồng vị II nhiều hơn số nơ tron của đồng vị III là 1 hạt
Viết kí hiệu nguyên tử các đồng vị đó
Nguyên tố X có 2 đồng vị, tỉ lệ số nguyên tử đồng vị 1: đồng vị 2 là 27:23. Hạt nhân đồng vị 1 chứa 35 hạt proton, 44 hạt nơtron. Đồng vị thứ 2 hơn đồng vị 1 là 2 notron.
a) Tính nguyên tử khối trung bình của X.
b) X có thể tạo hợp chất CaX2. Nguyên tử khối của Ca = 40, tính % khối lượng của đồng vị 1 có trong CaX2
nguyên tố X có 2 đồng vị tỉ lệ với nhau là 27:23. hạt nhân của 1 đồng vị chứa 44 nơtron, hạt nhân của đồng vị 2 nhiều hơn 2 nơtron, biết nguyên tử khối trung bình là 79,92. tìm số khối của mỗi đồng vị
Bài 20: Nguyên tố A có 2 đồng vị X và Y có số nguyên tử tỉ lệ với nhau là 27 7/23 . Hạt nhân đồng vị X chứa 35 proton và 44 nơtron. Hạt nhân đồng vị Y chứa nhiều hơn X 2 nơtron. Xác định nguyên tử khối trung bình và tên nguyên tố A
Nguyên tố X có 2 đồng vị có tỉ lệ số nguyên tử 27 : 23 (27 là số khối, 23 là số e, p, số đvđthn). Hạt nhân X có 35p. Đồng vị có 44 nơtron. Đồng vị 2 nhiều hơn đômgf vị 1 là 2 nơtron
=> Nguyên tử khối của X
Một nguyên tố X có 2 đồng vị có tỉ lệ số nguyên tử là 27/23. Hạt nhân của X có 35 proton. Đồng vị thứ nhất có 44 nơtron. Đồng vị thứ hai có nhiều hơn đồng vị thứ nhất là 2 nơtron. Nguyên tử khối trung bình của nguyên tố X là
A. 78,90.
B. 79,20.
C. 79,92.
D. 80,5.
Chọn C
Số khối của đồng vị thứ nhất là: 79
Số khối của đồng vị thứ hai là: 79 + 2 = 81.
Một cách gần đúng, coi số khối xấp xỉ nguyên tử khối.
Nguyên tử khối trung bình của X là:
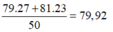
3. Nguyên tố brom có 2 đồng vị X, Y với tỉ lệ số nguyên tử X/Y = 27/23. Hạt nhân nguyên tử brom có 35 proton. Trong nguyên tử của đồng vị X có 44 nơtron. Số nơtron trong nguyên tử của đồng vị Y nhiều hơn trong đồng vị X là 2. Tính nguyên tử khối trung bình của nguyên tố brom.
Có 3 đồng vị của nguyên tố X, mà tổng số hạt trong 3 nguyên tử đồng vị là 75. Trong đồng vị 1, số p = số n, đồng vị 2 có số n kém thua đồng vị 3 là 1.
a. Xác định số khối của mỗi đồng vị
b. Trong X, số nguyên tử của các đồng vị thứ nhất, 2, 3 lần lướt theo tỉ lệ 115:3:2. Tìm khối lượng mol trung bình của X
do là đồng vị nên các nguyên tử có cùng số proton =>
p + n1 + p + n2 + p + n3 = 75 <=> 3p + n1 + n2 + n3 =75 (1)
mà nguyên tử đồng vị 1 có p = n => (1) <=> 4p + n2 + n3 = 75 (2)
ta lại có n3 - n2 = 1 => (2) <=> 4p + 2 n2 = 74 <=> 2p + n2 = 37 dùng bất pt bạn được p =< 12,33 và p >= 10.5 vậy chỉ thỏa khi p = 12 => n2 = 13 Vậy số khối 3 đồng vị lần lượt là 24 25 26
A trung bình của X là = 24 . 115 + 25. 3 + 26. 2 / ( 115 + 3 +2 ) = 24,0583