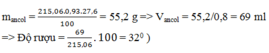Hoà tan 25g chất X vào 100 gam nước , dung dịch có khối lương riêng là 1,143 g/ml . Nồng độ % và thể tích dung dịch là bao nhiêu ?

Những câu hỏi liên quan
Hoà tan 25g một chất vào 100g nước. thu được dung dịch có khối lượng riêng là 1,143 g/ml . Tính nồng độ phần tram và thể tích dung dịch.
Hoà tan 28,7g ZnSO4.7H2O vào 171,3 ml nước. Tính nồng độ mol của dung dịch thu được( Coi thể tích dung dịch thu được bằng tổng thể tích nước và nước có khối lượng riêng là 1g/mol)
\(m_{H_2O}=\dfrac{171,3}{1}=171,3\left(g\right)\\ m_{dd.thu.được}=m_{tinh.thể}+m_{H_2O}=28,7+171,3=200\left(g\right)\\ n_{ZnSO_4}=n_{tinh.thể}=\dfrac{28,7}{161+7.18}=0,1\left(mol\right)\\ V_{H_2O\left(dd.thu.được\right)}=\dfrac{200-0,1.161}{1000}=0,1839\left(l\right)\\ C_{MddZnSO_4}=\dfrac{0,1}{0,1839}\approx0,5438\left(M\right)\)
Đúng 1
Bình luận (1)
Hòa tan hoàn toàn 24 gam SO3 vào nước, thu được dung dịch X có nồng độ 20% (loãng, khối lượng riêng là 1,14 g/ml).
a) Tính thể tích dung dịch X thu được.
b) Hòa tan m gam Fe vào dung dịch X ở trên, phản ứng xảy ra vừa đủ, sau phản ứng thu được dung dịch T và V lít khí (ở 25 độ C và 1 bar).
- Tính các giá trị của m và V.
- Tính nồng độ phần trăm của dung dịch T.
a) PTHH: \(SO_3+H_2O\rightarrow H_2SO_4\)
Ta có: \(n_{SO_3}=\dfrac{24}{80}=0,3\left(mol\right)=n_{H_2SO_4}\) \(\Rightarrow m_{ddH_2SO_4}=\dfrac{0,3\cdot98}{20\%}=147\left(g\right)\)
\(\Rightarrow V_{ddH_2SO_4}=\dfrac{147}{1,14}\approx128,95\left(ml\right)\)
b) PTHH: \(Fe+H_2SO_4\rightarrow FeSO_4+H_2\uparrow\)
Theo PTHH: \(n_{Fe}=n_{H_2SO_4}=n_{H_2}=0,3\left(mol\right)=n_{FeSO_4}\)
\(\Rightarrow\left\{{}\begin{matrix}m_{Fe}=0,3\cdot56=16,8\left(g\right)\\V_{H_2}=0,3\cdot24,76=7,428\left(l\right)\\m_{FeSO_4}=0,3\cdot152=45,6\left(g\right)\\m_{H_2}=0,3\cdot2=0,6\left(g\right)\end{matrix}\right.\)
Mặt khác: \(m_{dd}=m_{Fe}+m_{ddH_2SO_4}-m_{H_2}=163,2\left(g\right)\)
\(\Rightarrow C\%_{FeSO_4}=\dfrac{45,6}{163,2}\cdot100\%\approx27,94\%\)
Đúng 1
Bình luận (0)
Đem hòa tan rượu etylic vào nước được 215,06 ml dung dịch rượu có nồng độ 27,6%, khối lượng riêng của dung dịch rượu là 0,93 g/ml, khối lượng riêng của rượu etylic nguyên chất là 0,8 g/ml. Dung dịch trên có độ rượu là: A. 27,60 B. 220 C. 320 D. Đáp án khác.
Đọc tiếp
Đem hòa tan rượu etylic vào nước được 215,06 ml dung dịch rượu có nồng độ 27,6%, khối lượng riêng của dung dịch rượu là 0,93 g/ml, khối lượng riêng của rượu etylic nguyên chất là 0,8 g/ml. Dung dịch trên có độ rượu là:
A. 27,60
B. 220
C. 320
D. Đáp án khác.
Hoà tan 0,5 mol CuSO4.5H2O vào 245g nước. Tính nồng độ %, nồng độ mol và suy ra khối lượng riêng của dung dịch (giả sử hoà tan không làm thay đổi thẻ tích dung dịch, Dnc = 1g/ml)
Bài 7: hoà tan 21,6 g NaOH vào 400 gam nước được dung dịch Aa. tính khối lượng dung dịch Ab.tính thể tích tích dung dịch A c) tính nồng độ mol/lit nồng độ phần trăm của cac chất trong dung dịch AMN giải chi tiết và đơn giản giúp mình vs
Đọc tiếp
Bài 7: hoà tan 21,6 g NaOH vào 400 gam nước được dung dịch A
a. tính khối lượng dung dịch A
b.tính thể tích tích dung dịch A
c) tính nồng độ mol/lit nồng độ phần trăm của cac chất trong dung dịch A
MN giải chi tiết và đơn giản giúp mình vs
\(a.m_{dd}=21,6+400=421,6\left(g\right)\\ b.V_{dd}=400\left(mL\right)\\ c.C_M=\dfrac{\dfrac{21,6}{40}}{0,4}=1,35\left(mol\cdot L^{-1}\right)\)
Đúng 1
Bình luận (0)
\(a.m_A=m_{NaOH\left(loãng\right)}=21,6+400=421,6\left(g\right)\)
b,c. thiếu D nhé
Đúng 1
Bình luận (2)
Hòa tan m gam tinh thể CuSO4.5H2O vào V ml dung dịch CuSO4 có nồng độ c% (khối lượng riêng bằng d g/ml) thu được dung dịch X. Tính nồng độ % của dung dịch X theo m, V, c và d.
Khối lượng CuSO4 có trong m gam tinh thể : \(\frac{160}{250}\)m = 0,64(g)
Khối lượng CuSO4 trong V ml dung dịch CuSO4 c% ((khối lượng riêng bằng d g/ml) là : \(\frac{V.d.c}{100}\) = 0,01 V.d.c (g)
Khối lượng dung dịch X bằngv : m+V.d (g)
Nồng độ phần trăm của dung dịch X:
\(\frac{0,64m+0,01V.d.c}{m+V.d}.100\%=\frac{64m+V.d.c}{m+V.d}\left(\%\right)\)
Đúng 0
Bình luận (0)
Hòa tan 30 g NaCl vào 170 gam nước, được dung dịch có khối lượng riêng 1,1 gam/ml. Tính nồng độ phần trăm và nồng độ mol của dung dịch thu được
\(C\%=\dfrac{30}{170}.100\%=17,647\%\)
\(V_{\text{dd}}=\left(30+170\right)1,1=220ml\)
\(n_{NaCl}=\dfrac{30}{58,5}=0,513mol\)
\(C_M=\dfrac{0,513}{0,22}=0,696M\)
\(C\%_{NaCl}=\dfrac{30}{170+30}.100\%=15\%\\ C_M=C\%.\dfrac{10D}{M}=10.\dfrac{10.1,1}{58,5}=1,88M\)
Đúng 1
Bình luận (1)
Câu 8: Cho 99,4 gam P2O5 vào 500 gam nước (dư), thu được dung dịch A.
a. Tính khối lượng chất tan, khối lượng nước trong dung dịch A.
b. Tính nồng độ phần trăm dung dịch A.
c. Tính nồng độ mol/l của dung dịch A. Biết thể tích dung dịch A là 500 ml.
giúp vs ae
\(n_{P_2O_5}=\dfrac{99,4}{142}=0,7\left(mol\right)\)
\(P_2O_5+3H_2O\rightarrow2H_3PO_4\)
0,7 2,1 1,4
a, \(m_{H_3PO_4}=1,4.98=137,2\left(g\right)\)
\(m_{ddH_3PO_4}=99,4+500=599,4\left(g\right)\)
Kl nước trong dd A :
\(m_{H_2O}=599,4-137,2=462,2\left(g\right)\)
\(b,C\%_{H_3PO_4}=\dfrac{137,2}{599,4}.100\%\approx22,89\%\)
\(c,C_M=\dfrac{n}{V}=\dfrac{1,4}{0,5}=2,8M\)
Đúng 2
Bình luận (0)