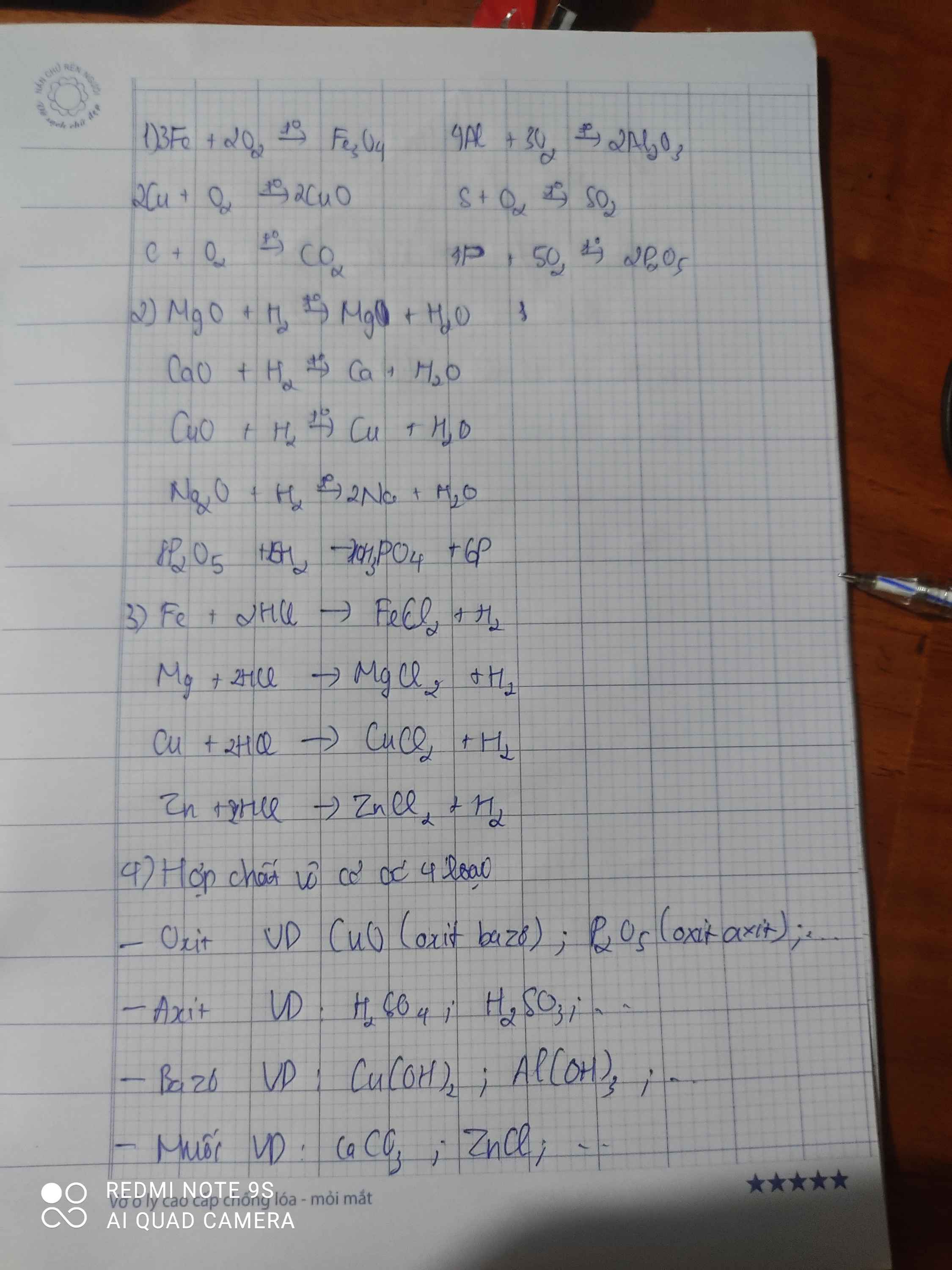Cho khí \(H_2\) qua các ống mắc nối tiếp :
MgO - CaO - CuO - \(Al_2O_3\) - \(Na_2O\).
Sau đó lấy sản phẩm thu được tác dụng với \(H_2O\), dd \(H_2SO_4\)loãng, dd KOH, khí CO, khí \(O_2\). Viết PTHH

Những câu hỏi liên quan
cho 200ml dd KOH 1M tác dụng với 200ml dd \(H_2SO_4\)1M, sau pứ cho thêm 1mảng Mg dư vào sản phẩm thấy thoát ra 1 thể tích khí \(H_2\)(đktc) là bao nhiêu?
PTHH: \(2KOH+H_2SO_4\rightarrow K_2SO_4+2H_2O\)
\(Mg+H_2SO_4\rightarrow MgSO_4+H_2\uparrow\)
Ta có: \(\left\{{}\begin{matrix}n_{KOH}=0,2\cdot1=0,2\left(mol\right)\\n_{H_2SO_4}=0,2\cdot1=0,2\left(mol\right)\end{matrix}\right.\)
Xét tỉ lệ: \(\dfrac{0,2}{2}< \dfrac{0,2}{1}\) \(\Rightarrow\) Axit còn dư 0,1 mol
\(\Rightarrow n_{H_2}=0,1\left(mol\right)\) \(\Rightarrow V_{H_2}=0,1\cdot22,4=2,24\left(l\right)\)
Đúng 0
Bình luận (0)
Cho 1 luồng khí H2 dư đi lần lượt đi qua các ống mắc nối tiếp,nung nóng đựng các chất sau tới phản ứng xảy ra hoàn toàn:CaO,CuO,Al2O3,MgO,Fe2O3.Sau đó lấy các chất còn lại trong ống ch tác dụng lần lượt với CO2,dung dịch HCl,dung dịch AgNO3.Viết PTHH xảy ra.
Xem chi tiết
Viết các PTHH và ghi đầy đủ điều kiện (nếu có) ? 1/Cho khí Oxi tác dụng lần lượt với : Fe , Al , Cu , S , C , P. 2/Cho khí hiđro đi qua các ống mắc nối tiếp , nung nóng , chứa lần lượt các chất : MgO, CaO, CuO, Na2O, P2O5. 3/Cho dung dịch axit HCl tác dụng lần lượt với các chất : Al, Fe, Mg, Cu, Zn. 4/Có mấy loại hợp chất vô cơ? Mỗi loại lấy 2 VD về CTHH? Đọc tên chúng
hh khí X gồm khí O2 và khí Y sau khi thực hiện phản ứng nổ làm lạnh sản phẩm thi được khí A và chất lỏng B. Cho khí A tác dụng với Fe thu được chất rắn C.Cho B tác dụng với SO3 thu được dd D.Cho C tác dụng với dd D loãng dư thu được khí Y. Cho khí Y tác dụng với CuO thu được chất rắn G. Viết PTHH xảy ra và cho biết các chất có trong A,B,C,D,G,Y. Biết khí Y được dùng bơm vào kinh khí cầu
Đọc tiếp
hh khí X gồm khí O2 và khí Y sau khi thực hiện phản ứng nổ làm lạnh sản phẩm thi được khí A và chất lỏng B. Cho khí A tác dụng với Fe thu được chất rắn C.Cho B tác dụng với SO3 thu được dd D.Cho C tác dụng với dd D loãng dư thu được khí Y. Cho khí Y tác dụng với CuO thu được chất rắn G. Viết PTHH xảy ra và cho biết các chất có trong A,B,C,D,G,Y. Biết khí Y được dùng bơm vào kinh khí cầu
cho 10h hỗn hợpCcu và CuO tác dụng với dd h2so4 (loãng) lấy chất rắn không tan cho vào dd h2so4 (đặc ) nóng thì thu được 1,12 lít khí A a) a)viết pthh các pư xảy ra và cho biết tên khí A
b)tính % kl các chất có trong hỗn hợp
CuO + H2SO4 --> CuSO4 + H2O
Cu + 2H2SO4(đđ) --> CuSO4 + SO2 + 2H2O
b) Theo ptrinh` 2, ta có:
nCu = nSO2 = V/22,4 = 1,12/22,4 = 0,05 mol
=> mCu = n . M = 0,05 . 64 = 3,2 g
theo đề, ta có:
mCu + mCuO = mhỗnhợp
=> mCuO = 10 - 3,2 = 6,8 g
Đúng 0
Bình luận (3)
cho 10g hh Cu và CuO tác dụng vừa đủ với đd H2SO4 loãng lọc lấy chất rắn không tan ,cho vào dd H2SO4 đặc nóng thì thu được 1,12 lít khí A (đktc)
a, viết PTHH và cho biết tên của khí A
b, tính thành phần % khối lượng các chất có trong hh
Cho 26 gam kẽm (Zn) tác dụng vừa đủ với dung dịch axit sunfuric (H_2SO_4) loãng. Sau phản ứng thu được kẽm sunfat (ZnSO_4) và khí hiđro (H_2)a) Viết PTHH và tính khối lượng của axit sunfuric (H_2SO_4) cần dùng.b) Tính khối lượng của kẽm sunfat ( ZnSO_4) tạo thành.c) Tính khối lượng khí H_2 và thể tích khí H_2 sinh ra ở đktc.
Đọc tiếp
Cho 26 gam kẽm (Zn) tác dụng vừa đủ với dung dịch axit sunfuric (\(H_2SO_4\)) loãng. Sau phản ứng thu được kẽm sunfat (\(ZnSO_4\)) và khí hiđro (\(H_2\))
a) Viết PTHH và tính khối lượng của axit sunfuric (\(H_2SO_4\)) cần dùng.
b) Tính khối lượng của kẽm sunfat ( \(ZnSO_4\)) tạo thành.
c) Tính khối lượng khí \(H_2\) và thể tích khí \(H_2\) sinh ra ở đktc.
a) Zn + H2SO4 --> ZnSO4 + H2
\(n_{Zn}=\dfrac{26}{65}=0,4\left(mol\right)\)
PTHH: Zn + H2SO4 --> ZnSO4 + H2
0,4-->0,4------->0,4---->0,4
=> \(m_{H_2SO_4}=0,4.98=39,2\left(g\right)\)
b) \(m_{ZnSO_4}=0,4.161=64,4\left(g\right)\)
c) \(\left\{{}\begin{matrix}m_{H_2}=0,4.2=0,8\left(g\right)\\V_{H_2}=0,4.22,4=8,96\left(l\right)\end{matrix}\right.\)
Đúng 3
Bình luận (0)
\(n_{Zn}=\dfrac{26}{65}=0,4\left(mol\right)\\
pthh:Zn+H_2SO_4\rightarrow ZnSO_4+H_2\)
0,4 0,4 0,4
\(m_{H_2SO_4}=0,8.98=78,4\left(g\right)\\
m_{ZnSO_4}=136.0,4=54,4\left(g\right)\\
m_{H_2}=0,4.2=0,6\left(g\right)\\
V_{H_2}=0,4.22,4=8,96\left(l\right)\)
Đúng 3
Bình luận (0)
Bài 1: Lập PTHH và cho biết số nguyên tử, số phân tử giữa các chất trong mỗi PƯ sau:
\(P+O_2->P_2O_5\\ Fe\left(OH\right)_3->Fe_2O_3+H_2O\)
\(Al_2O_3+HCl->AlCl_3+H_2O\\ K+H_2O->KOH+H_2\\ Na+O_2--->Na_2O\\ KClO_3--->KCl+O_2\)
4P+5O2−>2P2O5
2Fe(OH)3−>Fe2O3+3H2O
Al2O3+6HCl−>2AlCl3+3H2O
2K+2H2O−>2KOH+H2
4Na+O2−−−>2Na2O
2KClO3−−−>2KCl+3O2
Đúng 0
Bình luận (0)
a, 4P+5O2--->2P2O5
Tỉ lệ: 4:5:2
b, 2Fe(OH)3--->Fe2O3+3H2O
Tỉ lệ: 2:1:3
c, Al2O3+6HCl--->2AlCl3+3H2O
Tỉ lệ: 1:6:2:3
d, 2K+2H2O--->2KOH+H2
Tỉ lệ: 2:2:2:1
e, 4Na+O2--->2Na2O
Tỉ lệ: 4:1:2
f, 2KClO3--->2KCl+3O2
Tỉ lệ: 2:2:3
Đúng 0
Bình luận (0)
Viết các phương trình phản ứng cho hiện tượng mô tả dưới đây: Dẫn khí CO qua bột CuO nung nóng thu được hh chất rắn A và khí B. Cho hh A vào dd \(H_2SO_4\) đặc nóng. Dẫn khí B vào dd \(Ca(OH)_2\) dư
\(CO+CuO\underrightarrow{t^0}Cu+CO_2\)
Hỗn hợp A gồm Cu và CuO dư sau phản ứng
\(Cu+2H_2SO_{4\left(đ,t^0\right)}\rightarrow CuSO_4+SO_2+2H_2O\)
\(CuO+H_2SO_{4\left(đ,t^0\right)}\rightarrow CuSO_4+H_2O\)
\(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3+H_2O\)
Đúng 2
Bình luận (0)
\(CO+CuO\xrightarrow[]{t^0}Cu+CO_2\\ Cu+2H_2SO_4\left(đặc,t^0\right)\xrightarrow[]{}CuSO_4+2H_2O+SO_2\\ CO_2+Ca\left(OH\right)_2+CaCO_3\downarrow+H_2O\)
Đúng 0
Bình luận (0)