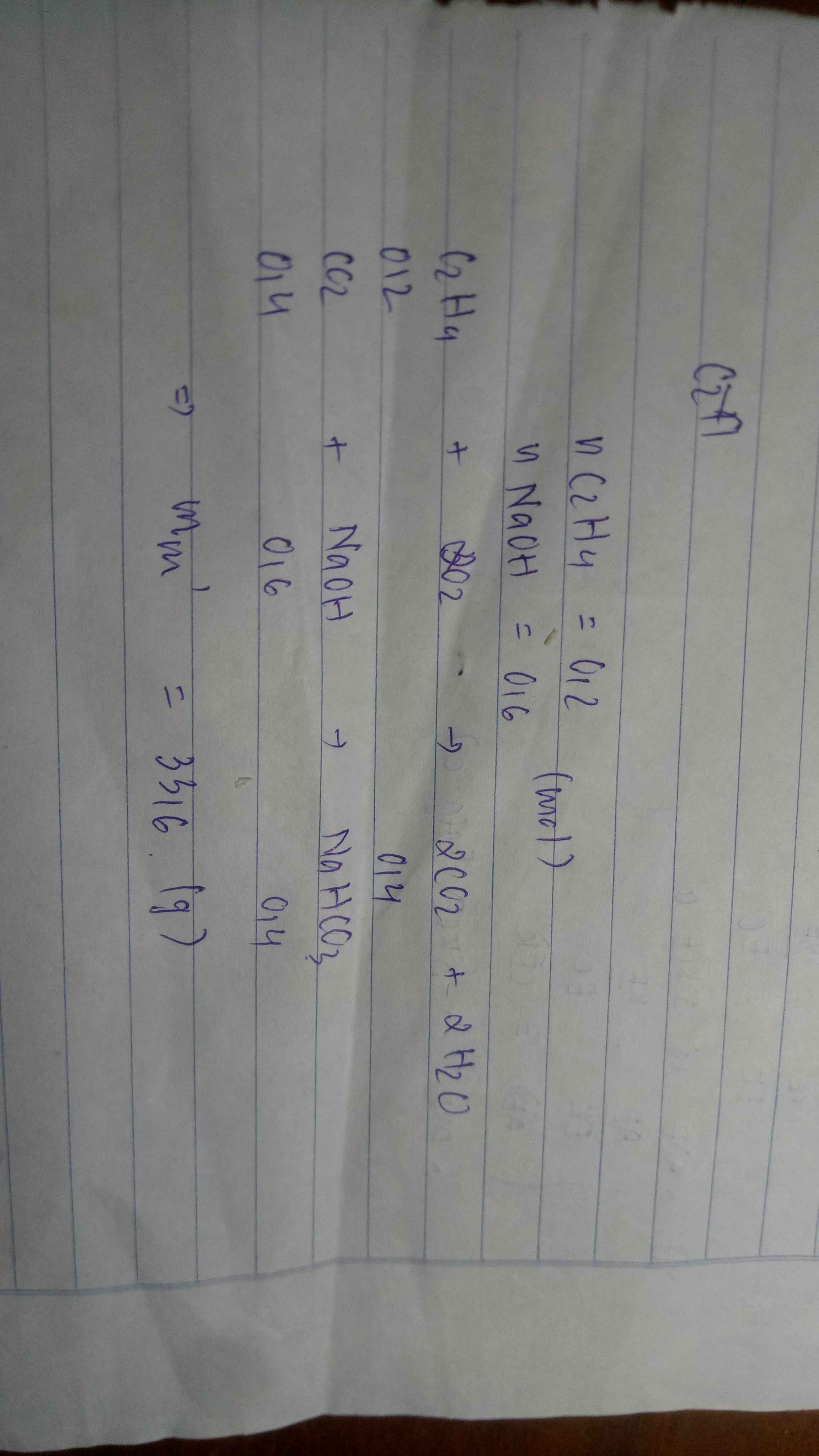đốt cháy hoàn toàn 6,72 lít khí h2s ở đktc rồi cho toàn bộ lượng khí sinh ra hấp thụ bởi 200ml đ naoh 2m . muối gì sinh ra sau phản ứng ? bao nhiêu gam ?

Những câu hỏi liên quan
Bài 2:Đốt cháy hoàn toàn 11,2 lít khí metan(ĐKTC) Hãy tính:
a) Thể tích không khí cần dùng (ĐKTC)
b) Nếu dùng 500 ml dung dịch NaOH 0,5 M hấp thụ toàn bộ lượng CO2 sinh ra ở trên.Tính khối lượng muối thu được sau phản ứng
a.\(n_{CH_4}=\dfrac{V_{CH_4}}{22,4}=\dfrac{11,2}{22,4}=0,5mol\)
\(CH_4+2O_2\rightarrow\left(t^o\right)CO_2+2H_2O\)
0,5 1 0,5 ( mol )
\(V_{kk}=V_{O_2}.5=\left(1.22,4\right).5=112l\)
b.\(n_{NaOH}=0,5.0,5=0,25mol\)
\(NaOH+CO_2\rightarrow NaHCO_3\)
0,25 < 0,5 ( mol )
0,25 0,25 ( mol )
\(m_{NaHCO_3}=0,25.84=21g\)
Đúng 1
Bình luận (1)
CH4+2O2-to>CO2+2H2O
0,5-----1----------0,5 mol
n CH4=
Đúng 0
Bình luận (2)
Bài 1:Đốt cháy hoàn toàn 11,2 lít khí metan(ĐKTC) Hãy tính:
a) Thể tích không khí cần dùng (ĐKTC)
b) Nếu dùng 500 ml dung dịch NaOH 0,5 M hấp thụ toàn bộ lượng CO2 sinh ra ở trên.Tính khối lượng muối thu được sau phản ứng
CH4+2O2-to>CO2+2H2O
0,5-----1----------0,5 mol
n CH4=\(\dfrac{11,2}{22,4}\)=0,5 mol
=>Vkk=1.22,4.5=112l
NaOH+CO2->NaHCO3
0,25------0,25-------0,25
n NaOH=0,5.0,5=0,25 mol
=>Tạo ra muối axit, CO2 dư
=>m NaHCO3=0,25.84=21g
Đúng 1
Bình luận (0)
hỗn hợp khí A gồm CO và một hidrocacbon X. Đốt cháy hoàn toàn 8,96 lít khí A thu được 10,8 gam nước; toàn bộ lượng khí CO2 sinh ra trong phản ứng được hấp thụ vào 69,2 gam dung dịch NaOH, thu được dung dịch chứa hỗn hợp muối Na2CO3 và NaHCO3 có nồng độ tương ứng là 21,2% và 42%. a/Hãy xác định CTPT của hidrocacbon X và % thể tích các khí trong hỗn hợp A. Biết 2,688 lít khí A cân nặng 3,36 gam.Các thể tích khí đo ở đktc b/Tính thể tích dung dịch KOH 0,8M đủ để hấp thu toàn bộ lượng khí CO2 sinh r...
Đọc tiếp
hỗn hợp khí A gồm CO và một hidrocacbon X. Đốt cháy hoàn toàn 8,96 lít khí A thu được 10,8 gam nước; toàn bộ lượng khí CO2 sinh ra trong phản ứng được hấp thụ vào 69,2 gam dung dịch NaOH, thu được dung dịch chứa hỗn hợp muối Na2CO3 và NaHCO3 có nồng độ tương ứng là 21,2% và 42%. a/Hãy xác định CTPT của hidrocacbon X và % thể tích các khí trong hỗn hợp A. Biết 2,688 lít khí A cân nặng 3,36 gam.Các thể tích khí đo ở đktc b/Tính thể tích dung dịch KOH 0,8M đủ để hấp thu toàn bộ lượng khí CO2 sinh ra ở trên tạo dung dịch chứa hỗn hợp 2 muối
a) Gọi số mol Na2CO3, NaHCO3 là a, b (mol)
Có \(\dfrac{m_{Na_2CO_3}}{m_{NaHCO_3}}=\dfrac{106a}{84b}=\dfrac{21,2\%}{42\%}\)
=> \(\dfrac{a}{b}=\dfrac{2}{5}\)
Bảo toàn C: nCO2 = a + b = 3,5a (mol)
mdd sau pư = 69,2 + 154a (g)
=> \(C\%_{Na_2CO_3}=\dfrac{106a}{69,2+154a}.100\%=21,2\%\)
=> a = 0,2 (mol)
=> b = 0,5 (mol)
=> nC = 0,7 (mol)
\(n_{H_2O}=\dfrac{10,8}{18}=0,6\left(mol\right)\) => nH = 1,2 (mol)
\(\overline{M}_A=\dfrac{3,36}{\dfrac{2,688}{22,4}}=28\left(g/mol\right)\)
Mà MCO = 28 (g/mol)
=> MX = 28 (g/mol)
=> X là C2H4
Đặt \(\left\{{}\begin{matrix}n_{CO}=x\left(mol\right)\\n_{C_2H_4}=y\left(mol\right)\end{matrix}\right.\)
Bảo toàn C: x + 2y = 0,7
Và x + y = \(\dfrac{8,96}{22,4}=0,4\)
=> x = 0,1 (mol); y = 0,3 (mol)
=> \(\left\{{}\begin{matrix}\%V_{CO}=\dfrac{0,1}{0,4}.100\%=25\%\\\%V_{C_2H_4}=\dfrac{0,3}{0,4}.100\%=75\%\end{matrix}\right.\)
b)
Xét tỉ lệ T = \(\dfrac{n_{KOH}}{n_{CO_2}}=\dfrac{n_{KOH}}{0,7}\)
Pư tạo ra 2 muối khi 1 < T < 2
<=> \(1< \dfrac{n_{KOH}}{0,7}< 2\)
<=> 0,7 < nKOH < 1,4
Vậy \(0,875\left(l\right)< V_{dd}< 1,75\left(l\right)\)
Đúng 3
Bình luận (0)
n H2O=0,1 mol
-> V H2O=2,24 lít
2CO + O2-to->2CO2
a-> 0,5a-> a lít
CxHy + (x+y/4)O2-to->xCO2+y/2H2O
b-> b(x+y/4)-> bx -> 0,5by lít
a+b=6,72
0,5a +bx +by/4=7,84
a+bx =8,96
0,5by=2,24
giải pt
a=4,48
b=2,24
x=2
y=2
-> CT :C2H2
CH nối ba CH
%V CO=66,67%
%V C2H2=33,33%
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn m gam Cácbon bằng khí o2 thu được khí co2 . hấp thụ toàn bộ lượng khí CO2 sinh ra vào 2 lít dung dịch hỗn hợp X gam NaOH 0,03M và Ca(OH)2 0,02M, Sau khi phản ứng xảy ra hoàn toàn thì thu được 3 gam kết tủa .tính giá trị của m
Làm giúp em với ạ!!!
(☆▽☆)
Đốt cháy hoàn toàn 4,48 lít khí C2H4( đktc). Toàn bộ lượng khí sinh ra dẫn qua 300 ml dung
dịch NaOH 2M. Phản ứng kết thúc tổng khối lượng muối thu được
A.21,2g B.16,8 g C.38 g D.Một đáp án khác
Đốt cháy hoàn toàn m gam cacbon trong không khí O2 thu được CO2. Hấp thụ toàn bộ lượng khí CO2 sinh ra vào 2 lít dung dịch hỗn hợp X gồm NaOH 0.03M và Ca(OH)2 0,02M, sau khi các phản ứng xảy ra hoàn toàn thì thu được 3gam kết tủa. Tính giá trị của M
Xem chi tiết
\(n_{NaOH}=2.0,03=0,06\left(mol\right)\)
\(n_{Ca\left(OH\right)2}=2.0,02=0,04\left(mol\right)\)
\(n_{CaCO3}=\dfrac{3}{100}=0,03\left(mol\right)\)
Thứ tự các pthh :
\(C+O_2-t^o->CO_2\) (1)
\(CO_2+Ca\left(OH\right)_2-->CaCO_3+H_2O\) (2)
\(CO_2+2NaOH-->Na_2CO_3+H_2O\) (3)
\(CO_2+Na_2CO_3-->2NaHCO_3\) (4)
\(CO_2+CaCO_3-->Ca\left(HCO_3\right)_2\) (5)
Vì \(n_{CaCO3}< n_{Ca\left(OH\right)2}\left(0,03< 0,04\right)\) => Có 2 giá trị của CO2 thỏa mãn
TH1: CO2 thiếu ở pứ 2 => Chỉ xảy ra pứ (1) và (2) => Không có pứ hòa tan kết tủa
Theo pthh (2) : \(n_{CO_2}=n_{CaCO3}=0,03\left(mol\right)\)
Bảo toản C : \(n_C=n_{CO2}=0,03\left(mol\right)\)
=> m = 0,03.12 = 0,36 (g)
TH2 : CO2 dư ở pứ (2) ; (3); (4), đến pứ (5) thì thiếu => Có pứ hòa tan kết tủa
Xét pứ (2); (3); (4) ; (5) :
\(\Sigma n_{CO2}=n_{Ca\left(OH\right)2}+\dfrac{1}{2}n_{NaOH}+n_{Na2CO3}+n_{CaCO3\left(tan\right)}\)
\(=n_{Ca\left(OH\right)2}+\dfrac{1}{2}n_{NaOH}+\dfrac{1}{2}n_{NaOH}+\left(n_{CaCO3\left(sinh.ra\right)}-n_{CaCO3thu.duoc}\right)\)
\(=n_{Ca\left(OH\right)2}+n_{NaOH}+\left(n_{Ca\left(OH\right)2}-0,03\right)\)
\(=2n_{Ca\left(OH\right)2}+n_{NaOH}-0,03\)
\(=2.0,04+0,06-0,03\)
\(=0,09\left(mol\right)\)
Bảo toàn C : \(n_C=n_{CO2}=0,09\left(mol\right)\)
\(\Rightarrow m=0,09.12=1,08\left(g\right)\)
Đúng 0
Bình luận (2)
bạn ơi, bạn sửa cho mình TH2 từ đoạn :
\(n_{CO2}=2.0,04+0,06-0,03=0,11\left(mol\right)\)
Bảo toàn C : \(n_C=n_{CO2}=0,11\left(mol\right)\)
=> mC = 0,11.12 = 1,32 (g)
p/s: sorry nhé, mình tính nhầm số mol co2 nên mới sai
Đúng 1
Bình luận (0)
Hấp thụ hoàn toàn 6,72 lít khí H 2 S (đktc) vào dung dịch chứa 16g NaOH. Tiến hành cô cạn dung dịch sau phản ứng thu được lượng muối khan là
A. 19,0 gam.
B. 20,8 gam.
C. 21,2 gam.
D. 12,1 gam.
Đốt cháy hoàn toàn 0,448 khí axetilen(đktc) A) Tính thể tích không khí cần dùng để đốt cháy hoàn toàn khi trên B) để hấp thụ hoàn toàn khí sinh ra sau phản ứng trên cần dùng bao nhiêu ml dung dịch Ca(OH)2 0,2 M?
C2H2+5\2O2-to>2CO2+H2O
0,02--------0,05--------0,04
CO2+Ca(OH)2->CaCO3+H2O
0,04---------0,04
n C2H2=0,02 mol
=>Vkk=0,05.22,4.5=5,6l
VCa(OH)2=\(\dfrac{0,04}{0,2}\)=0,2l=200ml
Đúng 3
Bình luận (0)
Cho 3,36 lít khí H2S (đktc) phản ứng hoàn toàn với 250 ml dd NaOH 1M. Tính khối lượng muối khan sinh ra
\(n_{NaOH}=0,25.1=0,25\left(mol\right)\\ n_{H_2S}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
\(T=\dfrac{0,25}{0,15}=\dfrac{5}{3}\rightarrow\) Tạo cả 2 muối
Gọi \(\left\{{}\begin{matrix}n_{NaOH\left(\text{tạo muối trung hoà}\right)}=a\left(mol\right)\\n_{NaOH\left(\text{tạo muối axit}\right)}=b\left(mol\right)\end{matrix}\right.\)
PTHH:
2NaOH + H2S ---> Na2S + 2H2O
a \(\dfrac{a}{2}\) \(\dfrac{a}{2}\)
NaOH + H2S ---> NaHS + H2O
b b b
Hệ pt \(\left\{{}\begin{matrix}a+b=0,25\\\dfrac{a}{2}+b=0,15\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,2\left(mol\right)\\b=0,05\left(mol\right)\end{matrix}\right.\)
\(\rightarrow m_{muối}=\dfrac{0,2}{2}.78+0,05.56=10,6\left(g\right)\)
Đúng 3
Bình luận (0)