Từ 80 tấn quặng FeS2 chứa 40% lưu huỳnh sản xuất được 92 tấn H2SO4
a) tính hiệu suất của quá trình
b) từ 92 tấn H2SO4 có thể pha chế thành bao nhiêu tấn dd H2SO4
mình cần gấp gấp cực kì giúp mình
nha
Từ 80 tấn quặng FeS2 chứa 40% lưu huỳnh sản xuất được 92 tấn H2SO4
a) tính hiệu suất của quá trình
b) từ 92 tấn H2SO4 có thể pha chế thành bao nhiêu tấn dd H2SO4
giúp mình nha mấy chế
Từ 1,2 tấn quặng pillit sắt (FeS2) có thể sản xuất được bao nhiêu tấn dung dịch H2SO4 50%, biết hiệu suất của quá trình sản xuất là 80%.
Đổi 1,2 tấn = 1200 kg
Ta có: \(n_{FeS_2}=\dfrac{1200}{120}=10\left(kmol\right)\)
Bảo toàn Lưu huỳnh: \(n_{H_2SO_4\left(lý.thuyết\right)}=2n_{FeS_2}=20\left(kmol\right)\)
\(\Rightarrow m_{ddH_2SO_4\left(thực\right)}=\dfrac{20\cdot98}{50\%}\cdot80\%=3136\left(kg\right)=3,136\left(tấn\right)\)
Từ 1 tấn quặng Lưu huỳnh có 2% tạp chất cho người ta có thể sản xuất bao nhiêu tấn dung dịch h2so4 98% với hiệu suất chung của quá trình sản suất là 80%
Từ 80 tấn quặng FeS2 chứa 40% lưu huỳnh sản xuất được 92 tấn H2SO4
a) tính hiệu suất của quá trình
b) từ 92 tấn H2SO4 có thể pha chế thành bao nhiêu tấn dd H2SO4
FeS2+8HNO3→2H2O+2H2SO4+5NO+Fe(NO3)3
a) khối lượng S trong quặng pirit:
mS=80*40%=32(tấn)
khối lượng S trong H2SO4
m=92:98*32=30(tấn)
H=\(\frac{30}{32}\cdot100\%\)=93,75%
b) C%=\(\frac{m_{ct}}{m_{dd}}\cdot100\%\) =???(thiếu đề thì phải bạn xem lại )
trong công nghiệp để sản xuất được 58,8 tấn h2so4 phải dùng 80 tấn quặng pirit chứa 75% FeS2 .Tính hiệu suất của quá trình sản xuất H2SO4 (Please!! Help me)
Trong công nghiệp người ta sản xuất axít sunfuric theo sơ đồ sau: FeS2 → SO2 → SO3 → H2SO4 . Người ta sử dụng 15 tấn quặng pirit sắt (chứa 80% FeS2) để sản xuất ra 39,2 tấn dung dịch H2SO4 40%. Vậy hiệu suất chung cho cả quá trình sản xuất axít sunfuric từ quặng trên là:
A. 40%
B. 60%
C. 80%
D. 62,5%
Trong công nghiệp người ta sản xuất axit sunfuric theo sơ đồ sau:
FeS2 → SO2 → SO3 → H2SO4.
Người ta sử dụng 15 tấn quặng pirit sắt (chứa 80% FeS2) để sản xuất ra 39,2 tấn dung dịch H2SO4 40%. Vậy hiệu suất chung cho cả quá trình sản xuất axit sunfuric từ quặng trên là:
A. 40%.
B. 60%.
C. 80%.
D. 62,5%
Đáp án C.
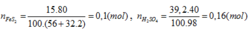
FeS2→ 2H2SO4
0,08 ← 0,16 (mol)
H% = 0,08.100/0,1= 80%
Từ 40 tấn quặng Pirit chứa 40% lưu huỳnh, người ta sản xuất được 73,5 tấn axit sunfuric.
a) Tính hiệu suất của quá trình sản xuất axit sunfuric.
b) Tính khối lượng của dd axit sunfuric 50% thu được từ 73,5 tấn H2SO4 đã được sản xuất ở trên 

Đề có phải là : ' Từ 80 tấn quặng Pirit chứa 40% lưu huỳnh , người ta sản xuất được 73,5 tấn axit sunfuric . '' đúng không
không phải
Câu 7: Từ 160 tấn quạng pipi sắt FeS2 (chứa 40% lưu huỳnh Agta sản xuất được 147 tấn axit sunfuric. Tính hiệu suất của quá trình sản xuất axit sunfuric H2SO4
: trog FeS2 có : %S = (32*2*100):120 = 160/3%* 40% = 64g
mFé2 = 64*160/3% = 120 TẤN
120 TẤN TẠO 196 (98*2) TẤN AXIT
H = 147*100/196=75%