Có 8 dung dịch chứa: NaNO3, Mg(NO3)2, Fe(NO3)2, Cu(NO3)2, Na2SO4, MgSO4, FeSO4, CuSO4. Hãy nêu các thuốc thử và trình bày phương án phân biệt 8 dung dịch nói trên.

Những câu hỏi liên quan
Có 8 dung dịch chứa:
N
a
N
O
3
,
M
g
N
O
3
2
,
F
e
N
O
3
2
C...
Đọc tiếp
Có 8 dung dịch chứa:
N a N O 3 , M g N O 3 2 , F e N O 3 2 C u N O 3 2 , N a 2 S O 4 , M g S O 4 , F e S O 4 , C u S O 4 .
Hãy nêu 2 thuốc thử cần để nhận biết 8 dung dịch trên
A. NaOH, NaCl
B. HCl, NaCl
C. NaOH, B a C l 2
D. HCl, NaOH
Trích mẫu thử đánh thứ tự từ 1 đến 8, cho dd BaCl2 vào các mẫu thử
- Nhóm 1: Tạo kết tủa trắng thì chất ban đầu là
M g 2 S O 4 , F e S O 4 , N a 2 S O 4 , C u S O 4
Nhóm 2: Không có kết tủa thì chất ban đầu là
N a N O 3 , M g N O 3 , F e N O 3 , C u N O 3
Cho NaOH vào nhóm 1.
+ Trường hợp tạo kết tủa trắng thì chất ban đầu là M g O H 2
M g S O 4 + 2 N a O H → M g O H 2 + N a 2 S O 4
+ Trường hợp tạo kết tủa trắng xanh hóa nâu đỏ trong không khí thì chất ban đầu là F e S O 4 :
F e S O 4 + 2 N a O H → F e O H 2 + N a 2 S O 4 4 F e O H 2 + O 2 + 2 H 2 O → 4 F e O H 3
+ Trường hợp tạo kết tủa màu xanh lam là :
C u S O 4 + 2 N a O H → C u O H 2 + N a 2 S O 4
+ Trường hợp không có hiện tượng nào xảy ra là N a 2 S O 4 .
Cho NaOH vào nhóm 2, hiện tượng tương tự như nhóm 1, giúp ta nhận biết 4 chất nhóm 2.
⇒ Chọn C.
Đúng 0
Bình luận (0)
Có các dung dịch al(no3)3, NaNO3, mg(no3)2, H2SO4. Thuốc thử để phân biệt các dung dịch đó là: A.dd BaCl2 B.dd NaOH C.dd CH3COOAg D.quì tím
Đọc tiếp
Có các dung dịch al(no3)3, NaNO3, mg(no3)2, H2SO4. Thuốc thử để phân biệt các dung dịch đó là:
A.dd BaCl2
B.dd NaOH
C.dd CH3COOAg
D.quì tím
Chọn B
Với Al(NO3)3 cho kết tủa sau đó tan
Với Mg(NO3)2 cho kết tủa không tan
Đổ hai dung dịch còn lại vào dung dịch Al(NO3)3 có kết tủa là H2SO4
Còn lại là NaNO3
Đúng 0
Bình luận (0)
A/ Chỉ dùng một thuốc thử hãy phân biệt các dung dịch sau:
NaOH, CuSO4, Fe(NO3)3, Fe(NO3)2, NH4Cl, AlCl3
B/ Có 5 mẫu kim loại :Ba, Mg, Fe, Ag, Al chỉ dùng dung dịch H2SO4 loãng (không được dùng chất khác ). Hãy nhận biết ra 5 kim loại trên.
giúp mình với!!!!!!!
a. Cho dung dịch NaOH lần lượt vào các mẫu thử :
- Kết tủa xanh lam : CuSO4
- Kết tủa nâu đỏ : Fe(NO3)3
- Kết tủa trắng xanh , hóa nâu đỏ trong không khí : Fe(NO3)2
- Sủi bọt khí mùi khai : NH4Cl
- Kết tủa keo trắng , tan dần trong NaOH dư : AlCl3
- Không HT : NaOH
\(2NaOH+CuSO_4\rightarrow Na_2SO_4+Cu\left(OH\right)_2\)
\(3NaOH+Fe\left(NO_3\right)_3\rightarrow3NaNO_3+Fe\left(OH\right)_3\)
\(2NaOH+Fe\left(NO_3\right)_2\rightarrow2NaNO_3+Fe\left(OH\right)_2\)
\(NaOH+NH_4Cl\rightarrow NaCl+NH_3+H_2O\)
\(3NaOH+AlCl_3\rightarrow3NaCl+Al\left(OH\right)_3\)
\(NaOH+Al\left(OH\right)_3\rightarrow NaAlO_2+2H_2O\)
Đúng 1
Bình luận (0)
a, - Trích từng dung dịch làm mẫu thử và đánh số thứ tự .
- Chọn thuốc thử là dung dịch NaOH dư .
- Nhỏ vào từng mẫu thử .
+, Mẫu thử không hiện tượng là NaOH
+, Mẫu thử tạo kết tủa xanh lơ là CuSO4
PTHH : CuSO4 + 2NaOH -> Cu(OH)2 + Na2SO4
+, Mẫu thử tạo kết tủa nâu đỏ là Fe(NO3)3
PTHH : Fe(NO3)3 + 3NaOH -> 3NaNO3 + Fe(OH)3
+, Mẫu thử tạo kết tủa trắng xanh rồi hóa nâu đỏ trong không khí là Fe(NO3)2
Fe(NO3)2 + 2NaOH -> Fe(OH)2 + 2NaNO3
2Fe(OH)2 + O2 + H2O -> 2Fe(OH)3
+, Mẫu thử tạo khí mùi khai là NH4Cl
PTHH : NH4Cl + NaOH -> NaCl + NH3 + H2O
+, Mẫu thử tạo kết tủa keo rồi tan là AlCl3
3NaOH + AlCl3 -> Al(OH)3 + 3NaCl
Al(OH)3 + NaOH -> NaAlO2 + H2O
Đúng 1
Bình luận (0)
b.
Cho dung dịch H2SO4 loãng lần lượt vào từng chất :
- Tan , sủi bọt , tạo kết tủa trắng : Ba
- Tan , sủi bọt : Mg , Fe , Al
- Không tan : Ag
Cho Ba phản ứng đến dư với dung dịch H2SO4 => Lọc kết tủa , thu được dung dịch Ba(OH)2
Cho dung dịch Ba(OH)2 vào các dung dịch còn lại :
- Kết tủa trắng : chất ban đầu là : Mg
- Kết tủa trắng xanh , hóa nâu đỏ trong không khí : Fe
- Kết tủa keo trắng , tan dần : Al
PTHH em tự viết nhé !
Đúng 2
Bình luận (0)
hãy nhạn biết các ống nghiêm mất nhãn chứa các dd sau:
a/Na2CO3,NaOH,NaCl,HCl.
b/HCl,NaOH,Na2SO4;NaCl,NaNO3.
c/NaNO3,Mg(NO3)2,Fe(NO3)2,Cu(NO3)2.
d/FeSO4,Fe2(SO4)3,MgSO4.
a) - Lấy mỗi dung dịch một ít rồi đổ từ từ vào nhau theo từng cặp thì nhận thấy khi cho HCl vào Na2CO3 hay ngược lại có khí bay ra:
2 HCl + Na2CO3 ------------> 2 NaCl + CO2 +H2O
- Chia làm hai nhóm:
Nhóm 1 gồm : H2O và NaCl
Nhóm 2 gồm : HCl và Na2CO3
- Đem cô cạn nhóm 1 : mẫu thử nào sau khi cô cạn có cặn trắng là NaCl , mẫu thử nào không có cặn là H2O
- Đem cô cạn nhóm 2 : mẫu thử nào sau khi cô cạn có cặn trắng là Na2CO3 , mẫu thử nào không có cặn trắng là HCl
Đúng 0
Bình luận (0)
b)lần 1:trích từng mẫu thử rồidùng quỳ tím
-quỳ chuyển đỏ-->HCl
-quỳ chuyển xanh-->Na0H
-quỳ ko chuyển màu-->NaSO4,NaCl,NaNO3 (1)
Để phân biệt (1) dùng dd Ba(0H)2
-xh kết tủa trắng --->Na2S04
Ba(0H)2+Na2S04--->BaS04+2Na0H
-ko hiện tượng--->NaCl,NaNO3
Để phân biệt tiếp NaCl,NaNO3 thì dùng dd AgN03
-xh kết tủa trắng --->NaCl
NaCl+AgN03--->AgCl+NaN03
- ko hiện tượng là NaN03
Đúng 0
Bình luận (1)
Nhận biết 8dd
NaNO3 , Mg(NO3)2 , Fe(NO3)2 , Cu(NO3)2 , Na2SO4 , MgSO4 , CuSO4
* Dùng Ba(OH)2 vào các dd:
- Không xuất hiện dấu hiệu là NaNO3
- Xuất hiện kết tủa là trắng là gồm
Mg(NO3)2 + Ba(OH)2 --------- Ba(NO3)2 + Mg(OH)2
MgSO4 + Ba(OH)2 --------- BaSO4 + Mg(OH)2
- Xuất hiện kết tủa trắng có lẩn màu xanh là gồm:
Fe(NO3)2 + Ba(OH)2 ------------ Ba(NO3)2 + Fe(OH)2
FeSO4 + Ba(OH)2 ------------ BaSO4 + Fe(OH)2
- Xuất hiện kết tủa xanh gồm:
Cu(NO3)2 + Ba(OH)2 ------------- Ba(NO3)2 + Cu(OH)2
CuSO4 + Ba(OH)2 ------------ BaSO4 + Cu(OH)2
Lọc lấy các kết tủa mỗi phần hòa tan vào dd HCl
Cho dd HCl dư vào hai kết tủa trắng
Kết tủa tan hết trong dd HCl thì dd ban đầu là Mg(NO3)2
do phản ứng Mg(OH)2 + HCl ----------- MgCl2 + H2O
Kết tủa tan một phần còn một phần không tan ( do BaSO4) là MgSO4
-- Tương tự muối Fe và Cu
Đúng 0
Bình luận (0)
Cách nhận biết của 2 bạn kia cũng đúng nhé, bạn có thể tham khảo thêm cách này
cho NaOH vào :
Nhóm 1 \(\begin{cases}NaNO3\\Na2SO4\end{cases}\) không hiện tượng
Nhóm 2\(\begin{cases}Mg\left(NO3\right)2\\MgSO4\end{cases}\) có xuất hiện kết tủa trắng là của Mg(OH)2
Nhóm 3 \(\begin{cases}Cú\left(NO3\right)2\\CuSO4\:\end{cases}\) có xuất hiện kết tủa xanh lơ ( xanh da trời) là của Cu(OH)2
Fe(NO3)2 kết tủa trắng xanh (Nhận biết )
Cho Ba(OH)2 vào từng nhóm trên:
Nhóm 1 : xuất hiện kết tủa trắng là Na2SO4 ( nhận biết )
Nhóm 3 : Xuất hiện kết tủa trắng xanh là CuSO4 ( nhận biết )
Nhóm 2 : sau khi Ba(OH)2 vào ta thêm HCl , ống nào kết tủa tan thì là Mg(NO3)2 ( nhận biết )
Đúng 0
Bình luận (0)
Xem thêm câu trả lời
Cho một mảnh Mg vào dung dịch chứa hỗn hợp các muối: Al(NO3)3, Cu(NO3)2, Zn(NO3)2, NaNO3, Fe(NO3)3, AgNO3. Sau khi phản ứng xảy ra hoàn toàn thu được dung dịch A và chất rắn B chứa hỗn hợp kim loại. Hãy xác định thành phần các chất có trong dung dịch A và các chất trong B, viết các phương trình phản ứng xảy ra trong các trường hợp sau:a) Dung dịch A chứa 3 muối.b) Chất rắn B chứa 4 kim loại.
Đọc tiếp
Cho một mảnh Mg vào dung dịch chứa hỗn hợp các muối: Al(NO3)3, Cu(NO3)2, Zn(NO3)2, NaNO3, Fe(NO3)3, AgNO3. Sau khi phản ứng xảy ra hoàn toàn thu được dung dịch A và chất rắn B chứa hỗn hợp kim loại. Hãy xác định thành phần các chất có trong dung dịch A và các chất trong B, viết các phương trình phản ứng xảy ra trong các trường hợp sau:
a) Dung dịch A chứa 3 muối.
b) Chất rắn B chứa 4 kim loại.
a) A chứa 3 muối là Mg(NO3)2, Al(NO3)3, NaNO3
PTHH:
\(Mg+2AgNO_3\rightarrow Mg\left(NO_3\right)_2+2Ag\)
\(Mg+2Fe\left(NO_3\right)_3\rightarrow Mg\left(NO_3\right)_2+2Fe\left(NO_3\right)_2\)
\(Mg+Cu\left(NO_3\right)_2\rightarrow Mg\left(NO_3\right)_2+Cu\)
\(Mg+Fe\left(NO_3\right)_2\rightarrow Mg\left(NO_3\right)_2+Fe\)
\(Mg+Zn\left(NO_3\right)_2\rightarrow Mg\left(NO_3\right)_2+Zn\)
B chứa các kim loại: Ag, Cu, Fe, Zn
b)
B chứa 4 kim loại: Ag, Cu, Fe, Zn
PTHH:
\(Mg+2AgNO_3\rightarrow Mg\left(NO_3\right)_2+2Ag\)
\(Mg+2Fe\left(NO_3\right)_3\rightarrow Mg\left(NO_3\right)_2+2Fe\left(NO_3\right)_2\)
\(Mg+Cu\left(NO_3\right)_2\rightarrow Mg\left(NO_3\right)_2+Cu\)
\(Mg+Fe\left(NO_3\right)_2\rightarrow Mg\left(NO_3\right)_2+Fe\)
\(Mg+Zn\left(NO_3\right)_2\rightarrow Mg\left(NO_3\right)_2+Zn\)
=> A chứa các muối: NaNO3, Mg(NO3)2, Al(NO3)3 và có thể có Zn(NO3)2
a) A chứa 3 muối là Mg(NO3)2, Al(NO3)3, NaNO3
PTHH:
\(Mg+2AgNO_3\rightarrow Mg\left(NO_3\right)_2+2Ag\)
\(Mg+2Fe\left(NO_3\right)_3\rightarrow Mg\left(NO_3\right)_2+2Fe\left(NO_3\right)_2\)
\(Mg+Cu\left(NO_3\right)_2\rightarrow Mg\left(NO_3\right)_2+Cu\)
\(Mg+Fe\left(NO_3\right)_2\rightarrow Mg\left(NO_3\right)_2+Fe\)
\(Mg+Zn\left(NO_3\right)_2\rightarrow Mg\left(NO_3\right)_2+Zn\)
\(3Mg+2Al\left(NO_3\right)_3\rightarrow3Mg\left(NO_3\right)_2+2Al\)
B chứa các kim loại: Ag, Cu, Fe, Zn và có thể có Al
b)
B chứa 4 kim loại: Ag, Cu, Fe, Zn
PTHH:
\(Mg+2AgNO_3\rightarrow Mg\left(NO_3\right)_2+2Ag\)
\(Mg+2Fe\left(NO_3\right)_3\rightarrow Mg\left(NO_3\right)_2+2Fe\left(NO_3\right)_2\)
\(Mg+Cu\left(NO_3\right)_2\rightarrow Mg\left(NO_3\right)_2+Cu\)
\(Mg+Fe\left(NO_3\right)_2\rightarrow Mg\left(NO_3\right)_2+Fe\)
\(Mg+Zn\left(NO_3\right)_2\rightarrow Mg\left(NO_3\right)_2+Zn\)
=> A chứa các muối: NaNO3, Mg(NO3)2, Al(NO3)3 và có thể có Zn(NO3)2
Đúng 0
Bình luận (0)
Có 6 dung dịch đựng trong 6 lọ mất nhãn : Mg
(
N
O
3
)
2
, Zn, Pb
(
N
O
3
)
2
, Al
C
l
3
, KOH và NaCl. Chỉ dùng thêm dung dịch
A...
Đọc tiếp
Có 6 dung dịch đựng trong 6 lọ mất nhãn : Mg ( N O 3 ) 2 , Zn, Pb ( N O 3 ) 2 , Al C l 3 , KOH và NaCl. Chỉ dùng thêm dung dịch A g N O 3 và một thuốc thử nữa, hãy trình bày cách nhận biết từng dung dịch. Viết các phương trình hoá học dưới dạng phân tử và ion rút gọn của các phản ứng nhận biết đó.
Dùng dung dịch phenolphtalein nhận ra dung dịch KOH.
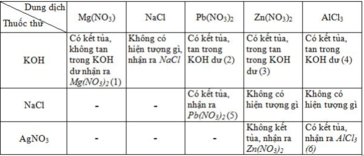
Các phương trình hoá học :
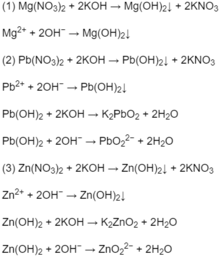
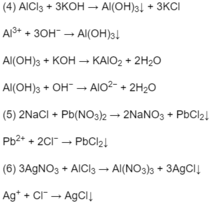
Đúng 0
Bình luận (0)
Chỉ dùng một thuốc thử, trình bày phương pháp phân biệt các dung dịch riêng biệt: NH4Cl, (NH4)2SO4, NaNO3, Al(NO3)3, MgCl2, FeCl2, FeCl3
Phương pháp: thử 5 hóa chất hữu dụng: Ba(OH)2, H2SO4, AgNO3, Quì, HCl
|
|
NH4Cl |
(NH4)2SO4 |
NaNO3 |
| Ba(OH)2 |
↑NH3 Mùi khai |
↑NH3 Mùi khai BaSO4 ↓trắng |
x |
|
|
MgCl2 |
FeCl2 |
FeCl3 |
|
|
Mg(OH)2 Trắng |
Fe(OH)2 xanh |
Fe(OH)3 Nâu đỏ |
|
|
Al(NO3)3 |
|
|
|
|
Al(OH)3 Trắng sau đó tan dần |
|
|
Đúng 0
Bình luận (0)
Chọn thuốc thử để phân biệt 3 dung dịch sau: KNO3 , Cu(NO3)2 , Fe(NO3)3.
A. NaOH
B. H2SO4
C. AgNO3
D. CO2
Đáp án A.
Mẫu không phản ứng là KNO3
Mẫu tạo tủa xanh là Cu(NO3)2
![]()
Mẫu tạo tủa đỏ nâu là Fe(NO3)3
![]()
Đúng 0
Bình luận (0)
















