Cân bằng các phương trình hóa học
cần khẩn ạ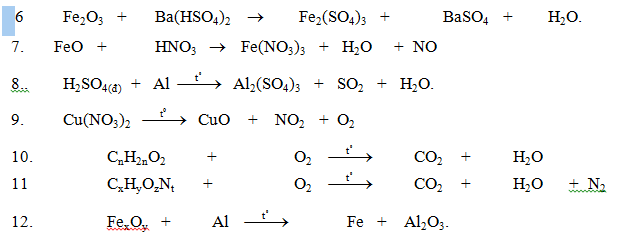
Cân bằng các phản ứng oxi hóa khử theo phương pháp thăng bằng electron, xác định chất khử, chất oxi hóa, quá trình khử và quá trình oxi hóa?
Al + HNO3 → Al(NO3)3 + NO2 + H2O
giải giúp em với ạ
\(Al:\) Chất khử
\(HNO_3:\) Chất OXH
\(Al\rightarrow Al^{+3}+3e\)
\(N^{+5}+1e\rightarrow N^{+4}\)
\(Al+6HNO_3\rightarrow Al\left(NO_3\right)_3+3NO_2+3H_2O\)
\(Al+6HNO_3->Al\left(NO_3\right)_3+3NO_2+3H_2O\)
Chất khử: Al, chất oxh: HNO3
| QT khử | N+5+1e --> N+4 | x3 |
| QT oxh | Al0 -3e--> Al+3 | x1 |
Ai Giải Thích chi tiết cách cân bằng phương trình hóa học giúp ạ
bạn xem thử nha


Điền thêm những công thức hóa học của những chất cần thiết vào các phương trình phản ứng hóa học sau đây rồi cân bằng phương trình: A l + H 2 S O 4 → ? + ?
2 A l + 3 H 2 S O 4 → A l 2 S O 4 3 + 3 H 2
Điền thêm những công thức hóa học của những chất cần thiết vào các phương trình phản ứng hóa học sau đây rồi cân bằng phương trình: C a O + H 3 P O 4 → ? + ?
3 C a O + 2 H 3 P O 4 → C a 3 P O 4 2 + 3 H 2 O
Điền thêm những công thức hóa học của những chất cần thiết vào các phương trình phản ứng hóa học sau đây rồi cân bằng phương trình: M g + H C l → ? + ?
Điền thêm những công thức hóa học của những chất cần thiết vào các phương trình phản ứng hóa học sau đây rồi cân bằng phương trình: M g O + H C l → ? + ?
Lấy ví dụ thực tế (và các phương trình hóa học) về các yếu tố ảnh hưởng đến cân bằng hóa học. (Bài 38 - Hóa 10)
Có 3 yếu tố làm ảnh hưởng đến cân bằng hóa học
- Ảnh hưởng của nhiệt độ đến cân bằng hóa học
VD: N2(k) + 3H2(k) ⇔ 2NH3(k) ∆Ho = -92,6kJ.
Vì ∆H0 < 0, khi nhiệt độ tăng, cân bằng chuyển dịch theo chiều nghịch (chiều thu nhiệt), nếu nhiệt độ của hệ giảm xuống thì cân bằng chuyển dịch theo chiều thuận (chiều tỏa nhiệt).
- Ảnh hưởng của áp suất đến cân bằng hóa học
VD : N2(k) + 3H2(k) ⇔ 2NH3(k)
Có ∆n = 2 – (3 + 1) = -2
+ Nếu P tăng ⇒ cân bằng dịch chuyển theo chiều P giảm (giảm số mol khí ∆n < 0). => Cân bằng chuyển theo chiều thuận
+ Nếu P giảm ⇒cân bằng dịch chuyển theo chiều P tăng (tăng số mol khí ∆n > 0). => Cân bằng chuyển theo chiều nghịch
-Ảnh hưởng của nồng độ đến cân bằng hóa học
C(r)+CO2(k)⇌2CO(k)
- Khi tăng CO2 thì cân bằng chuyển dịch theo chiều thuận (chiều làm giảm CO2).
- Khi giảm CO2 thì cân bằng chuyển dịch theo chiều nghịch (chiều làm tăng CO2).
Cân bằng các phương trình sau bằng phương pháp thăng bằng e, chỉ rõ đâu là chất oxi hóa, đâu là chất khử
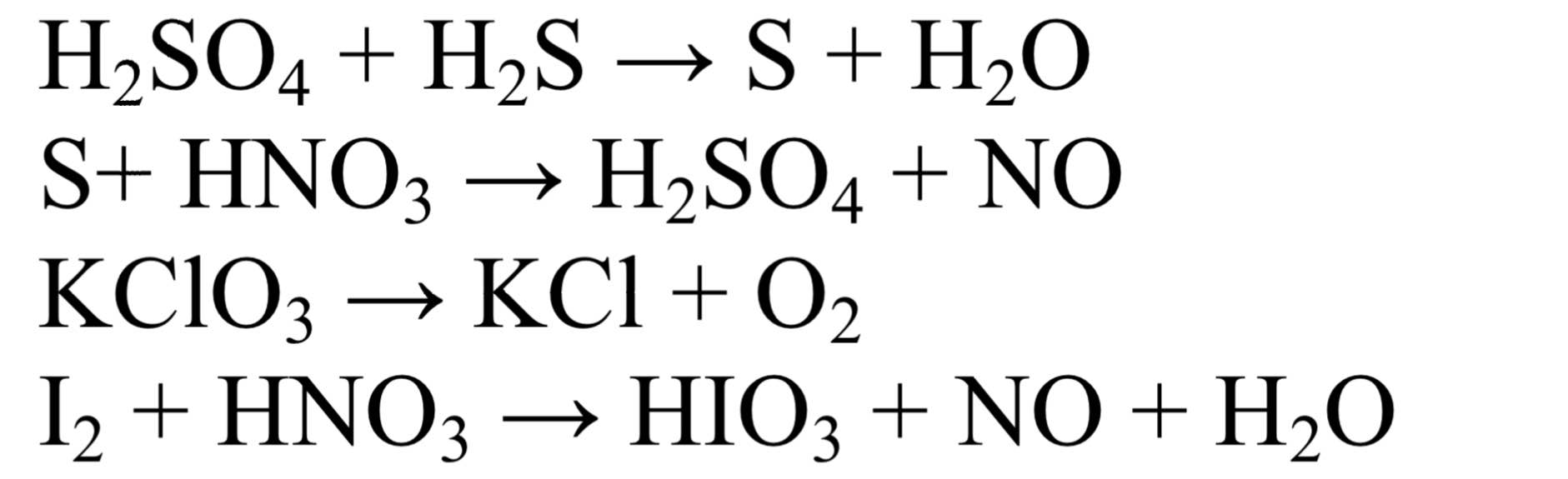
\(H_2SO_4+3H_2S->4S+4H_2O\)
Chất oxi hóa: H2SO4
Chất khử: H2S
| S+6 + 6e --> S0 | x1 |
| S-2 -2e --> S0 | x3 |
\(S+2HNO_3->H_2SO_4+2NO\)
Chất oxi hóa: HNO3
Chất khử: S
| S0 - 6e --> S+6 | x1 |
| N+5 + 3e --> N+2 | x2 |
\(2KClO_3->2KCl+3O_2\)
| Cl+5+6e-->Cl-1 | x2 |
| 2O3-2 -12e --> 3O20 | x1 |
\(3I_2+10HNO_3->6HIO_3+10NO+2H_2O\)
Chất oxi hóa: HNO3
Chất khử: I2
| I20 -10e --> 2I+5 | x3 |
| N+5 + 3e --> N+2 | x10 |
Cân bằng các phương trình phản ứng hóa học sau:
F e + C l 2 − t o → F e C l 3