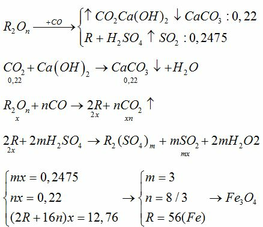Cho 46,4 gam một oxit kim loại tác dụng với vừa đủ 17,92 lít khí hidro (ddktc) . Cho toàn bộ lượng kim loại thu được tac dung het voi 43,8 gam HCl . Xác định công thức hóa học của oxit.(Cố gắng lên nha ^_^)

Những câu hỏi liên quan
Cho 46,4 gam một oxit kim loại tác dụng vừa đủ với 17,92 lít khí hiđrô (đktc) . Cho toàn bộ lượng kim loại thu được tác dụng hết với 43,8 gam HCl. Xác định công thức hóa học của oxit
Gọi CTHH của oxit là MxOy
PTHH: MxOy + yH2 --t--> xM + yH2O
xM + 2yHCl ----> xMCl2y/x + yH2
nH2 = 17,92/22,4=0,8 mol
Ta thấy: nO (MxOy) = nH2
=> nO(MxOy) = y = 0,8 mol
nHCl= 43,8/36,5= 1,2 mol
=> nM = 1,2.x/2y = 0,6x/y (mol)
mMxOy = mM + mO = M.(0,6x/y) + 0,8.16 = 46,4
=> 0,6Mx/y = 33,6
=> 0,6Mx = 33,6y
=> Mx = 56y
=> M = 28.2y/x
Chạy nghiệm và biện luận M theo 2y/x ta đc 2y/x = 2 thỏa mãn
=> M = 56 (Fe)
Mà 56x + 16.0,8 = 46,4
=> x = 0,6
=> x : y = 0,6 : 0,8 = 3 : 4
Vậy x = 3; y = 4
CTHH của oxit là Fe3O4
Đúng 0
Bình luận (0)
Gọi CTHH của oxit là MxOy
PTHH: MxOy + yH2 --t--> xM + yH2O
xM + 2yHCl ----> xMCl2y/x + yH2
nH2 = 17,92/22,4=0,8 mol
Ta thấy: nO (MxOy) = nH2
=> nO(MxOy) = y = 0,8 mol
nHCl= 43,8/36,5= 1,2 mol
=> nM = 1,2.x/2y = 0,6x/y (mol)
mMxOy = mM + mO = M.(0,6x/y) + 0,8.16 = 46,4
=> 0,6Mx/y = 33,6
=> 0,6Mx = 33,6y
=> Mx = 56y
=> M = 28.2y/x
Chạy nghiệm và biện luận M theo 2y/x ta đc 2y/x = 2 thỏa mãn
=> M = 56 (Fe)
Mà 56x + 16.0,8 = 46,4
=> x = 0,6
=> x : y = 0,6 : 0,8 = 3 : 4
Vậy x = 3; y = 4
CTHH của oxit là Fe3O4
Đúng 0
Bình luận (1)
Gọi CTHH của oxit là MxOy
PTHH: MxOy + yH2 --t--> xM + yH2O
xM + 2yHCl ----> xMCl2y/x + yH2
nH2= 17,92/22,4=0,8 mol
Ta thấy: nO(MxOy) = nH2
=> nO(MxOy) = y = 0,8 mol
nHCl= 43,8/36,5= 1,2 mol
=> nM = 1,2.x/2y = 0,6x/y (mol)
mMxOy = mM + mO = M.(0,6x/y) + 0,8.16 = 46,4
=> 0,6Mx/y = 33,6
=> 0,6Mx = 33,6y
=> Mx = 56y
=> M = 28.2y/x
Chạy nghiệm và biện luận M theo 2y/x ta đc 2y/x = 2 thỏa mãn
=> M = 56 (Fe)
Mà 56x + 16.0,8 = 46,4
=> x = 0,6
=> x : y = 0,6 : 0,8 = 3 : 4
Vậy x = 3; y = 4
CTHH của oxit là Fe3O4.
Đúng 0
Bình luận (2)
Xem thêm câu trả lời
Khử 3,48 gam một oxit kim loại M cần dùng 1,344 lít khí hiđro (ở đktc). Toàn bộ lượng kim loại thu được tác dụng với dung dịch HCl dư cho 1,008 lít khí hiđro (ở đktc). Xác định kim loại M và công thức hóa học của oxit trên?
CTHH: AxOy
\(n_{H_2}=\dfrac{1,344}{22,4}=0,06\left(mol\right)\)
PTHH: AxOy + yH2 --to--> xA + yH2O
\(\dfrac{0,06}{y}\)<--0,06---->\(\dfrac{0,06x}{y}\)
2A + 2nHCl --> 2ACln + nH2
\(\dfrac{0,06x}{y}\)---------------->\(\dfrac{0,03xn}{y}\)
=> \(\dfrac{0,03xn}{y}=\dfrac{1,008}{22,4}=0,045\left(mol\right)\)
=> \(\dfrac{y}{x}=\dfrac{2}{3}n\)
\(M_{A_xO_y}=\dfrac{3,48}{\dfrac{0,06}{y}}=58y\left(g/mol\right)\)
=> \(x.M_A=42y\)
=> \(M_A=\dfrac{42y}{x}=28n\left(g/mol\right)\)
Xét n = 2 thỏa mãn => MA = 56 (g/mol)
=> A là Fe
\(\dfrac{x}{y}=\dfrac{3}{2n}=\dfrac{3}{4}\) => CTHH: Fe3O4
Đúng 4
Bình luận (0)
Cho kim loại sắt Fe tác dụng vừa đủ với 147gam dung dịch H2SO4 có nồng độ 20℅ thu được muối và khí hidro. Dân toàn bộ khí hidro qua 16g oxit kim loại có hóa trị III. Xác định công thức hóa học của oxit cầu cíu các cao nhân
\(n_{H_2SO_4}=\dfrac{147.20\%}{98}=0,3\left(mol\right)\\ Fe+H_2SO_4\rightarrow FeSO_4+H_2\\ n_{H_2}=n_{axit}=0,3\left(mol\right)\\ Đặt:A_2O_3\\ A_2O_3+3H_2\rightarrow\left(t^o\right)2A+3H_2O\\ n_{oxit}=\dfrac{n_{H_2}}{3}=\dfrac{0,3}{3}=0,1\left(mol\right)\\ M_{oxit}=\dfrac{16}{0,1}=160\left(\dfrac{g}{mol}\right)=2M_A+48\\ \Rightarrow M_A=56\left(\dfrac{g}{mol}\right)\\ \Rightarrow A:Sắt\left(Fe=56\right)\\ \Rightarrow Oxit:Fe_2O_3\)
Đúng 1
Bình luận (0)
Khử hoàn toàn 12,76 gam một oxit kim loại (RxOy) bằng khí CO vừa đủ thu được kim loại R và khí CO2. Hấp thụ hết khí CO2 sinh ra vào dung dịch Ca(OH)2 dư, thu được 22 gam kết tủa trắng. Cho toàn bộ lượng kim loại R thu được ở trên tác dụng hết với dung dịch H2SO4 đặc nóng, dư thu được 5,544 lít một khí có mùi hắc (đktc). Xác định công thức của RxOy
Đọc tiếp
Khử hoàn toàn 12,76 gam một oxit kim loại (RxOy) bằng khí CO vừa đủ thu được kim loại R và khí CO2. Hấp thụ hết khí CO2 sinh ra vào dung dịch Ca(OH)2 dư, thu được 22 gam kết tủa trắng. Cho toàn bộ lượng kim loại R thu được ở trên tác dụng hết với dung dịch H2SO4 đặc nóng, dư thu được 5,544 lít một khí có mùi hắc (đktc). Xác định công thức của RxOy
Khử hoàn toàn 6,4 gam một oxit kim loại cần dùng 0,12 mol H2. Kim loại thu được cho tác dụng với dung dịch HCl dư thu được 0,08 mol H2. Xác định công thức hóa học của oxit kim loại trên
1.Cho 46,4 gam một oxit kim loại tác dụng vừa đủ với 17,92 lít khí hiđrô (đktc). Cho toàn bộ lượng kim loại thu được tác dụng hết với 43,8 gam HCl. Xác định công thức hóa học của oxit.
2.Cho 13,7 gam hỗn hợp X gồm Al và Fe tác dụng hết với dung dịch axit HCl. Sau phản ứng thu được dung dịch Y và V lít khí hiđrô (đktc). Khối lượng dung dịch Y nặng hơn hơn dung dịch axit ban đầu là 12,6 gam.
a. Viết các PTHH của phản ứng. Tính V
b. Tính thành phần % khối lượng mỗi kim loại trong X
Giúp mình nha....
Đọc tiếp
1.Cho 46,4 gam một oxit kim loại tác dụng vừa đủ với 17,92 lít khí hiđrô (đktc). Cho toàn bộ lượng kim loại thu được tác dụng hết với 43,8 gam HCl. Xác định công thức hóa học của oxit.
2.Cho 13,7 gam hỗn hợp X gồm Al và Fe tác dụng hết với dung dịch axit HCl. Sau phản ứng thu được dung dịch Y và V lít khí hiđrô (đktc). Khối lượng dung dịch Y nặng hơn hơn dung dịch axit ban đầu là 12,6 gam.
a. Viết các PTHH của phản ứng. Tính V
b. Tính thành phần % khối lượng mỗi kim loại trong X
Giúp mình nha...>-<
Gọi CTHH của oxit là MxOy
PTHH: MxOy + yH2 --t--> xM + yH2O
xM + 2yHCl ----> xMCl2y/x + yH2
nH2 = 17,92/22,4=0,8 mol
Ta thấy: nO (MxOy) = nH2 => nO(MxOy) = y = 0,8 mol
nHCl= 43,8/36,5= 1,2 mol
=> nM = 1,2.x/2y = 0,6x/y (mol)
mMxOy = mM + mO = M.(0,6x/y) + 0,8.16 = 46,4
=> 0,6Mx/y = 33,6
=> 0,6Mx = 33,6y
=> Mx = 56y
=> M = 28.2y/x
Chạy nghiệm và biện luận M theo 2y/x ta đc 2y/x = 2 thỏa mãn
=> M = 56 (Fe)
Mà 56x + 16.0,8 = 46,4
=> x = 0,6
=> x : y = 0,6 : 0,8 = 3 : 4
Vậy x = 3; y = 4
CTHH của oxit là Fe3O4
Đúng 0
Bình luận (0)
9. Khử 3,48 gam oxit một kim loại M cần dùng 1,344 lít CO (đktc). Toàn bộ lượng kim loại thu được cho tác dụng với dung dịch HCl dư thu được 1,008 lít H2 (đktc). Xác định kim loại M và oxit của nó.
Gọi CT oxit là M2Om
Mol H2 TN1=0,06 mol
Mol H2 TN2=0,045 mol
M2Om + mH2→ 2M + mH2O
0,06/m mol<=0,06 mol. =>0,12/m mol
=>0,06(2M+16m)/m=3,48
2M + 2nHCl→ 2MCln + nH2
0,12/m mol. 0,045 mol
⇒⇒0,045.2/n=0,12/m⇒⇒m=8/3; n=2 tm
Thay m=8/3 vào công thức tính m có M=56 FeFe
Oxit là Fe3O4 vì n=8/3
Đúng 1
Bình luận (10)
Khử hoàn toàn 32 g một oxit kim loại M cần dùng tới 13,44 lít H2. Cho toàn bộ kim loại thu được tác dụng với dung dịch HCl dư thì thu được 8,96 lít H2. Xác định kim loại m và công thức hóa học của oxit. Giải dễ hiểu nhất dùm mình nhan!
\(n_{H_2thuđược}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
\(n_{H_2cầndùng}=\dfrac{13,44}{22,4}=0,6\left(mol\right)\)
Ta có : Số mol Oxi/Oxit = n H2 dùng = 0,6 ( mol )
\(m_{\dfrac{O}{Oxit}}=0,6.16=9,6\left(g\right)\)
\(m_{\dfrac{M}{Oxit}}=32-9,6=22,4\left(g\right)\)
Gọi hóa trị M là n
PTHH :
\(2M+2nHCl\rightarrow2MCl_2+nH_2\uparrow\)
\(\dfrac{2}{n}.0,4\) 0,4
\(M_M=\dfrac{22,4}{\dfrac{2}{n}.0,4}=28.n\)
| n | 1 | 2 | 3 |
| M | 28 | 56 | 84 |
| Dk | (L) | T/M (Fe) | (L) |
Vậy kim loại M là Fe
\(\rightarrow\dfrac{n_{Fe}}{n_O}=\dfrac{\dfrac{22,4}{56}}{0,6}=\dfrac{2}{3}\)
Vậy CTPT của Oxit kim loại M là Fe2O3 .
Đúng 2
Bình luận (3)
Khử 3,48 gam một oxit của kim loại M cần dùng 1,344 lít
H
2
(đktc). Toàn bộ lượng kim loại M sinh ra cho tác dụng với dung dịch HCl dư thu được 1,008 lít H2 (đktc). Công thức oxit là A.
F
e
3
O
4
B.
F
e
2
O
3
C.
F
e
O
D.
Z...
Đọc tiếp
Khử 3,48 gam một oxit của kim loại M cần dùng 1,344 lít H 2 (đktc). Toàn bộ lượng kim loại M sinh ra cho tác dụng với dung dịch HCl dư thu được 1,008 lít H2 (đktc). Công thức oxit là
A. F e 3 O 4
B. F e 2 O 3
C. F e O
D. Z n O