định lượng phot pho trong mẫu phân bón , cân 1g mẫu và tạo tủa dưới dạng MgNH4PO4. nung tủa ở 600 độ C được dạng cân Mg2P2O7 có khối lượng 0,2350g. tính %P trong mẫu phân bón??
Cho 100ml dung dịch AlCl3 1M tác dụng với 200ml dung dịch NaOH. Kết tủa tạo thành được làm khô và nung đến khối lượng không đổi cân nặng 2,55g. Tính nồng độ dung dịch NaOH ban đầu.
A. 0,75 M
B. 1,75M
C. 1M
D. 1,25M
Đáp án B
Số mol AlCl3 là nAlCl3= 0,1.1 = 0,1 (mol)
Số mol Al2O3 là nAl2O3= 2,55/102 = 0,025 (mol)
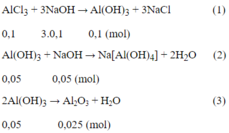
Theo pt (3) ta thấy số mol Al(OH)3 còn lại là 0,05 mol
Như vậy đã có: 0,1 - 0,05 = 0,05 mol Al(OH)3 đã bị hòa tan.
Từ (1) và (2) số mol NaOH = 3.0,1 + 0,05 = 0,35 (mol)
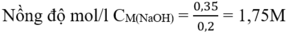
Tìm các phân số tối giản có mẫu khác 1, biết rằng tích của tử và mẫu bằng 3150 và phân số này có thể viết được dưới dạng số thập phân hữu hạn.
Gọi phân số tối giản phải tìm là a/b; (a; b ∈ Z; b ≠ 1), ƯCLN (a, b) = 1
Ta có a.b = 3150 = 2. 32. 52. 7 và a, b đều là ước của 3150.
Vì phân số này có thể viết được dưới dạng số thập phân hữu hạn nên b chỉ có ước nguyên tố là 2 và 5.
Do đó, b ∈ {2; 25; 50}.
- Với b = 2 thì a = 3150:2 = 1575
- Với b = 25 thì a = 3150:25 = 126
- Với b = 50 thì a = 3150:50 = 63
Vậy các phân số phải tìm là:
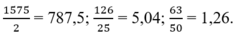
Tìm các phân số tối giản có mẫu khác 1 biết rằng tích của tử và mẫu bằng 3150 và phân số này có thể viết được dưới dạng số thập phân hữu hạn
Có bao nhiêu phân số có mẫu khác 1, biết tổng tử và mẫu của phân số đó bằng 18, và phân số đó viết được dưới dạng số thập phân vô hạn tuần hoàn. Có tất cả..... phân số
cho mình sửa đề bài. viết đc dưới dạng stp hữu hạn nha
Lấy 25ml dung dịch A gồm FeSO4 và Fe2(SO4)3 rồi chuẩn độ bằng dung dịch hỗn hợp KMnO4 0,025M thì hết 18,10ml. Mặt khác, thêm lượng dư dung dịch NH3 vào 25ml dung dịch A thì thu được kết tủa, lọc kết tủa rồi nung đỏ trong không khí ở nhiệt độ cao đến khối lượng không đổi, cân được 1,2g. Nồng độ mol/l của FeSO4 và Fe2(SO4)3 lần lượt là:
A. 0,091 và 0,25
B. 0,091 và 0,265
C. 0,091 và 0,255
D. 0,087 và 0,255
Lấy 25ml dung dịch A gồm FeSO4 và Fe2(SO4)3 rồi chuẩn độ bằng dung dịch hỗn hợp KMnO4 0,025M thì hết 18,10ml. Mặt khác, thêm lượng dư dung dịch NH3 vào 25ml dung dịch A thì thu được kết tủa, lọc kết tủa rồi nung đỏ trong không khí ở nhiệt độ cao đến khối lượng không đổi, cân được 1,2g. Nồng độ mol/l của FeSO4 và Fe2(SO4)3 lần lượt là:
A. 0,091 và 0,25
B. 0,091 và 0,265
C. 0,091 và 0,255
D. 0,087 và 0,255
Để định lượng Fe2+ trong mẫu phân tích người ta dùng phương pháp chuẩn độ đicromat dựa vào sơ đồ phản ứng sau:
Fe2+ + H+ + Cr2O72- → Fe3+ + Cr2+ + H2O
Hãy tính khối lượng Fe2+ trong dung dịch X biết đã dùng hết 30ml K2Cr2O7 0,1M.
A. 0,56
B. 0,112
C. 1,008
D. 1,56
Đáp án C
![]()
Phương trình phản ứng:
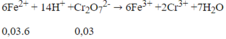
→ mFe = 0,03.6.56 = 1,008g
Một lò xo có độ cứng k đươc treo vào điểm cố định, đầu dưới treo vật có khối lượng m, tại nơi có gia tốc trọng trường g. Khi vật nằm cân bằng, độ biến dạng của lò xo là:
A. k m g
B. m g k
C. m k g
D. g m k
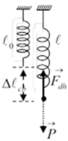
Khi cân bằng:
P → + F d h → = 0 → → F d h = P ↔ k Δ l = m g → Δ l = m g k
Đáp án: B
Một lò xo có độ cứng k được treo vào điểm cố định, đầu dưới treo vật có khối lượng m, tại nơi có gia tốc trọng trường g. Khi vật nằm cân bằng, độ biến dạng của lò xo là
A. k/ mg
B. mg/k
C. mk/g
D.g/mk
Chọn B.
Khi vật nằm cân bằng, trọng lực P → cân bằng với lực đàn hồi F đ h → . Do vậy ta có:
![]()