Cho 160g dung dịch sắt sunfat 0.5%(chưa rõ hóa trị) tác dụng với dung dịch BaCl2 vừa đủ. Sau pahn3 ứng thu được 1.398g chất kết tủa trắng và 350g dung dịch C
a-xác định muối đã dùng
b-tính nồng độ % của dung dịch thu được
Cho 160g dung dịch sắt sunfat 0.5%(chưa rõ hóa trị) tác dụng với dung dịch BaCl2 vừa đủ. Sau pahn3 ứng thu được 1.398g chất kết tủa trắng và 350g dung dịch C
a-xác định muối đã dùng
b-tính nồng độ % của dung dịch thu được
Cho 11,2 gam sắt tác dụng với 50ml dung dịch axít sunfuric thu được muối sắt (II) sunfat và khí hidro a) viết phương trình hóa học đã xảy ra b) tính khối lượng muối thu được sau phản ứng c) tính nồng độ mol của dung dịch h2so4 đã dùng
Sửa đề : 11.2 g sắt
\(n_{Fe}=\dfrac{11.2}{56}=0.2\left(mol\right)\)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
\(0.2....0.2.................0.2\)
\(m_{FeSO_4}=0.2\cdot152=30.4\left(g\right)\)
\(C_{M_{H_2SO_4}}=\dfrac{0.2}{0.05}=4\left(M\right)\)
\(m_{Fe}=\dfrac{11}{56}=0.19\left(mol\right)\)
\(Fe+H_2SO_4->FeSO_4+H_2\)
0.19 0.19 0.19 (mol)
\(m_{FeSO_4}=0.19\cdot152=28.28\left(g\right)\)
\(Cm=\dfrac{0.19}{0.05}=3.8M\)
PTHH:Fe+H2SO4→FeSO4+H2Fe+H2SO4→FeSO4+H2
TPT: 1 1 1 1 1 1 1 MOL
TĐ: 0,2 0,2 0,20 2 0,2 0,2 0,2 MOL
nFe=11.256=0.2(mol)
mFeSO4=0,2⋅152=30,4(g)
Cho 200 g dung dịch CuSO4 10% tác dụng vừa đủ với dung dịch BaCl2 5%. a. Tính khối lượng kết tủa thu được sau phản ứng? b. Tính khối lượng dung dịch BaCl2 cần dùng? c. Tính C% của muối trong dung dịch sau phản ứng?
Cho 8 gam sắt 3 oxit tác dụng vừa đủ với 100 gam dung dịch axit sunfuric a% Tính a Tính nồng độ phần trăm dung dịch muối sau phản ứng Cho dung dịch muối sau phản ứng tác dụng với dung dịch natri hiđroxit dư tính khối lượng kết tủa thu được
\(n_{Fe_2O_3}=\dfrac{8}{160}=0,05\left(mol\right)\)
PTHH: Fe2O3 + 3H2SO4 --> Fe2(SO4)3 + 3H2O
______0,05------>0,15--------->0,05
=> mH2SO4 = 0,15.98 = 14,7(g)
=> \(C\%\left(H_2SO_4\right)=\dfrac{14,7}{100}.100\%=14,7\%\)
\(C\%\left(Fe_2\left(SO_4\right)_3\right)=\dfrac{0,05.400}{8+100}.100\%=18,52\%\)
PTHH: Fe2(SO4)3 + 6NaOH --> 2Fe(OH)3\(\downarrow\) + 3Na2SO4
________0,05----------------------->0,1
=> mFe(OH)3 = 0,1.107=10,7(g)
Trộn 200 gam dung dịch một muối sunfat của kim loại kiềm nồng độ 13,2% với 200 gam dung dịch NaHCO3 4,2% sau phản ứng thu được m gam dung dịch A (m < 400 gam). Cho 200 gam dung dịch BaCl2 20,8% vào dung dịch A sau phản ứng còn dư muối sunfat. Thêm tiếp 40 gam dung dịch BaCl2 20,8%, dung dịch thu được còn dư BaCl2. Biết các phản ứng xảy ra hoàn toàn.
a) Xác định công thức muối sunfat của kim loại kiềm ban đầu.
b) Tính nồng độ % của các chất tan trong dung dịch A.
c) Dung dịch muối sunfat của kim loại kiềm ban đầu có thể tác dụng được với các chất nào sau đây: MgCO3, Ba(HSO3)2, Al2O3, Fe(OH)2, Ag, Fe, CuS, Fe(NO3)2? Viết phương trình hóa học của các phản ứng xảy ra.
a) Vì: mA < 400 (g) nên phải có khí thoát ra → muối có dạng MHSO4 và khí là: CO2
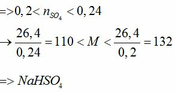
b)
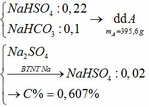
c) Tác dụng được với: MgCO3, Ba(HSO3)2, Al2O3, Fe(OH)2, Fe, Fe(NO3)2
Pt: 2NaHSO4 + MgCO3 → Na2SO4 + MgSO4 + CO2↑ + H2O
2NaHSO4 + Ba(HSO3)2 → BaSO4 + Na2SO4 + SO2↑ + 2H2O
6NaHSO4 + Al2O3 → 3Na2SO4 + Al2(SO4)3 + 3H2O
2NaHSO4 + Fe(OH)2 → Na2SO4 + FeSO4 + 2H2O
2NaHSO4 + Fe → Na2SO4 + FeSO4 + H2↑
12NaHSO4 + 9Fe(NO3)2 → 5Fe(NO3)3 + 2Fe2(SO4)3 + 6Na2SO4 + 3NO↑ + 6H2O
Cho 177,6g dd CaCl2 tác dụng vừa đủ dung dịch Na2CO3 16% thu được dung dịch A và kết tủa B . Lấy dd A cho tác dụng vừa đủ với dung dịch AgNO3 , thu dc dung dịch C và 57,4g kết tủa D.
a) Xác định A,B,C,D
b) Tính nồng độ % (C%) dung dịch A và khối lượng kết tủa B
PTHH: \(CaCl_2+Na_2CO_3\rightarrow2NaCl+CaCO_3\downarrow\)
\(NaCl+AgNO_3\rightarrow NaNO_3+AgCl\downarrow\)
A là dd NaCl
B là CaCO3
C là dd NaNO3
D là AgCl
Ta có: \(n_{AgCl}=\dfrac{57,4}{143,5}=0,4\left(mol\right)=n_{NaCl}\)
\(\Rightarrow n_{CaCO_3}=0,2\left(mol\right)=n_{Na_2CO_3}\) \(\Rightarrow\left\{{}\begin{matrix}m_{NaCl}=0,4\cdot58,5=23,4\left(g\right)\\m_{CaCO_3}=0,2\cdot100=20\left(g\right)\\m_{ddNa_2CO_3}=\dfrac{0,2\cdot106}{16\%}=132,5\left(g\right)\end{matrix}\right.\)
Mặt khác: \(m_{ddA}=m_{ddCaCl_2}+m_{ddNa_2CO_3}-m_{CaCO_3}=290,1\left(g\right)\)
\(\Rightarrow C\%_{NaCl}=\dfrac{23,4}{290,1}\cdot100\%\approx8,07\%\)
Cho dung dịch NaOH 10% tác dụng vừa đủ với 48,75 gam FeCl3 . a, Tính khối lượng kết tủa thu được. b, Tính khối lượng dd NaOH đã dùng. c, Tính nồng độ % các chất có trong dd sau phản ứng. d, xác định thể tích dung dịch H2SO4 20% có khối lượng riêng 1,14g/ml cần dùng để hòa tan hết lượng kết tủa thu được ở trên.
\(n_{FeCl_3}=\dfrac{48,75}{162,5}=0,3(mol)\\ 3NaOH+FeCl_3\to Fe(OH)_3\downarrow+3NaCl\\ \Rightarrow n_{Fe(OH)_3}=0,3(mol);n_{NaOH}=n_{NaCl}=0,9(mol)\\ a,m_{Fe(OH)_3}=0,3.107=32,1(g)\\ b,m_{dd_{NaOH}}=\dfrac{0,9.40}{10\%}=360(g)\\ c,C\%_{NaCl}=\dfrac{0,9.58,5}{360+48,75-32,1}.100\%=13,98\%\\ \)
\(d,2Fe(OH)_3+3H_2SO_4\to Fe_2(SO_4)_3+6H_2O\\ \Rightarrow n_{H_2SO_4}=0,45(mol)\\ \Rightarrow m_{dd_{H_2SO_4}}=\dfrac{0,45.98}{20\%}=220,5(g)\\ \Rightarrow V_{dd_{H_2SO_4}}=\dfrac{220,5}{1,14}=193,42(ml)\)
. Cho 5,6 lít khí CO2(đktc) tác dụng vừa đủ với 100ml dung dịch Ca(OH)2.( phản ứng chỉ thu được muối trung hòa và nước)
a/ Tính nồng độ mol của dung dịch Ca(OH)2 đã dùng?
b/ Tính khối lượng chất kết tủa thu được?
\(a.n_{CO_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\\ a.Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3+H_2O\\ 0,25.......0,25............0,25..........0,25\left(mol\right)\\ C_{MddCa\left(OH\right)_2}=\dfrac{0,25}{0,1}=2,5\left(M\right)\\ b.m_{\downarrow}=m_{CaCO_3}=100.0,25=25\left(g\right)\)
Bài 10: cho 200 gam dung dịch Na2CO3 10,6% tác dụng vừa đủ với 120 gam dung dịch Bacl2. sau khi phản úng kết thúc thu được dung dịch A
a) tính khối lượng kết tủa thu được ,b) tính C%của dung dịch Bacl2 đã dùng?
c)tính c% chất có trong dung dịch A
Bài 11: cho 250 gam dung dịch CuSO4 16% tác dụng vừa đủ với 120 gam dung dịch NaOH . sau khi phản ứng kết thúc thu được dung dịch A
a) tính C% của dung dịch NaOH đã dùng ; b)tính C% chất có trong dung dịch A
Bài 12:cho 150 gam dung dịch CuSO4 16% tác dụng với 224 gam dung dịch KOH 25% . sau khi phản ứng kết thúc thu được dung dịch A
a) tính khối lượng kết tủa thu được;
b)tính C% chất có trong dung dịch A
Bài 10:
PTHH: \(Na_2CO_3+BaCl_2\rightarrow2NaCl+BaCO_3\downarrow\)
a) Ta có: \(n_{Na_2CO_3}=\dfrac{200\cdot10,6\%}{106}=0,2\left(mol\right)=n_{BaCO_3}\)
\(\Rightarrow m_{BaCO_3}=0,2\cdot197=39,4\left(g\right)\)
b) Theo PTHH: \(n_{BaCl_2}=n_{BaCO_3}=0,2mol\)
\(\Rightarrow C\%_{BaCl_2}=\dfrac{0,2\cdot208}{120}\cdot100\%\approx34,67\%\)
c) Theo PTHH: \(n_{NaCl}=2n_{BaCl_2}=0,4mol\) \(\Rightarrow m_{NaCl}=0,4\cdot58,5=23,4\left(g\right)\)
Mặt khác: \(m_{dd}=m_{ddNa_2CO_3}+m_{ddBaCl_2}-m_{BaCO_3}=280,6\left(g\right)\)
\(\Rightarrow C\%_{NaCl}=\dfrac{23,4}{280,6}\cdot100\%\approx8,34\%\)