
Những câu hỏi liên quan
cho 15 gam một muối cacbonat của kim loại hóa trị II tác dụng với dung dịch HCl sau phản ứng thu được dung dịch muối nồng độ 3,33% trong đó còn có axit dư nồng độ 2,726% ngta thấy rằng tổng khối lượng của dung dịch sau phản ứng đã giảm đi 6,6 g. tìm CTHH của muối cacbonat và nồng độ % của dung dịch HCl
Xem chi tiết
Đặt CT của muối cacbonat là ACO3 MA = x (g)
PT: ACO3 + 2HCl ACl2 + CO2 + H2O
n ACO3 = (mol)
Khối lượng của dd giảm đi là do CO2 đã thoát ra khỏi dd.
⇒ m CO2 = 6,6g ⇒ m CO2 = 0,15 mol
Theo PT: n ACO3 = n CO2 ⇒ = 0,15 ⇔ x = 40.
Do đó A là kim loại Ca (vì MCa = 40g; Ca có hóa trị II)
PT: CaCO3 + 2HCl CaCl2 + CO2 + H2O
0,15 : 0,3 : 0,15 : 0,15 (mol)
m HCl pư = 10,95 (g)
m CaCl2 = 16,65g ⇒ m dd spứ= = 500 (g)
⇒ m HCl dư = = 13,63 (g)
Theo ĐLBTKL: mdd HCl bđ = mdd spư – m CaCO3 + m CO2 = 491,6 (g)
m HCl bđ = 10,95 + 13,63 = 24,58 (g)
⇒ C% dd HCl bđ = 5 %
Đúng 0
Bình luận (0)
Cho 8.4 gam 1 kin loại hóa trị 2 tác dụng với dung dịch h2s04 sau phản ứng thu được dung dịch muối có nồng độ 4.56% trong đó còn có axit dư nồng độ 2.726% người ta thấy rằng tổng khối lượng dung dịch sau phản ứng giảm 0.3 gam xác định tên kim loại và tính nồng độ phần trăm của dung dịch h2so4 đã dùng. @Giúp em
nR = nH2 = 0,15
=> MR = 8,4/0,15 = 56: R là Fe
nFeSO4 = nH2SO4 phản ứng = 0,15
=> mdd sau phản ứng = 0,15.152/4,56% = 500
=>mH2SO4 dư = 500.2,726% = 13,63
mddH2SO4 ban đầu = 500 + mH2 – mFe = 491,
C%H2SO4 ban đầu = (13,63 + 0,15.98)/491,9 = 5,76%
Cho a gam kim loại M hóa trị (II) tác dụng hết với dung dịch HCl có nồng độ C1%, được dung dịch A. Trung hòa vừa hết lượng axit dư trong A bằng 100 gam dung dịch Na2SO4 10,6%, phản ứng đó tạo nên dung dịch B trong đó NaCl có nồng độ 3,844% và muối clorua của M có nồng độ là 12,484%. Tiếp đó cho B tác dụng với lượng dư dung dịch NaOH thu được kết tủa. Lọc rửa kết tủa, nung kết tủa ở nhiệt độ cao đến khi thu được chất rắn có khối lượng không đổi, cân được 16 gam.a) Viết các phương trình phản ứng x...
Đọc tiếp
Cho a gam kim loại M hóa trị (II) tác dụng hết với dung dịch HCl có nồng độ C1%, được dung dịch A. Trung hòa vừa hết lượng axit dư trong A bằng 100 gam dung dịch Na2SO4 10,6%, phản ứng đó tạo nên dung dịch B trong đó NaCl có nồng độ 3,844% và muối clorua của M có nồng độ là 12,484%. Tiếp đó cho B tác dụng với lượng dư dung dịch NaOH thu được kết tủa. Lọc rửa kết tủa, nung kết tủa ở nhiệt độ cao đến khi thu được chất rắn có khối lượng không đổi, cân được 16 gam.
a) Viết các phương trình phản ứng xảy ra; xác định kim loại M và khối lượng a. b) Tính nồng độ C% của dung dịch HCl.
Cho 3,64 gam hỗn hợp E gồm một oxit, một hiđroxit và một muối cacbonat trung hòa của một kim loại M có hóa trị II tác dụng vừa đủ với 117,6 gam dung dịch H2SO4 10%. Sau phản ứng, thu được 0,448 lít khí (đktc) và dung dịch muối duy nhất có nồng độ 10,867% (khối lượng riêng là 1,093 gam/ml); nồng độ mol là 0,545M. a) Viết các phương trình phản ứng xảy ra và xác định kim loại M. b) Tính % khối lượng của các chất có trong hỗn hợp E.
Đọc tiếp
Cho 3,64 gam hỗn hợp E gồm một oxit, một hiđroxit và một muối cacbonat trung hòa của một kim loại M có hóa trị II tác dụng vừa đủ với 117,6 gam dung dịch H2SO4 10%. Sau phản ứng, thu được 0,448 lít khí (đktc) và dung dịch muối duy nhất có nồng độ 10,867% (khối lượng riêng là 1,093 gam/ml); nồng độ mol là 0,545M.
a) Viết các phương trình phản ứng xảy ra và xác định kim loại M.
b) Tính % khối lượng của các chất có trong hỗn hợp E.
a) Đặt số mol của MO, M(OH)2, MCO3 tương ứng là x, y, z.
Nếu tạo muối trung hòa ta có các phản ứng:
MO + H2SO4 →MSO4 + H2O (1)
M(OH)2 + H2SO4 →MSO4 + 2H2O (2)
MCO3 + H2SO4 →MSO4 + H2O + CO2 (3)
Nếu tạo muối axít ta có các phản ứng:
MO + 2H2SO4 →M(HSO4)2 + H2O (4)
M(OH)2 + 2H2SO4 →M(HSO4)2 + 2H2O (5)
MCO3 + 2H2SO4 →M(HSO4)2 + H2O + CO2 (6)
Ta có :
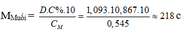
– TH1: Nếu muối là MSO4 M + 96 = 218 M = 122 (loại)
– TH2: Nếu là muối M(HSO4)2 M + 97.2 = 218 M = 24 (Mg)
Vậy xảy ra phản ứng (4, 5, 6) tạo muối Mg(HSO4)2
b) Theo (4, 5, 6) Số mol CO2 = 0,448/22,4 = 0,02 molz = 0,02 (I)
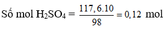
2x + 2y + 2z = 0,12 (II)
Đề bài: 40x + 58y + 84z = 3,64 (III)
Giải hệ (I, II, III): x = 0,02; y = 0,02; z = 0,02
%MgO = 40.0,02.100/3,64 = 21,98%
%Mg(OH)2 = 58.0,02.100/3,64 = 31,87%
%MgCO3 = 84.0,02.100/3,64 = 46,15%
Đúng 0
Bình luận (0)
Cho 12,4 gam muối cacbonat của một kim loại hóa trị II tác dụng hoàn toàn với dung dịch H2SO4 loãng thu được 16 gam muối sunfat.
a. Tìm công thức của muối cacbonat đó.
b. Nếu lượng axit H2SO4 dùng với lượng vừa đủ và có nồng độ C% là 9,8%. Xác định nồng độ của muối sunfat thu được sau phản ứng.
a)
$RCO_3 + H_2SO_4 \to RSO_4 + CO_2 + H_2O$
Theo PTHH :
$n_{RCO_3} = n_{RSO_4}$
Suy ra : \(\dfrac{12,4}{R+60}=\dfrac{16}{R+96}\)
Suy ra : R = 64(Cu)
Vậy muối là $CuCO_3$
b)
$n_{CO_2} = n_{H_2SO_4} = n_{CuSO_4} = 16 : 160 = 0,1(mol)$
$m_{dd\ H_2SO_4} = \dfrac{0,1.98}{9,8\%} = 100(gam)$
$m_{dd\ sau\ pư} = 12,4 + 100 -0,1.44 = 108(gam)$
$C\%_{CuSO_4} = \dfrac{16}{108}.100\% = 14,81\%$
Đúng 0
Bình luận (1)
Trộn 200 gam dung dịch một muối sunfat của kim loại kiềm nồng độ 13,2% với 200 gam dung dịch NaHCO3 4,2% sau phản ứng thu được m gam dung dịch A (m 400 gam). Cho 200 gam dung dịch BaCl2 20,8% vào dung dịch A sau phản ứng còn dư muối sunfat. Thêm tiếp 40 gam dung dịch BaCl2 20,8%, dung dịch thu được còn dư BaCl2. Biết các phản ứng xảy ra hoàn toàn. a) Xác định công thức muối sunfat của kim loại kiềm ban đầu. b) Tính nồng độ % của các chất tan trong dung dịch A. c) Dung dịch muối sunfat của kim l...
Đọc tiếp
Trộn 200 gam dung dịch một muối sunfat của kim loại kiềm nồng độ 13,2% với 200 gam dung dịch NaHCO3 4,2% sau phản ứng thu được m gam dung dịch A (m < 400 gam). Cho 200 gam dung dịch BaCl2 20,8% vào dung dịch A sau phản ứng còn dư muối sunfat. Thêm tiếp 40 gam dung dịch BaCl2 20,8%, dung dịch thu được còn dư BaCl2. Biết các phản ứng xảy ra hoàn toàn.
a) Xác định công thức muối sunfat của kim loại kiềm ban đầu.
b) Tính nồng độ % của các chất tan trong dung dịch A.
c) Dung dịch muối sunfat của kim loại kiềm ban đầu có thể tác dụng được với các chất nào sau đây: MgCO3, Ba(HSO3)2, Al2O3, Fe(OH)2, Ag, Fe, CuS, Fe(NO3)2? Viết phương trình hóa học của các phản ứng xảy ra.
a) Vì: mA < 400 (g) nên phải có khí thoát ra → muối có dạng MHSO4 và khí là: CO2
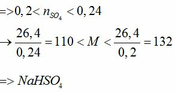
b)
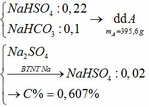
c) Tác dụng được với: MgCO3, Ba(HSO3)2, Al2O3, Fe(OH)2, Fe, Fe(NO3)2
Pt: 2NaHSO4 + MgCO3 → Na2SO4 + MgSO4 + CO2↑ + H2O
2NaHSO4 + Ba(HSO3)2 → BaSO4 + Na2SO4 + SO2↑ + 2H2O
6NaHSO4 + Al2O3 → 3Na2SO4 + Al2(SO4)3 + 3H2O
2NaHSO4 + Fe(OH)2 → Na2SO4 + FeSO4 + 2H2O
2NaHSO4 + Fe → Na2SO4 + FeSO4 + H2↑
12NaHSO4 + 9Fe(NO3)2 → 5Fe(NO3)3 + 2Fe2(SO4)3 + 6Na2SO4 + 3NO↑ + 6H2O
Đúng 0
Bình luận (0)
cho M gam kim loại R có hóa trị II tác dụng với Clo dư,sau phản ứng thu được 13,6 gam muối,mặt khác,để hòa tan M gam kim loại R cần vừa đủ 200ml dung dịch HCL có nồng độ 1M
a, viết pthh
b,xác định kim loại R
giúp mình với ạ
R + Cl2 → RCl2
R + 2HCl → RCl2 + H2
nHCl = 0,2.1 = 0,2 mol => nR = 0,2/2 = 0,1 mol
Mà nRCl2 = nR
=> MRCl2 = \(\dfrac{13,6}{0,1}\)= 136 (g/mol) => MR = 136 - 35,5.2 = 64 g/mol
Vậy R là kim loại đồng (Cu)
Đúng 2
Bình luận (0)
Hòa tan 14,4 gam kim loại R hóa trị II trong dung dịch HCl 29,2%. Sau khi phản ứng hoàn toàn thu được dung dịch mới có nồng độ HCl 5,456% và nồng độ muối clorua là 28,401%. Xác định kim loại R.
a)cho 9,75 gam kim loại x hóa trị 2 tác dụng với dung dịch HCl dư thu được dung dịch A có 3,36 lít khí thoát ra
b) nếu dùng 200 ml dung dịch HCl 2n cho phản ứng trên tính khối lượng muối và nồng độ các chất tan trong dung dịch A
\(a,PTHH:X+2HCl\to XCl_2+H_2\\ \Rightarrow n_{X}=n_{H_2}=\dfrac{3,36}{22,4}=0,15(mol)\\ \Rightarrow M_X=\dfrac{9,75}{0,15}=65(g/mol)(Zn)\\ b,n_{HCl}=2.0,2=0,4(mol)\)
Vì \(\dfrac{n_{H_2}}{1}<\dfrac{n_{HCl}}{2}\) nên \(HCl\) dư
\(\Rightarrow n_{ZnCl_2}=n_{H_2}=0,15(mol)\\ \Rightarrow m_{ZnCl_2}=136.0,15=20,4(g)\\ C_{M_{ZnCl_2}}=\dfrac{0,15}{0,2}=0,75M\)
Đúng 2
Bình luận (1)



















