Trộn đều 2g MnO2 và 98g hỗn hợp X gồm KClO3 và KCl rồi đun nóng đến khi phản ứng xảy ra hoàn toàn thì thu được chất rắn cân nặng 76g. Xác định khối lượng mỗi muối trong hỗn hợp X.

Những câu hỏi liên quan
Thêm 3,0 gam MnO2 vào 200gam hỗn hợp X gồm KCl và KClO3, trộn kĩ hỗn hợp thu được và đun nóng đến phản ứng xảy ra hoàn toàn (khối lượng hỗn hợp không đổi) thu được chất rắn Y cân nặng 145,4gam. Xác định thành phần phần trăm theo khối lượng của các muối trong hỗn hợp X
mgiảm = mO2 (sinh ra) = 200 + 3 - 145,4 = 57,6 (g)
\(\rightarrow n_{O_2}=\dfrac{57,6}{32}=1,8\left(mol\right)\)
PTHH: 2KClO3 --to, MnO2--> 2KCl + 3O2
1,2 1,8
\(\rightarrow m_{KClO_3}=1,2.122,5=147\left(g\right)\\ \rightarrow\left\{{}\begin{matrix}\%m_{KClO_3}=\dfrac{147}{200}=73,5\%\\\%m_{KCl}=100\%-73,5\%=26,5\%\end{matrix}\right.\)
Đúng 6
Bình luận (0)
Khối lượng oxi thoát ra: 197 + 3 – 152 = 48(g)
Số mol O2=4832=1,5(mol)O2=4832=1,5(mol)
Phương trình hóa học của phản ứng :
2KClO3MnO2,to⟶2KCl+3O22KClO3⟶MnO2,to2KCl+3O2
2 mol 3 mol
1,5×23=1mol1,5×23=1mol ←← 1,5 mol
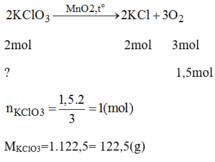
Khối lượng KClO3KClO3 trong hỗn hợp : 1 x 122,5 =122,5 (g)Khối lượng KCl trong hỗn hợp ban đầu: 197 – 122,5 = 74,5(g)→%mKClO3=62,18%;%mKCl=37,82%→%mKClO3=62,18%;%mKCl=37,82%
Trộn đều 2g MnO2 và 98g hỗn hợp KCl và KClO3 rồi đem đun nóng đến khi phản ứng xảy ra hoàn toàn thì thu được hỗn hợp chất rắn nặng 76g. Xác định khối lượng muối trong hỗn hợp ban đầu.
Sau phản ứng thu được: \(76-2=74gKCl\)
\(\Rightarrow n_{KCls.p.ứ}=\frac{74}{74,5}=1mol\)
Gọi \(x\) là mol \(KCl;y\) là mol \(KClO_3\) ban đầu.
\(\Rightarrow74,5x+122,5y=98\left(1\right)\)
\(PTHH:2KClO_3\overset{t^0}{\rightarrow}2KCl+3O_2\)
\(\Rightarrow n_{KCl.nung}=y\)
\(\Rightarrow x+y=1\left(2\right)\)
\(\left(1\right)\left(2\right)\Rightarrow x=y=0,5\)
\(m_{KCl}=0,5.74,5=37,25g\)
\(m_{KClO_3}=0,5.122,5=61,25g\)
Thêm 3,0g M n O 2 vào 197g hỗn hợp muối KCl và K C l O 3 . Trộn kĩ và đun nóng hỗn hợp đến phản ứng hoàn toàn, thu được chất rắn nặng 152g. Hãy xác định thành phần phần trăm khối lượng của các chất trong hỗn hợp muối đã dùng.
Khối lượng oxi thoát ra: m O 2 = 197 + 3 – 152 = 48(g)
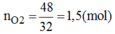
PTHH của phản ứng:
Khối lượng của KCl trong hỗn hợp ban đầu:
m K C l = 197-122,5 = 74,5(g)
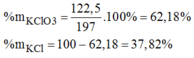
Đúng 0
Bình luận (0)
Thêm 3 gam MnO 2 vào 197 gam hỗn hợp X gồm KCl và KClO 3 . Trộn kĩ và đun hỗn hợp đến phản ứng hoàn toàn, thu được chất rắn cân nặng 152 gam. Khối lượng KCl trong 197 gam X là
A. 74,50 gam
B. 13,75 gam
C. 122,50 gam
D. 37,25 gam
Thêm 3 gam MnO2 vào 197 gam hỗn hợp X gồm KCl và KClO3. Trộn kĩ và đun hỗn hợp đến phản ứng hoàn toàn, thu được chất rắn cân nặng 152 gam. Khối lượng KCl trong 197 gam X là: A. 74,50 gam. B. 13,75 gam. C. 122,50 gam. D. 37,25 gam.
Đọc tiếp
Thêm 3 gam MnO2 vào 197 gam hỗn hợp X gồm KCl và KClO3. Trộn kĩ và đun hỗn hợp đến phản ứng hoàn toàn, thu được chất rắn cân nặng 152 gam. Khối lượng KCl trong 197 gam X là:
A. 74,50 gam.
B. 13,75 gam.
C. 122,50 gam.
D. 37,25 gam.
Đáp án A.
Bảo toàn khối lượng: mO2 = 3 + 197 – 152 = 48 (gam)
nO2 = 1,5 (mol)
2KClO3 → 2KCl + 3O2 ↑
⇒ mKCl = 197 – 1.122,5 = 74,5 (gam)
Đúng 0
Bình luận (0)
Thêm 3g MgO2 vào hỗn hợp KCl và KClO3 trộn kĩ và đun nóng đến phản ứng hoàn toàn thu được chất rắn cân nặng 152g yêu cầu tính % khối lượng các chất trong hỗn hợp đầu.
Gíup mik với mai mik kt rồi
Thêm 3,5 gam MnO2 vào 197 gam hỗn hợp muối KCl và KClO3. Trộn kĩ và đun nóng hỗn hợp đến phản ứng hoàn toàn, thu được chất rắn nặng 152,5 gam. Tính thành phần phần trăm theo số mol của hỗn hợp muối đã dùng: A. 62,18% KClO3 và 37,82% KCl B. 37,82% KClO3 và 62,18% KCl C. 50% KClO3 và 50% KCl D. 30% KClO3 và 70% KCl
Đọc tiếp
Thêm 3,5 gam MnO2 vào 197 gam hỗn hợp muối KCl và KClO3. Trộn kĩ và đun nóng hỗn hợp đến phản ứng hoàn toàn, thu được chất rắn nặng 152,5 gam. Tính thành phần phần trăm theo số mol của hỗn hợp muối đã dùng:
A. 62,18% KClO3 và 37,82% KCl
B. 37,82% KClO3 và 62,18% KCl
C. 50% KClO3 và 50% KCl
D. 30% KClO3 và 70% KCl
Đáp án C
MnO2 là chất xúc tác nên sử dụng định luật bảo toàn khối lượng ta được:
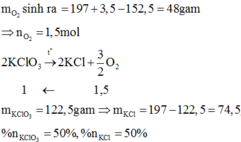
Đúng 0
Bình luận (0)
Hỗn hợp X gồm a mol KClO3 và b mol Cu. Nung nóng hỗn hợp X đến khi các phản ứng xảy ra hoàn toàn thì thấy khối lượng hỗn hợp chất rắn Y thu được bằng khối lượng hỗn hợp X. Xác định mối liên hệ của a và b.
Do khối lượng chất rắn trong X và Y bằng nhau
=> Lượng O2 sinh ra khi phân hủy KClO3 phản ứng hết với Cu
PTHH: 2KClO3 --to--> 2KCl + 3O2
a--------------->1,5a
2Cu + O2 --to--> 2CuO
3a<--1,5a
=> b \(\ge\) 3a
Đúng 7
Bình luận (0)
Tiến hành thí nghiệm sau: – Thí nghiệm 1: cho 1,74 gam MnO2 tác dụng với HCl đặc, dư, đun nóng thu được khí A màu vàng lục. – Thí nghiệm 2: cho một lượng sắt vào dung dịch H2SO4 loãng đến khi khối lượng dung dịch tăng 167,4 gam thì thu được một lượng khí B. – Thí nghiệm 3: thêm 3 gam MnO2 vào 197 gam hỗn hợp KCl và KClO3 thu được hỗn hợp X. Trộn kĩ và đun nóng hỗn hợp X đến khi phản ứng xảy ra hoàn toàn thì thu được chất rắn nặng 152 gam và một lượng khí D. – Thí nghiệm 4: Nạp toàn bộ lượng khí...
Đọc tiếp
Tiến hành thí nghiệm sau:
– Thí nghiệm 1: cho 1,74 gam MnO2 tác dụng với HCl đặc, dư, đun nóng thu được khí A màu vàng lục.
– Thí nghiệm 2: cho một lượng sắt vào dung dịch H2SO4 loãng đến khi khối lượng dung dịch tăng 167,4 gam thì thu được một lượng khí B.
– Thí nghiệm 3: thêm 3 gam MnO2 vào 197 gam hỗn hợp KCl và KClO3 thu được hỗn hợp X. Trộn kĩ và đun nóng hỗn hợp X đến khi phản ứng xảy ra hoàn toàn thì thu được chất rắn nặng 152 gam và một lượng khí D.
– Thí nghiệm 4: Nạp toàn bộ lượng khí A, khí B và khí D thu được ở các thí nghiệm trên vào một bình kín, nâng nhiệt độ cao để thực hiện hoàn toàn các phản ứng rồi đưa nhiệt độ về 250C thu được dung dịch Y chỉ chứa một chất tan duy nhất.
Viết các phương trình hóa học xảy ra và tính nồng độ % của chất tan có trong dung dịch Y
















