Một hỗn hợp gồm đường saccarozơ (C12H22O11) và muối ăn (NaCl) có tổng khối lượng là 129,375 g. Biết trong hỗn hợp số mol NaCl gấp 3 lần số mol C12H22O11. Hãy xác định số mol mỗi chất trong hỗn hợp

Những câu hỏi liên quan
Hãy tính:
a/ Số mol của 85,2g Al(NO3)3
b/ Thể tích của 0,015 mol khí NO2, ở điều kiện chuẩn
c/ Khối lượng của một hỗn hợp gồm 0,5 mol C12H22O11 và 0,6 mol C6H12O6
$\rm a) n_{Al(NO_3)_3} = \dfrac{m}{M} = \dfrac{85,2}{213} = 0,4 (mol)$
$\rm b) V_{NO_2(đkc)} = n.24,79 = 0,015.24,79 = 0,37185(l)$
$\rm c)m_{C_{12}H_{22}O_{11}} = n.M = 0,5.342 = 171 (g)$
$\rm d)m_{C_6H_{12}O_6} = n.M = 0,6.180 = 108(g)$
$\rm \Rightarrow m_{hh} = m_{C_{12}H_{22}O_{11}} + m_{C_6H_{12}O_6} = 171 + 108 = 279 (g)$
Đúng 0
Bình luận (0)
Hỗn hợp M gồm RCl2 và R(NO3)2, có khối lượng bằng 32,82 gam, trong đó tổng số mol 2 chất bằng 0,2 mol. Trong M, số mol oxygen gấp 7 lần số mol nitrogen. Xác định tên kim loại R.
Đọc tiếp
Hỗn hợp M gồm RCl2 và R(NO3)2, có khối lượng bằng 32,82 gam, trong đó tổng số mol 2 chất bằng 0,2 mol. Trong M, số mol oxygen gấp 7 lần số mol nitrogen. Xác định tên kim loại R.
Một hỗn hợp gồm CuSO4 và Fe2(SO4)3, trong đó % khối lượng S là 22,61%.
a/ Tính % khối lượng O trong hỗn hợp.
b/ Biết số mol Fe trong hỗn hợp là 18.1024.
- Tính số mol từng chất trong hỗn hợp.
- Tính khối lượng hỗn hợp.
Một hỗn hợp gồm CuSO4 và Fe2(SO4)3, trong đó % khối lượng S là 22,61%.
a/ Tính % khối lượng O trong hỗn hợp.
b/ Biết số mol Fe trong hỗn hợp là 18.1024.
- Tính số mol từng chất trong hỗn hợp.
- Tính khối lượng hỗn hợp.
Hỗn hợp A gồm 2 oxit là Fe2O3 và CuO, trong đó số mol CuO gấp 3 lần số mol Fe2O3.
Tính % khối lượng mỗi oxit trong hỗn hợp A.
Gọi \(n_{Fe_2O_3}=a\left(mol\right)\Rightarrow n_{CuO}=3a\left(mol\right)\)
Ta có: \(m_{hh}=160a+80.3a=400a\left(g\right)\)
\(\%m_{Fe_2O_3}=\dfrac{160a.100\%}{400a}=40\%\)
\(\%m_{CuO}=100-40=60\%\)
Đúng 2
Bình luận (0)
Hỗn hợp M chứa ancol no A và axit cacboxylic đơn chức B, cả hai đều mạch hở. Tổng số mol 2 chất trong hỗn hợp M là 0,5 mol. Để đốt cháy hoàn toàn hỗn hợp M cần dùng vừa hết 30,24 lít
O
2
. Sản phẩm cháy gồm có 23,4 g H2O và 26,88 lít
C
O
2
. Các thể tích đo ở đktc.Hãy xác định công thức phân tử, công thức cấu tạo, tên gọi và phần trăm khối lượng từng chất trong hỗn hợp M, biết rằng chất B hơn chất A m...
Đọc tiếp
Hỗn hợp M chứa ancol no A và axit cacboxylic đơn chức B, cả hai đều mạch hở. Tổng số mol 2 chất trong hỗn hợp M là 0,5 mol. Để đốt cháy hoàn toàn hỗn hợp M cần dùng vừa hết 30,24 lít O 2 . Sản phẩm cháy gồm có 23,4 g H2O và 26,88 lít C O 2 . Các thể tích đo ở đktc.
Hãy xác định công thức phân tử, công thức cấu tạo, tên gọi và phần trăm khối lượng từng chất trong hỗn hợp M, biết rằng chất B hơn chất A một nguyên tử cacbon.
Khi đốt 0,5 mol hỗn hơp M, số mol C O 2 thu đươc là :
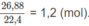
Nếu đốt 1 mol hỗn hợp M, số mol C O 2 thu được sẽ là 2,4 (mol).
Như vậy chất A và chất B có chứa trung bình 2,40 nguyên tử cacbon , chất A lại kém chất B 1 nguyên tử cacbon. Vậy, A có 2 và B có 3 nguyên tử cacbon.
A là ancol no có 2 cacbon: C 2 H 6 - x ( O H ) x hay C 2 H 6 O x
B là axit đơn chức có 3 cacbon: C 3 H y O 2 .
Đặt số mol A là a, số mol B là b :
a + b = 0,5 (1)
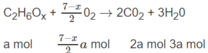
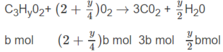
Số mol O 2 là: (3,5 - 0,5x)a + (2 + 0,25y)b = 1,35 (mol) (2)
Số mol C O 2 là: 2a + 3b = 1,2 (mol) (3)
Số mol C O 2 là:
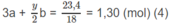
Giải hệ phương trình đại số tìm được: a = 0,3; b = 0,2; x = 2; y = 4.
Chất A:
C
2
H
6
O
2
hay 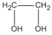 etanđiol (hay etylenglicol)
etanđiol (hay etylenglicol)
Chiếm  khối lượng M.
khối lượng M.
Chất B: C 3 H 4 O 2 hay C H 2 = C H - C O O H , axit propenoic chiếm 43,64% khối lượng M.
Đúng 0
Bình luận (0)
Một hỗn hợp X gồm etanol (C2H6O) và glixerol (C3H8O3) có tỉ lệ khối lượng tương ứng là 1 : 4.
a) Tính số mol của mỗi chất có trong 103,5 g hỗn hợp X.
b) Đem hòa tan 34,5 g hỗn hợp X vào cốc nước thì được 58,8 g dung dịch lỏng. Tính số mol mỗi chất (C2H6O, C3H8O3, H2O) có trong cốc
Cho 13 g hỗn hợp A gồm Fe, Mg, Zn phản ứng với 1,2 mol HCl
a.Chứng tỏ rằng A tan hết
b. Nếu tổng số mol của 3 kim loại trong 13 g hỗn hợp A là 0,3 mol, tỉ lệ số mol giữa Fe và Mg là 1:1. Tính khối lượng mỗi kim loại trong hỗn hợp A
hòa tan hết hỗn hợp kim loại gồm : Al , Mg , Fe trong dung dịch HCl thaayssinh ra 49,28 lí khí H2 (đktc) . cho biết trong hỗn hợp số mol Fe chỉ bằng 2/3 số mol Mg và bằng một nửa số mol Al . hãy xác định khối lượng của mỗi kim loại có trong hỗn hợp và thành phần phần trăm về khối lương của mỗi kim loại
các anh , chi giỏi hóa giúp e với
Mg ko pư vs HCl
Gọi số mol của Fe là a(a>0)
=> nAl= 2a(mol)
nMg = 3/2 a (mol)
nH2=49,28/22,4=2,2(mol)
PTHH
Fe + 2HCl ------> FeCl2 + H2
a a (mol)
2Al + 6HCl ------> 2AlCl3 + 3H2
2a 3a (mol)
=> nH2 = a+3a=4a=2,2(mol)
=> a=0,55 = nFe
=> nAl = 2a = 1,1 ( mol)
nMg = 0,825 ( mol)
%mFe = ( 0,55.56)/(0,55.56 + 1,1.27 + 0,825.24) . 100% = 38,35 %
%mAl =(1,1.27)/(0,55.56 + 1,1.27 + 0,825.24) . 100% = 37%
%mMg = 100% - %mFe - %mAl = 100% -38,36%-37% = 24,65%
( kết quả có thể khác , bn tự lm lại theo hướng này )
#Học-tốt
















