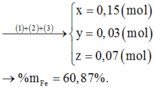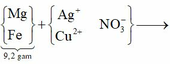cho 19,73g hỗn hợp 3 kim loại Mg,Al, và Cu. Đung nóng hỗn hợp trong không khí dư oxi để phản ứng xảy ra hoàn toàn thu được 28,45g chất rắn . Hỏi để hòa tan hết lượng chất rắn đó cần dùng ít nhất bao nhiêu ml dug dịch HCl 5M

Những câu hỏi liên quan
Nung nóng 16,8 gam hỗn hợp gồm Mg, Cu, Al với một lượng dư khí O2, đến khi các phản ứng xảy ra hoàn toàn, thu được 23,2 gam chất rắn X (MgO, CuO, Al2O3). Tính thể tích dung dịch HCl 2M vừa đủ để hòa tan hết chất rắn X ?
$2Mg + O_2 \xrightarrow{t^o} 2MgO$
$2Cu + O_2 \xrightarrow{t^o} 2CuO$
$4Al + 3O_2 \xrightarrow{t^o} 2Al_2O_3$
$MgO + 2HCl \to MgCl_2 + H_2O$
$CuO + 2HCl \to CuCl_2 + H_2O$
$Al_2O_3 + 6HCl \to 2AlCl_3 + 3H_2O$
Gọi $n_{MgO} = a(mol) ; n_{CuO} = b(mol) ; n_{Al_2O_3} = c(mol)$
Bảo toàn khối lượng : $m_{O_2} = 23,2 - 16,8 = 6,4(gam)$
$n_{O_2} = 0,2(mol)$
$\Rightarrow 0,5a + 0,5b + 1,5c = 0,2(1)$
Theo PTHH :
$n_{HCl} =2 n_{MgO} + 2n_{CuO} + 6n_{Al_2O_3} = 0,8(theo (1))$
Suy ra : $V_{dd\ HCl} = \dfrac{0,8}{2} = 0,4(lít)$
Đúng 1
Bình luận (0)
Cho 21,3 gam hỗn hợp X gồm 3 kim loại Mg, Cu và Al tác dụng hoàn toàn với oxi dư (có đun nóng) , thu được hỗn hợp chất rắn B có khối lượng 33,3 gam. Để hoà tan hoàn toàn B ta phải cần dùng tối thiểu bao nhiêu ml dung dịch hỗn hợp HCl 2M và H2SO4 1M?
\(n_O=\dfrac{33,3-21,3}{16}=0,75\left(mol\right)\)
=> nH2O = 0,75 (mol)
Giả sử có V lít dd
=> \(\left\{{}\begin{matrix}n_{H_2SO_4}=V\left(mol\right)\\n_{HCl}=2V\left(mol\right)\end{matrix}\right.\)
Bảo toàn H: 2V + 2V = 0,75.2
=> V = 0,375 (lít) = 375 (ml)
Đúng 1
Bình luận (0)
Cho m gam hỗn hợp gồm Fe và Al ở dạng bột vào 200ml dd CuSO4 0,525M. Khuấy kỹ hỗn hợp để các phản ứng hóa học xảy ra hoàn toàn. Sau phản ứng thu được 7,84g chất rắn A gồm 2 kim loại và dung dịch B. Để hòa tan hoàn toàn chất rắn A cần dùng ít nhất bao nhiêu ml dd HNO3 2M, biết rằng phản ứng sinh ra sản phẩm khử duy nhất là NO? A. 211,12 ml B. 221,13 ml C. 166,67 ml D. 233,33 ml
Đọc tiếp
Cho m gam hỗn hợp gồm Fe và Al ở dạng bột vào 200ml dd CuSO4 0,525M. Khuấy kỹ hỗn hợp để các phản ứng hóa học xảy ra hoàn toàn. Sau phản ứng thu được 7,84g chất rắn A gồm 2 kim loại và dung dịch B. Để hòa tan hoàn toàn chất rắn A cần dùng ít nhất bao nhiêu ml dd HNO3 2M, biết rằng phản ứng sinh ra sản phẩm khử duy nhất là NO?
A. 211,12 ml
B. 221,13 ml
C. 166,67 ml
D. 233,33 ml
Đáp án C.
Chất rắn sau phản ứng gồm 2 kim loại → 2 kim loại đó là Cu và Fe , Al đã phản ứng hết → CuSO4 không dư → nCu = 0,105 mol => m= 6,72 gam → còn 1,12 gam là của Fe .
Phản ứng : Fe + 4HNO3 → Fe(NO3)3 + NO +2H2O
nFe = 0,02 mol → nHNO3= 0,08 mol .
n F e 3 + = 0,02 mol
chú ý phản ứng: Cu + 2Fe3+ → Cu2+ + 2Fe2+
⇒ 0,01 mol Cu + 0,02 mol Fe3+ → 0,01 mol Cu2+ và 0,02 mol Fe2+ )
Để HNO3 cần dùng là tối thiểu thì cần dùng 1 lượng hòa tan vừa đủ 0,105 – 0,01 = 0,095 mol Cu
3Cu + 8HNO3 → 3Cu(NO3)2 + 2NO + 4H2O
Từ đây tính được nHNO3= 0,095. 8 3 = 0,253 mol
→ tổng nHNO3 đã dùng là 0,253 + 0,08 = 0,333 mol
→ = 0,16667 lít = 166,67 ml
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 4,44g hỗn hợp Al và Fe trong khí oxi. Sau phản ứng kết thúc thu được chất rắn A. Cho dòng khí H2 dư đi qua A nung nóng cho tới khi các phản ứng xảy ra hoàn toàn thu được 5,4g chất rắn B. Tính khối lượng mỗi kim loại có trong hỗn hợp ban đầu.
Gọi $n_{Al}= a(mol) ; n_{Fe} = b(mol) \Rightarrow 27a + 56b = 4,44(1)$
$4Al + 3O_2 \xrightarrow{t^o} 2Al_2O_3$
$3Fe + 2O_2 \xrightarrow{t^o} Fe_3O_4$
$Fe_3O_4 + 4H_2 \xrightarrow{t^o} 3Fe + 4H_2O$
B gồm : $Al_2O_3, Fe$
$n_{Al_2O_3} = \dfrac{1}{2}n_{Al} = 0,5a(mol)$
Suy ra: $0,5a.102 + 56b = 5,4(2)$
Từ (1)(2) suy ra a = 0,04 ; b = 0,06
$m_{Al} = 0,04.27 =1,08\ gam$
$m_{Fe} = 0,06.56 = 3,36\ gam$
Đúng 3
Bình luận (0)
Hòa tan 16,55g hỗn hợp B gồm Al, Fe và Cu trong dung dịch HCl dư đến khi phản ứng xảy ra hoàn toàn thu được 9,6g chất rắn và 3,92 lít khí hidro (đktc) a. Tính khối lượng từng kim loại trong hỗn hợp b. Tính khối lượng HCl đã dùng
\(a) m_{Cu} = 9,6(gam)\\ n_{Al} = a(mol) ; n_{Fe} = b(mol)\\ \Rightarrow 27a + 56b = 16,55 -9,6 =6,95(1)\\ 2Al + 6HCl \to 2AlCl_3 + 3H_2\\ Fe + 2HCl \to FeCl_2 + H_2\\ n_{H_2} = 1,5a + b = \dfrac{3,92}{22,4} = 0,175(2)\\ (1)(2) \Rightarrow a = 0,05 ; b = 0,1\\ m_{Al} = 0,05.27 = 1,35(gam); n_{Fe} = 0,1.56 = 5,6(gam)\)
\(b) n_{HCl} = 2n_{H_2} = 0,175.2 = 0,35(mol) \Rightarrow m_{HCl} = 0,35.36,5 = 12,775(gam)\)
Đúng 1
Bình luận (0)
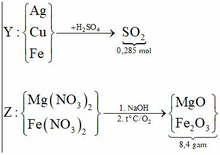
Cho 9,2 gam hỗn hợp X gồm Mg và Fe vào dung dịch hỗn hợp AgNO3 và Cu(NO3)2, thu được chất rắn Y (gồm 3 kim loại) và dung dịch Z. Hòa tan hết Y bằng dung dịch H2SO4 (đặc, nóng, dư), thu được 6,384 lít khí SO2 (sản phẩm khử duy nhất của S+6, ở đktc). Cho dung dịch NaOH dư vào Z, thu được kết tủa T. Nung T trong không khí đến khối lượng không đổi, thu được 8,4 gam hỗn hợp rắn. Biết các phản ứng xảy ra hoàn toàn. Phần trăm khôi lượng của Fe trong X là A. 79,13%. B. 28,00%. C. 70,00%. D. 60,87%.
Đọc tiếp
Cho 9,2 gam hỗn hợp X gồm Mg và Fe vào dung dịch hỗn hợp AgNO3 và Cu(NO3)2, thu được chất rắn Y (gồm 3 kim loại) và dung dịch Z. Hòa tan hết Y bằng dung dịch H2SO4 (đặc, nóng, dư), thu được 6,384 lít khí SO2 (sản phẩm khử duy nhất của S+6, ở đktc). Cho dung dịch NaOH dư vào Z, thu được kết tủa T. Nung T trong không khí đến khối lượng không đổi, thu được 8,4 gam hỗn hợp rắn. Biết các phản ứng xảy ra hoàn toàn. Phần trăm khôi lượng của Fe trong X là
A. 79,13%.
B. 28,00%.
C. 70,00%.
D. 60,87%.
Cho 9,2 gam hỗn hợp X gồm Mg và Fe vào dung dịch hỗn hợp AgNO3 và Cu(NO3)2, thu được chất rắn Y (gồm 3 kim loại) và dung dịch Z. Hòa tan hết Y bằng dung dịch H2SO4 (đặc, nóng, dư), thu được 6,384 lít khí SO2 (sản phẩm khử duy nhất của S+6, ở đktc). Cho dung dịch NaOH dư vào Z, thu được kết tủa T. Nung T trong không khí đến khối lượng không đổi, thu được 8,4 gam hỗn hợp rắn. Biết các phản ứng xảy ra hoàn toàn. Phần trăm khối lượng của Fe trong X là A. 79,13%. B. 28,00%. C. 70,00%. D. 60,87%.
Đọc tiếp
Cho 9,2 gam hỗn hợp X gồm Mg và Fe vào dung dịch hỗn hợp AgNO3 và Cu(NO3)2, thu được chất rắn Y (gồm 3 kim loại) và dung dịch Z. Hòa tan hết Y bằng dung dịch H2SO4 (đặc, nóng, dư), thu được 6,384 lít khí SO2 (sản phẩm khử duy nhất của S+6, ở đktc). Cho dung dịch NaOH dư vào Z, thu được kết tủa T. Nung T trong không khí đến khối lượng không đổi, thu được 8,4 gam hỗn hợp rắn. Biết các phản ứng xảy ra hoàn toàn. Phần trăm khối lượng của Fe trong X là
A. 79,13%.
B. 28,00%.
C. 70,00%.
D. 60,87%.
Cho 9,2 gam hỗn hợp X gồm Mg và Fe vào dung dịch hỗn hợp AgNO3 và Cu(NO3)2, thu được chất rắn Y (gồm 3 kim loại) và dung dịch Z. Hòa tan hết Y bằng dung dịch H2SO4 (đặc, nóng, dư), thu được 6,384 lít khí SO2 (sản phẩm khử duy nhất của S+6, ở đktc). Cho dung dịch NaOH dư vào Z, thu được kết tủa T. Nung T trong không khí đến khối lượng không đổi, thu được 8,4 gam hỗn hợp rắn. Biết các phản ứng xảy ra hoàn toàn. Phẩn trăm khối lượng của Fe trong X là A. 79,13% B. 28,00% C. 70,00% D. 60,87%
Đọc tiếp
Cho 9,2 gam hỗn hợp X gồm Mg và Fe vào dung dịch hỗn hợp AgNO3 và Cu(NO3)2, thu được chất rắn Y (gồm 3 kim loại) và dung dịch Z. Hòa tan hết Y bằng dung dịch H2SO4 (đặc, nóng, dư), thu được 6,384 lít khí SO2 (sản phẩm khử duy nhất của S+6, ở đktc). Cho dung dịch NaOH dư vào Z, thu được kết tủa T. Nung T trong không khí đến khối lượng không đổi, thu được 8,4 gam hỗn hợp rắn. Biết các phản ứng xảy ra hoàn toàn. Phẩn trăm khối lượng của Fe trong X là
A. 79,13%
B. 28,00%
C. 70,00%
D. 60,87%
Đáp án D
(Mg, Fe) + (AgNO3, Cu(NO3)2) => 3 kim loại
=> Chứng tỏ Mg, AgNO3, Cu(NO3)2 phản ứng hết, Fe còn dư; 3 kim loại là Ag, Cu, Fe.
Dung dịch Z chứa Mg(NO3)2 và Fe(NO3)2.
Đặt số mol Mg, Fe phản ứng, Fe dư lần lượt là a, b, c
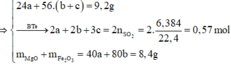
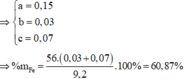
Đúng 0
Bình luận (0)
Cho 9,2 gam hỗn hợp X gồm Mg và Fe vào dung dịch hỗn hợp
A
g
N
O
3
và
C
u
(
N
O
3
)
2
, thu được chất rắn Y (gồm 3 kim loại) và dung dịch Z. Hòa tan hết Y bằng dung dịch
H
2
S
O
4
(đặc, nóng, dư), thu được 6,384 lit khí
S
O...
Đọc tiếp
Cho 9,2 gam hỗn hợp X gồm Mg và Fe vào dung dịch hỗn hợp A g N O 3 và C u ( N O 3 ) 2 , thu được chất rắn Y (gồm 3 kim loại) và dung dịch Z. Hòa tan hết Y bằng dung dịch H 2 S O 4 (đặc, nóng, dư), thu được 6,384 lit khí S O 2 (sản phẩm khử duy nhất của S + 6 , ở đktc). Cho dung dịch NaOH dư vào Z , thu được kết tủa T. Nung T trong không khí đến khối lượng không đổi, thu được 8,4 gam hỗn hợp rắn. Biết các phản ứng xảy ra hoàn toàn. Phần trăm khối lượng của Fe trong X là
A. 79,13%
B. 28,00%
C. 70,00%
D. 60,87%
Đáp án D
Sơ đồ quá trình:
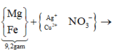
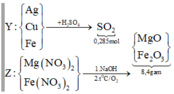
Gọi số mol Mg là x mol, Fe trong Y là y mol và Fe trong Z là z mol.
Ta có hệ phương trình:
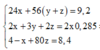
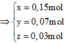
Theo đó, ![]()
Đúng 0
Bình luận (0)