Cho 1g hỗn hợp X gồm etan và etylen đi qua dung dịch Br2
a. Viết pt phản ứng sảy ra
b. Xác định % về klg của mỗi chất trong hỗn hợp biết rằng cho phản ứng xảy ra hoàn toàn thì phải dùng hết 80g dung dịch Br2 5%
Mong mn giúp đỡ cảm ơn nhiều ạ
Hỗn hợp X gồm: etan , etilen , axetilen và hiđro , trong đó thể tích etan bằng 1/6 thể tích của hiđrocacbon. Nung nóng 2240 ml hỗn hợp X với xúc tác Ni thì được 1344 ml hỗn hợp khí Y. Cho hỗn hợp Y đi châmk qua dung dịch nước Brôm dư thu được một khí Z thoát rakhỏi dung dịch , lượng Brôm đã phản ứng là 6,4 gam. Tính phần trăm thể tích mỗi khí trong hỗn hợp X. Biết các thể tích khí đều được đo ở đktc và các phản ứng sảy ra hoàn toàn.
Mỗi hỗn hợp khí X gồm 2 hiđrocacbon mạch hở (ở đktc). Lấy 268,8 ml X cho từ từ qua bình chứa dung dịch Br2 dư thì có 3,2 gam Br2 phản ứng, không có khí thoát ra khỏi bình. Mặt khác, đốt cháy hết 268,8 ml X thu được 1,408 gam CO2. Xác định công thức phân tử các hiđrocacbon trong X. Biết các phản ứng xảy ra hoàn toàn
Hòa tan hoàn toàn 13,92 gam hỗn hợp X gồm MgO, FeO và Fe2O3 phải dùng vừa hết 520 ml dung dịch HCl 1M. Mặt khác, khi lấy 0,27 mol hỗn hợp X đốt nóng trong ống sứ không có không khí rồi thổi một luồng H2 dư đi qua để phản ứng xảy ra hoàn toàn thì thu được m gam chất rắn và 4,86 gam nước. Xác định m ?
A. 16,56
B. 20,88
C. 25,06
D. 16,02
cho 5,6 lít (đkc) hỗn hợp X gồm 2 chất etilen và propin phản ứng hoàn toàn với dung dịch Brom thì tháy làm mất màu 400 ml dung dịch brom 1M.
a. Viết phương trình phản ứng xảy ra
b. tính thành phần % thể tích mỗi khí trong hỗn hợp
c . cho hỗn hợp X vào dung dịch bạc nitrat trong amoniac thu được m (gam) kết tủa . Tính m
\(a)C_2H_4+Br_2\rightarrow C_2H_4Br_2\\ C_3H_4+2Br_2\rightarrow C_3H_4Br_4\\ b)n_{hh}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\\ n_{Br_2}=0,4.1=0,4\left(mol\right)\\ Đặt:x=n_{C_2H_4};y=n_{C_3H_4}\\ Tacó:\left\{{}\begin{matrix}x+y=0,25\\x+2y=0,4\end{matrix}\right.\\ \Rightarrow\left\{{}\begin{matrix}x=0,1\\y=0,15\end{matrix}\right.\\ \%V_{C_2H_4}=\%n_{C_2H_4}=\dfrac{0,1}{0,25}.100=40\%;\%V_{C_3H_4}=60\%\\ c)X+AgNO_3/NH_3chỉcóC_3H_4pứ\\ C_3H_4+AgNO_3+NH_3\rightarrow C_3H_3Ag+2NH_4NO_3\\ n_{C_3H_2Ag_2}=n_{C_3H_4}=0,15\left(mol\right)\\ \Rightarrow m=0,15.147=22,05\left(g\right)\)
Một hỗn hợp A gồm etan (C2H6), etilen, axetilen, hiđro. Tỉ khối của hỗn hợp A so với CO2 là 0,4. Cho 11,2 lít hỗn hợp A đi qua dung dịch Br2 dư thấy khối lượng bình Br2 tăng thêm m gam. Hỗn hợp khí B thoát ra khỏi bình Br2 có thể tích 6,72 lít, trong đó khí có khối lượng phân tử nhỏ hơn chiếm 11,765% về khối lượng. Biết các phản ứng xảy ra hoàn toàn và các thể tích khí đo ở điều kiện tiêu chuẩn.
a. Viết các phương trình hóa học xảy ra.
b. Tính phần trăm thể tích các khí trong B.
c. Tính m gam.
a. Phương trình phản ứng :
C2H2 + 2Br2 → C2H2Br4 (1)
C2H4 + Br2 → C2H4Br2 (2)
b. Hỗn hợp khí B gồm có H2, C2H6. Gọi x, y ( mol ) lần lượt là số mol của H2 và C2H6 có trong 6,72 lít hỗn hợp B.
nB = x + y = 6,72 : 22,4 = 0,3 mol (I)
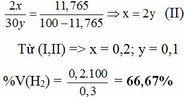
% V(C2H6) = 100% – 66,67% = 33,33%
c. nA = 11,2 : 22,4 = 0,5 mol , M A = 0,4 . 44 = 17,6 g/ mol
mA = 0,5 . 17,6 = 8,8 gam
mB = 0,2 . 2 + 0,1 . 30 = 3,4 gam
Vậy khối lượng bình Br2 tăng: m = mA – mB = 8,8 – 3,4 = 5,4 gam.
cho 28g hỗn hợp A gồm:axetilen,etilen,etan tác dụng hết AGNO3/NH3 thấy tạo thành 96g kết tủa vàng nhạt. Nếu cho hỗn hợp trên tác dụng với dd Br2 dư thì thấy tối đa 500ml Br2 2M a. Viết pt phản ứng xảy ra b.Tính khối lượng mỗi chất trong hỗn hợp A
\(n_{Br_2}=0,5.2=1\left(mol\right)\\ C_2H_2+2AgNO_3+2NH_3\rightarrow Ag_2C_2+2NH_4NO_3\\ n_{Ag_2C_2}=\dfrac{96}{240}=0,4\left(mol\right)\\ n_{C_2H_2}=n_{Ag_2C_2}=0,4\left(mol\right)\Rightarrow m_{C_2H_2}=0,4.26=10,4\left(g\right)\\ \Rightarrow m_{hh\left(C_2H_4,C_2H_6\right)}=28-10,4=17,6\left(g\right)\\ C_2H_2+2Br_2\rightarrow C_2H_2Br_4\left(1\right)\\ C_2H_4+Br_2\rightarrow C_2H_4Br_2\left(2\right)\\ n_{Br_2\left(2\right)}=1-2.0,4=0,2\left(mol\right)\\ n_{C_2H_4}=n_{Br_2\left(2\right)}=0,2\left(mol\right)\\ m_{C_2H_4}=0,2.28=5,6\left(g\right)\\ m_{C_2H_6}=17,6-5,6=12\left(g\right)\\ hhA:\left\{{}\begin{matrix}C_2H_4:5,6\left(g\right)\\C_2H_6:12\left(g\right)\\C_2H_2:10,4\left(g\right)\end{matrix}\right.\)
Trộn 0,15 mol H2 với 0,19 mol hỗn hợp anken A và ankin B, thu được hỗn hợp khí X ở nhiệt độ thường. Cho X đi từ từ qua Ni đun nóng để phản ứng xảy ra hoàn toàn, thu được hỗn hợp Y. Y cho qua dung dịch Br2 dư, phản ứng kết thúc thấy có 0,14 mol Br2 phản ứng. Phần trăm thể tích H2, A, B trong X tương ứng là
A. 44,12; 26,47; 29,41
B. 44,12; 29,41; 26,47
C. 44,12; 18,63; 37,25
D. 44,12; 37,25; 18,63
Cho 6,72 lít (đktc) hỗn hợp khí X gồm etilen và butadien vào dung dịch Br2 dư, sau khi phản ứng xảy ra hoàn toàn lượng brom phản ứng hết với 64g. Tính % về thể tích etilen và butadien trong X
\(n_{C_2H_4} = a(mol) ; n_{C_4H_6} = b(mol)\\ \Rightarrow a + b = \dfrac{6,72}{22,4} = 0,3(1)\\ C_2H_4 + Br_2 \to C_2H_4Br_2\\ C_4H_6 + 2Br_2 \to C_4H_6Br_4\\ n_{Br_2} = a + 2b = \dfrac{64}{160} = 0,4(2)\\ (1)(2) \Rightarrow a = 0,2 ; b = 0,1\\ \Rightarrow \%V_{C_2H_4} = \dfrac{0,2.22,4}{6,72}.100\% = 66,67%; \%V_{C_4H_6} =100\%-66,67\% = 33,33\%\)
Dẫn luồng hí CO dư đi qua 37,68 gam hỗn hợp X chứa CuO, Fe2O3, MgO, PbO, Fe3O4 nung nóng, đến khi các phản ứng xảy ra hoàn toàn thì thu được hỗn hợp chất rắn Y và hỗn hợp khí Z. Sục hỗn hợp khí Z vào dung dịch Ca(OH)2 dư, thu được 34,0 gam kết tủa trắng. a. Viết phương trình hóa học của các phản ứng xảy ra. b. Xác định khối lượng của hỗn hợp chất rắn Y
CO2 + Ca(OH)2 → CaCO3↓ + H2O
0,34 ←0,34
CO + O(Oxit) → CO2
Nhận thấy:
nO = nCO2
mX = mO (oxit) + mY
=> mY = 37,68 – 16 . 0,34 = 32,24g