Một loại đồng oxit màu đen có khối lượng mol phân tử là 80 g/mol. Oxit này có thành phần theo khối lượng là: 80% Cu và 20% O. Hãy tìm công thức hóa học của loại đồng oxit nói trên.

Những câu hỏi liên quan
Một loại oxit đồng màu đen có khối lượng mol phân tử là 80g. Oxit này có thành phần là 80% Cu và 20% O. Hãy tìm công thức hóa học của loại oxit đồng nói trên.
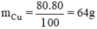
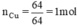 nguyên tử Cu.
nguyên tử Cu.
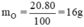
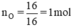 nguyên tử O.
nguyên tử O.
Suy ra trong 1 phân tử hợp chất có 1 nguyên tử Cu và 1 nguyên tử O.
Do đó công thức của oxit đồng màu đen là CuO.
Đúng 0
Bình luận (0)
Tìm thành phần phần trăm (theo khối lượng) các nguyên tố hóa học có trong những hợp chất sau:a) Fe3O4 và Fe2O3.b) SO2 và SO3.c. Một loại oxit đồng màu đen có khối lượng mol phân tử là 80g. Oxit này có thành phần là 80% Cu và 20% O. Hãy tìm công thức hóa học của loại oxit đồng nói trên.d. Hãy tìm công thức hóa học của khí A.- Khí A nặng hơn khí hiđro 17 lần.- Thành phần theo khối lượng của khí A là 5,88% H và 94,12% S.
Đọc tiếp
Tìm thành phần phần trăm (theo khối lượng) các nguyên tố hóa học có trong những hợp chất sau:
a) Fe3O4 và Fe2O3.
b) SO2 và SO3.
c. Một loại oxit đồng màu đen có khối lượng mol phân tử là 80g. Oxit này có thành phần là 80% Cu và 20% O. Hãy tìm công thức hóa học của loại oxit đồng nói trên.
d. Hãy tìm công thức hóa học của khí A.
- Khí A nặng hơn khí hiđro 17 lần.
- Thành phần theo khối lượng của khí A là 5,88% H và 94,12% S.
a) Với Fe3O4 thì Fe là 72,4% và O là 27,6%;
Với Fe2O3 thì Fe là 70% và O là 30%
b) Với SO2 thì S là 50% và O là 50%
Với SO3 thì S là 40% và O là 60%
c) mCu= \(\dfrac{80.80}{100}\)=64(g) ; mO=\(\dfrac{80.20}{100}\)=16(g)
nCu=\(\dfrac{64}{64}\)=1(mol) ; nO=\(\dfrac{16}{16}\)=1(mol)
Vậy CTHH của oxit đồng màu đen là: CuO
d) dA/H2=\(\dfrac{Ma}{2}\)=17 => MA=2.17=34(đvC)
H =\(\dfrac{5,88.34}{100}\)\(\approx\)2(đvC) ; S =\(\dfrac{94,12.34}{100}\)\(\approx\)32
=> CTHH của chất khí A là SH2
Đúng 0
Bình luận (0)
Một loại đồng oxit màu đen có khối lượng mol phân tử là 20g/mol, có thành phần về khối lượng là 80% Cu và 20% O. Công thức của oxit
Đồng oxit nào mà có M= 20(g/mol) được em.
Nhưng em bảo 80% Cu, 20% O thì anh thấy chắc là CuO rồi nè
Đúng 3
Bình luận (0)
sửa đề M = 80 g/mol
\(n_{Cu}=\dfrac{80.80\%}{64}=1\left(mol\right)\\ n_{O_2}=\dfrac{80-64}{16}=1\left(mol\right)\\ Cthh:CuO\)
Đúng 2
Bình luận (0)
Câu 4 (1 điểm): Một oxit của lưu huỳnh có thành phần trăm của lưu huỳnh là 50% và Oxi là 50%. Biết oxit này có khối lượng mol phân tử là 64 g/mol. Hãy tìm công thức hóa học của oxit đó.
Cho nguyên tử khối: O=16, Cu=64, Mg=24, Fe=56, Cl=35,5, Ag =108, N=14
\(m_S=\dfrac{64.50}{100}=32\left(g\right)=>n_S=\dfrac{32}{32}=1\left(mol\right)\)
\(m_O=\dfrac{64.50}{100}=32\left(g\right)=>n_O=\dfrac{32}{16}=2\left(mol\right)\)
=> CTHH: SO2
Đúng 0
Bình luận (2)
Một oxit của Sắt có thành phần trăm của Sắt là 70% và Oxi là 30%. Biết oxit này có khối lượng mol phân tử là 160 g/mol. Hãy tìm công thức hóa học của oxit trên.
Giải nhanh giùm mik
Khối lượng của các nguyên tố trong hợp chất là:
\(m_{FE}=\dfrac{70.160}{100}=112\left(g\right)\)
\(m_O=\dfrac{30.160}{100}=48\left(g\right)\)
Số mol có trong mỗi nguyên tố là:
\(n_{FE}=\dfrac{m_{FE}}{M_{FE}}=\dfrac{112}{56}=2\left(mol\right)\)
\(n_O=\dfrac{m_O}{M_O}=\dfrac{48}{16}=3\left(mol\right)\)
Vậy hợp chất có 2 nguyên tử Fe, 3 nguyên tử O
Công thức hóa học của hợp chất là: \(FE_2O_3\)
Đúng 3
Bình luận (0)
\(m_{Fe}=\dfrac{160.70}{100}=112g\\ m_O=160-112=48g\\ n_{Fe}=\dfrac{112}{56}=2mol\\n_O=\dfrac{48}{16}=3mol\\ \Rightarrow CTHH:Fe_2 O_3\)
Đúng 2
Bình luận (0)
gọi CT tổng quát là FexOy
mFe:mO=56x:16y
=70:30
=70/56:30/16
=2:3
vậy CTHH là Fe2O3
Đúng 0
Bình luận (0)
1 loại đồng oxít màu đen có khối lượng mol nguyên tử 80g/mol và 20%O
hãy tìm công thức hóa học của loại đồng oxít trên
CuxOy
\(\frac{16y}{80}\) .100% = 20% => y= 1
=> 64x + 16= 80 => x= 1
=> công thức CuO
Đúng 0
Bình luận (0)
16y/80*100%=20% ta duoc y=1
64x+16=80 ta duoc x=1
vay cong thuc hoa hoc CuO
Đúng 0
Bình luận (0)
Cho biết khối lượng mol một oxit của kim loại là 160 g/mol, thành phần về khối lượng của kim loại trong oxit đó là 70%. Lập công thức hóa học của oxit. Gọi tên oxit đó
\(CT:M_xO_y\)
\(\%M=\dfrac{xM}{160}\cdot100\%=70\%\)
\(\Rightarrow xM=112\)
\(\text{Với : }\) \(x=2\Rightarrow M=56\)
\(M=56\cdot2+16y=160\left(g\text{/}mol\right)\)
\(\Rightarrow y=3\)
\(CT:Fe_2O_3:\text{Sắt (III) oxit}\)
Đúng 4
Bình luận (0)
Một oxit kim loại có khối lượng mol là 102g , thành phần phần trăm theo khối lượng của kim loại trong oxit là 52,94% . Xác định công thức của oxit đó ?
Hóa học 8.
Một oxit của lưu huỳnh có thành phần trăm của lưu huỳnh là 50% và Oxi là 50%.Biết oxit này có khối lượng mol phân tử là 64g/mol.Hãy tìm công thức hóa học của oxit đó.
Ta có: \(\left\{{}\begin{matrix}m_S=64\cdot50\%=32\left(g\right)\\m_O=64\cdot50\%=32\left(g\right)\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}n_S=\dfrac{32}{32}=1\left(mol\right)\\n_O=\dfrac{32}{16}=2\left(mol\right)\end{matrix}\right.\)
Vậy CTHH là \(SO_2\)
Đúng 2
Bình luận (2)


























