Cho 1 lít khí oxi và 1 lít khí nitơ cùng ở 00C. Hãy so sánh thể tích của chúng khi nhiệt độ tăng lên 200C. Giải thích
tại nhiệt độ và áp suất xác định, khối lượng của 7 lít khí oxi & 8 lít khí nitơ đều có khối lượng 10 g. không khí có khoảng 80% thế tích khí nitơ và 20%thể tích khí oxi. tính thể tích của 10 g không khí tại cùng điều kiện nhiệt độ và áp suất trên
Đốt cháy hoàn toàn V lít hơi một amin X bằng một lượng oxi vừa đủ tạo ra 8V lít hỗn hợp gồm khí cacbonic, khí nitơ và hơi nước (các thể tích khí và hơi đều đo ở cùng điều kiện). Amin X tác dụng với axit nitrơ ở nhiệt độ thường, giải phóng khí nitơ. Chất X là:
A. C H 2 = C H - N H - C H 3
B. C H 3 - C H 2 - N H - C H 3
C. C H 3 - C H 2 - C H 2 - N H 2
D. C H 2 = C H - C H 2 - N H 2
Người ta nén 6 lít khí ở nhiệt độ 27 ° C để cho thể tích của khí chỉ còn 1 lít, vì nén nhanh nên khí bị nóng lên đến 77 ° C. Khi đó áp suất của khí tăng lên bao nhiêu lần?
A. 7 lần
B. 6 lần
C. 4 lần
D. 2 lần
Chọn đáp án A
? Lời giải:
+ Áp dụng công thức:
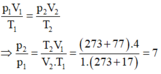
Người ta nén 10 lít khí ở nhiệt độ 270C để cho thể tích của khí chỉ còn 4 lít, vì nén nhanh nên khí bị nóng lên đến 600C. Khi đó áp suất của khí tăng lên bao nhiêu lần?
Áp dụng công thức
p 1 V 1 T 1 = p 2 V 2 T 2 ⇒ p 2 p 1 = T 2 V 1 V 2 . T 1 = ( 273 + 60 ) .10 4. ( 273 + 27 ) = 2 , 775
Người ta nén 10 lít khí ở nhiệt độ 27 ° C để cho thể tích của khí chỉ còn 4 lít, vì nén nhanh nên khí bị nóng lên đến 60 ° C . Khi đó áp suất của khí tăng lên bao nhiêu lần ?
Octain: C8H18 cháy trong oxi hoặc ko khí sinh ra CO2 và hơi nước
a) Tính thể tích khí octain cháy trong 500 lít ko khí biết oxi chiếm 1/5 ko khí
b) tính thể tích oxi cần dùng để đốt cháy 240 lít octain biết thể tích khí đó ở cùng nhiệt độ và áp suất
\(2C_8H_{18}+25O_2\xrightarrow{t^o}16CO_2+18H_2O\\ a,n_{O_2}=\dfrac{500}{5.16}=6,25(mol)\\ \Rightarrow n_{C_8H_{18}}=\dfrac{2}{25}.6,25=0,5(mol)\\ \Rightarrow V_{C_8H_{18}}=0,5.22,4=11,2(l)\\ b,n_{C_8H_{18}}=\dfrac{240}{22,4}=\dfrac{75}{7}(mol)\\ \Rightarrow n_{O_2}=\dfrac{1875}{14}(mol)\\ \Rightarrow V_{O_2}=\dfrac{1875}{14}.22,4=3000(l)\)
Tính khối lượng riêng khí oxi đựng trong một bình thể tích 10 lít dưới áp suất 150atm ở nhiệt độ 00C. Biết ở điều kiện chuẩn khối lượng riêng của oxi là 1,43kg/m3.
Ở điều kiện chuẩn có p0 = 1atm m = V0.
Ở O0C , áp suất 150atm m = V ρ .
Khối lượng không đổi:
V 0 . ρ 0 =V . ρ ⇒ V = ρ 0 . V 0 ρ
Mà V0 ρ o = V ρ
⇒ ρ = p . ρ 0 p 0 = 214 , 5 k g / m 3
Khi đốt 1 lít chất X cần 5 lít oxi thu được 3 lít CO2 , 4 lít hơi nước (thể tích các khí đo ở cùng điều kiện nhiệt độ, áp suất). Xác định CTPT của X.
VC = 3 lit; V H = 8
→ V O = 0 vì VO ban đầu = 5.2 = 10 lit = VO sau phản ứng = 2*VC+ V H
Công thức tổng quát : CxHy ta có x:y = 3:8 → công thức của X là C3H8.
VC = VCO2 = 3 (l)
VH = 2 . VH2O = 2 . 4 = 8 (l)
VO (trong oxi) = 5 . 2 = 10 (l)
VO (sau p/ư) = 4 . 2 + 3 = 10 (l)
So sánh: 10 = 10 => trong X chỉ có H và C
CTPT: CxHy
=> x : y = 3 : 8
Vậy X là C3H8
VC = 3 lit; V H = 8
→ V O = 0 vì VO ban đầu = 5.2 = 10 lit = VO sau phản ứng = 2*VC+ V H
Công thức tổng quát : CxHy ta có x:y = 3:8 → công thức của X là C3H8.
So sánh nhiệt lượng thu vào của hai vật trong các trường hợp sau:
a. Hai cục đồng cùng khối lượng, cục 1 tăng từ 200C lên 500C, cục 2 tăng từ 00C lên 900C ?
b. 5kg nước và 2kg nước cùng tăng từ 200C lên 800C ?
c. 5kg nhôm tăng từ 200C lên 500C và 10kg nhôm tăng từ 200C lên 800C ?
giúp e với ạ , e cảm ơn
Cho V lít hỗn hợp khí X gồm O2 và O3. Thực hiện phản ứng ozon phân hoàn toàn, sau một thời gian thu được khí Y và thể tích khí tăng lên 30% so với thể tích ban đầu , biết thể tích các khí đo ở cùng điều kiện nhiệt độ và áp suất. Phần trăm thể tích của O2 trong hỗn hợp đầu là:
A. 25%
B. 40%
C. 50%
D. 57,14%