cho 2,4 gam kim loại A có hóa trị 2 tác dụng với axit sunfuric dư,thấy thoát 2,24 khí Hidro ở điều kiện tiêu chuẩn.Tìm kim loại A
Các bạn giúp dùm mình với ạ :):):):)
Cho 2 gam một kim loại (chưa rõ hóa trị) tác dụng với dung dịch axit sunfuric loãng thu được 0,8 lít khí thoát ra (đktc). Xác định kim loại và viết công thức oxit (hóa trị cao nhất của kim loại đó) giúp mình với ạ
\(n_{H_2}=\dfrac{0,8}{22,4}=\dfrac{1}{28}\left(mol\right)\)
PTHH: 2A + xH2SO4 --> A2(SO4)x + xH2
_____\(\dfrac{1}{14x}\)<-----------------------------\(\dfrac{1}{28}\)
=> \(M_A=\dfrac{2}{\dfrac{1}{14x}}=28x\left(g/mol\right)\)
Xét x = 1 => MA = 28 (L)
Xét x = 2 => MA= 56 (g/mol) => Fe
=> CT oxit hóa trị cao nhất là Fe2O3
\(n_{Al} = \dfrac{2,7}{27} = 0,1(mol)\\ 2Al + 3H_2SO_4 \to Al_2(SO_4)_3 + 3H_2\\ n_{H_2} = \dfrac{3}{2}n_{Al} = 0,15(mol)\\ \Rightarrow V_{H_2} = 0,15.22,4 = 3,36(lít)\\ n_{HCl} = \dfrac{8,1}{36,5} = \dfrac{81}{365}(mol)\\ 2Al + 6HCl \to 2AlCl_3 + 3H_2\\ \dfrac{n_{Al}}{2} = 0,05 > \dfrac{n_{HCl}}{6} = \dfrac{27}{730} \to Al\ dư\\ n_{Al\ pư} = \dfrac{1}{3}n_{HCl} = \dfrac{27}{365}(mol)\\ \)
\(m_{Al\ dư} = 2,7 - \dfrac{27}{265}.27 = 0,703(gam)\)
Câu 2. Cho 19,4 gam hỗn hợp 2 kim loại Cu và Zn tác dụng với dung dịch HCl
(dư) thu được 4,48 lít khí hidro thoát ra (điều kiện tiêu chuẩn). Tính giá trị khối
lượng mỗi kim loại trong hỗn hợp.
a, Cu không tác dụng với dd HCl.
PT: Zn+2HCl→ZnCl2+H2
b, Ta có: nH2=\(\dfrac{4,48}{22,4}\)=0,2(mol)
Theo PT: nZn=nH2=0,2(mol)
⇒mZn=0,2.65=13(g)
⇒mCu=19,4−13=6,4(g)
a, Cu không tác dụng với dd HCl.
PT: Zn+2HCl→ZnCl2+H2
b, Ta có: nH2=4,48/22,4=0,2(mol)
Theo PT: nZn=nH2=0,2(mol)
⇒mZn=0,2.65=13(g)
⇒mCu=19,4−13=6,4(g)
Cho 4,6g kim loại X hóa trị I tác dụng hoàn toàn với H2O thu được 2,24(l) khí H2 ở điều kiện tiêu chuẩn. Tìm kim loại X?
2X+H2O⇒X2O+H2
+nH2=\(\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
+nX=2nH2=0,2(mol)
+X = \(\dfrac{4,6}{0,2}=23\left(dvC\right)\)⇒X là Natri
cho 6,5 g bột kim loại M có hóa trị không đôi tác dụng với HCl dư , thu được 2,24 lít khí ở điều kiện tiêu chuẩn . Xác định tên M .
Gọi hóa trị của KL M là n
2M +2nHCl=2 MCln+nH2
nH2=2,24/22,4=0,1 mol --> nM= 0,1.2/n=0,2/n mol
mM= 0,2.n. MM=6,5 => MM=32,5n
n=1 --> MM= 32,5( loại)
n=2 --> MM=65(Zn)
1.Khi làm bay hơi 82 g dung dịch NaCl 12% thu được A.12g NaCl B.9.84g NaCl C.9.48g D.8.2g 2. Cho 7,8 g kim loại x hóa trị 1 tác dụng hết với nước thấy thoát ra 2,24 lít h2 ở điều kiện tiêu chuẩn x là kim loại nào trong số các kim loại sau đây A.kali B.liti C.natri D.bạc
Câu 1 :
m NaCl = 82.12% = 9,84 gam
Đáp án B
Câu 2 : n H2 = 2,24/22,4 = 0,1(mol)
$2X + 2HCl \to 2XCl + H_2$
n X = 2n H2 = 0,2(mol)
=> M X = 7,8/0,2 = 39(Kali)
Đáp án A
Hỗn hợp X gồm Fe và kim loại M có hóa trị không đổi. Cho 15,2 gam X tác dụng với dung dịch HC1 dư, thấy thoát ra 2,24 lít khí H2 (đktc). Nếu cho lượng X như trên tác dụng với dung dịch HNO3 dư, thu được 4,48 lít khí NO (đktc). Kim loại M là
A. Ag.
B. Cu.
C. Al.
D. Mg.
Đáp án B
n H 2 = 0 , 1 ; n NO = 0 , 4 . Gọi n là hóa trị của M.
Căn cứ vào 4 đáp án ta có 2 trường hợp:
+) M là kim loại đứng trước H trong dãy hoạt động hóa học. Khi đó cả M và Fe có phản ứng với dung dịch HCl. Vì hóa trị của M không đổi nên sự chênh lệch về số electron trao đổi trong hai lần thí nghiệm là do sắt có hai mức hóa trị là II và III.
Áp dụng định luật bảo toàn mol electron:
- Khi hòa tan hỗn hợp vào dung dịch HCl, ta có: 2 n Fe + n . n M = 2 n H 2
- Khi hòa tan hỗn hợp vào dung dịch HNO3, ta có: 3 n Fe + n . n M = 3 n NO
Trừ hai vế của hai phương trình cho nhau, ta được:
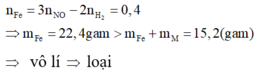
+) M là kim loại đứng sau H và trước Pt trong dãy hoạt động hóa học. Khi đó M không phản ứng được với dung dịch HCl và phản ứng được với dung dịch HNO3. Áp dụng định luật bảo toàn mol electron:
- Khi hòa tan hỗn hợp vào dung dịch HCl, ta có:

Cho 1,2 g kim loại magie tác dụng vừa đủ với dung dịch axit sunfuric. Thể tích khí hidro thu được ở điều kiện tiêu chuẩn là:
A. 44,8lit. B. 4,48 lit.
C. 2,24lit. D. 1,12 lit.
Giúp mình vs ạ:(((
\(n_{Mg}=\dfrac{1,2}{24}=0,05(mol)\\ Mg+H_2SO_4\to MgSO_4+H_2\\ \Rightarrow n_{H_2}=0,05(mol)\\ \Rightarrow V_{H_2}=0,05.22,4=1,12(l)\)
Cho 6,3g hỗn hợp 2 kim loại cùng hóa trị 1 tác dụng với axit sunfuric loãng thì thu được 2,24 lit khí (đktc). Hai kim loại đó là
\(n_{H_2}=\dfrac{2.24}{22.4}=0.1\left(mol\right)\)
\(2\overline{M}+H_2SO_4\rightarrow\overline{M}_2SO_4+H_2\)
\(0.2........................................0.1\)
\(M_{\overline{M}}=\dfrac{6.3}{0.2}=31.5\)
\(\Rightarrow A< 31.5< B\)
\(A:Na,Li\)
\(B:K\)
Vậy : hai chất có thể là : Li và K hoặc Na và K.