Tính thành phần phần trăm (theo khối lượng) của các nguyên tố hóa học có trong những hợp chất sau: CO2, Fe3O4, SO3, K2CO3, Na2SO4, KClO3, KMnO4, CuSO4, ZnCl2, NaHCO3.

Những câu hỏi liên quan
Tìm thành phần phần trăm (theo khối lượng) các nguyên tố hóa học có trong những hợp chất sau:
a) CO và CO2.
b) Fe3O4 và Fe2O3.
c) SO2 và SO3.
a) Hợp chất CO có MCO = 12 + 16 = 28 g/mol
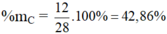
%mO = 100 – 42,86 = 57,14%
Hợp chất CO2: có MCO2 = 12 + 32 = 44 g/mol
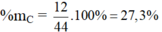
%mO = 100 – 27,3 = 72,7%
b) Hợp chất Fe3O4: MFe3O4 = 3.56 + 4.16 = 232 g/mol
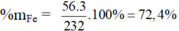
%mO = 100 – 72,4 = 27,6%
Hợp chất Fe2O3: MFe2O3 = 2.56 + 3.16 = 160 g/mol
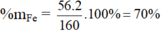
%mO = 100 – 70 = 30%
c) Hợp chất SO2 : MSO2 = 32 + 2.16 = 64 g/mol
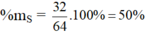
%mO = 100 – 50 = 50%
Hợp chất SO3 : MSO3 = 32 + 16.3 = 80 g/mol
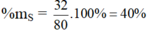
%mO = 100 – 40 = 60%
Đúng 2
Bình luận (0)
tìm thành phần phần trăm ( theo khối lượng ) của các nguyên tố hóa học có trong nhưng hợp chất sau
a/Fe2O3 b/Fe3O4 c/SO3 d/CuSO4 g/CH4
a) Fe2O3----> \(\dfrac{56.2}{56.2+16.3}.100\%=70\%\\ =>100\%-70\%=30\%\)
Đúng 1
Bình luận (0)
b) Fe3O4---->\(\dfrac{56.3}{56.3+16.4}.100\%=72,41\%\\ =>100\%-72,41\%=27,59\%\)
Đúng 1
Bình luận (0)
c)SO3---->\(\dfrac{32}{32+16.3}.100\%=40\%\\ =>100\%-40\%=60\%\)
Đúng 1
Bình luận (0)
Xem thêm câu trả lời
Tìm thành phần phần trăm theo khối lượng các nguyên tố hóa học có trong những hợp chất sau: CuO, MgCO3, AgCl, HNO3, CO2, KMnO4, Ba(OH)2.
\(PTK_{CuO}=64+16=80\left(đvC\right)\)
\(\%m_{Cu}=\) \(\dfrac{64}{80}.100=80\%\)
\(\%m_O=100-80=20\%\)
\(PTK_{MgCO_3}=24+12+3.16=84\left(đvC\right)\)
\(\%m_{Mg}=\dfrac{24}{84}.100=28,57\%\)
\(\%m_C=\dfrac{12}{84}.100=14,28\%\)
\(\%m_O=\dfrac{3.16}{84}.100=57,14\%\)
các ý còn lại làm tương tự
Đúng 1
Bình luận (0)
tính thành phần phần trăm(theo khối lượng) của các nguyên tố hóa học có trong hợp chất sau;KMnO4
\(M_{KMnO_4}=158(g/mol)\\ \%_{K}=\dfrac{39}{158}.100\%=24,68\%\\ \%_{Mn}=\dfrac{55}{158}.100\%=34,81\%\\ \%_O=100\%-24,68\%-34,81\%=40,51\%\)
Đúng 1
Bình luận (0)
Tính phần trăm khối lượng của mỗi nguyên tố trong hợp chất: CuSO4; K2CO3; Na2SO4.
\(M_{CuSO_4}=64+32+16.4=160\left(\dfrac{g}{mol}\right)\)
\(\%Cu=\dfrac{64}{160}.100\%=40\%\)
\(\%S=\dfrac{32}{160}.100\%=20\%\)
\(\%O=100\%-20\%-40\%=40\%\)
Đúng 4
Bình luận (0)
\(M_{K_2CO_3}=39.2+12+16.3=138\left(\dfrac{g}{mol}\right)\)
\(\%K=\dfrac{39.2}{138}.100\%=56,5\%\)
\(\%C=\dfrac{12}{138}.100\%=8,7\%\)
\(\%O=100\%-56,5\%-8,7\%=34,8\%\)
Đúng 1
Bình luận (0)
\(M_{Ná_2SO_4}=23.2+32+16.4=142\left(\dfrac{g}{mol}\right)\)
\(\%Na=\dfrac{23.2}{142}.100\%=32,4\%\)
\(\%S=\dfrac{32}{142}.100\%=22,5\%\)
\(\%O=100\%-32,4\%-22,5\%=45,1\%\)
Đúng 2
Bình luận (0)
Câu 10 : Tính thành phần phần trăm (theo khối lượng) của các nguyên tố hóa học có trong những hợp
chất sau :
a) CuSO4
b) Fe3O4
c) FeO
d) K2CO3
\(a,\%Cu=\dfrac{m_{Cu}}{M_{CuSO_4}}=\dfrac{64}{160}=40\%\\ \%S=\dfrac{m_S}{M_{CuSO_4}}=\dfrac{32}{160}=20\%\\ \%O=100\%-\%Cu-\%S=100\%-40\%-20\%=40\%\)
\(b,\%Fe=\dfrac{m_{Fe}}{M_{Fe_3O_4}}=\dfrac{168}{232}=72,41\%\\ \%O=100\%-\%Fe=100\%-72,41\%=27,59\%\)
\(c,\%Fe=\dfrac{m_{Fe}}{M_{FeO}}=\dfrac{56}{72}=77,77\%\\ \%O=100\%-\%Fe=100\%-77,77\%=22,23\%\)
\(d,\%K=\dfrac{m_K}{M_{K_2SO_3}}=\dfrac{78}{138}=56,52\%\\ \%C=\dfrac{m_C}{M_{K_2SO_4}}=\dfrac{12}{138}=8,69\%\\ \%O=100\%-\%K-\%C=100\%-56,52\%-8,69\%=34,79\%\)
Đúng 1
Bình luận (0)
a) \(M_{CúSO_4}=64+32+16.4=160\left(DvC\right)\)
\(m_{Cú}=\dfrac{64}{160}.100\%=40\%\)
\(m_S=\dfrac{32}{160}.100\%=20\%\)
\(m_O=\dfrac{16.4}{160}.100\%=40\%\)
Đúng 1
Bình luận (0)
b) \(M_{Fe_3O_4}=56.3+16.4=232\left(DvC\right)\\ \%Fe=\dfrac{56.3}{232}.100\%=72\%\\ \%O=100\%-74\%=26\%\)
Đúng 0
Bình luận (0)
Xem thêm câu trả lời
Tìm thành phần phần trăm (theo khối lượng) các nguyên tố hóa học có trong những hợp chất sau:a) Fe3O4 và Fe2O3.b) SO2 và SO3.c. Một loại oxit đồng màu đen có khối lượng mol phân tử là 80g. Oxit này có thành phần là 80% Cu và 20% O. Hãy tìm công thức hóa học của loại oxit đồng nói trên.d. Hãy tìm công thức hóa học của khí A.- Khí A nặng hơn khí hiđro 17 lần.- Thành phần theo khối lượng của khí A là 5,88% H và 94,12% S.
Đọc tiếp
Tìm thành phần phần trăm (theo khối lượng) các nguyên tố hóa học có trong những hợp chất sau:
a) Fe3O4 và Fe2O3.
b) SO2 và SO3.
c. Một loại oxit đồng màu đen có khối lượng mol phân tử là 80g. Oxit này có thành phần là 80% Cu và 20% O. Hãy tìm công thức hóa học của loại oxit đồng nói trên.
d. Hãy tìm công thức hóa học của khí A.
- Khí A nặng hơn khí hiđro 17 lần.
- Thành phần theo khối lượng của khí A là 5,88% H và 94,12% S.
a) Với Fe3O4 thì Fe là 72,4% và O là 27,6%;
Với Fe2O3 thì Fe là 70% và O là 30%
b) Với SO2 thì S là 50% và O là 50%
Với SO3 thì S là 40% và O là 60%
c) mCu= \(\dfrac{80.80}{100}\)=64(g) ; mO=\(\dfrac{80.20}{100}\)=16(g)
nCu=\(\dfrac{64}{64}\)=1(mol) ; nO=\(\dfrac{16}{16}\)=1(mol)
Vậy CTHH của oxit đồng màu đen là: CuO
d) dA/H2=\(\dfrac{Ma}{2}\)=17 => MA=2.17=34(đvC)
H =\(\dfrac{5,88.34}{100}\)\(\approx\)2(đvC) ; S =\(\dfrac{94,12.34}{100}\)\(\approx\)32
=> CTHH của chất khí A là SH2
Đúng 0
Bình luận (0)
tìm thành phần phần trăm(theo khối lượng)các nguyên tố hoá học có trong những hợp chất sau:
a,CO và CO2 b,Fe3O4 và Fe2O3 c,SO2 vàSO3
a/
+ CO
%mC = \(\frac{12}{12+16}.100\%=42,86\%\)%mO = 100% - 42,86% =57,14%+CO2
%mC = \(\frac{12}{12+16.2}.100\%=27,27\%\) %mO = 100% - 27,27% = 72,73%b/
+Fe3O4
%mFe = \(\frac{56.3}{56.3+16.4}.100\%=72,41\%\) %mO = 100% - 72,41% = 27,59%+ Fe2O3
%mFe = \(\frac{56.2}{56.2+16.3}.100\%=70\%\) %mO = 100% - 70% = 30%c/
+SO2
%mS = \(\frac{32}{32+16.2}.100\%=50\%\)%mO = 100% - 50% = 50%+ SO3
%mS = \(\frac{32}{32+16.3}.100\%=40\%\) %mO = 100% - 40% = 60%
Đúng 1
Bình luận (0)
Tính thành phần,phần trăm theo khối lượng các nguyên tố hóa học có trong những hợp chất sau:
a.CaO
b.MgCO3
c.NaOH
Xem chi tiết
\(CaO:\%^MCa=\dfrac{40}{40+16}\cdot100\%=71,43\%\\ \%^MO=100\%-71,43\%=28,57\%\)
\(MgCO_3:\%^MMg=\dfrac{24}{24+12+16\cdot3}\cdot100\%=28,57\%\\ \%^MC=\dfrac{12}{24+12+16\cdot3}\cdot100\%=14,29\%\\ \%^MO=100\%-28,57\%-14,29\%=57,14\%\)
\(NaOH:\%^MNa=\dfrac{23}{23+16+1}\cdot100\%=57,5\%\\ \%^MO=\dfrac{16}{23+16+1}\cdot100\%=40\%\\ \%^MH=100\%-57,5\%-40\%=2,5\%\)
Đúng 3
Bình luận (0)
Một hợp chất có công thức hóa học là K2CO3. Em hãy cho biết:
a) Khối lượng mol của chất đã cho.
b) Thành phần phần trăm (theo khối lượng) của các nguyên tố có trong hợp chất.
a) MK2CO3 = 39.2 + 12 + 16.3 = 138 (g)
b)
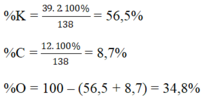
Đúng 0
Bình luận (0)
























