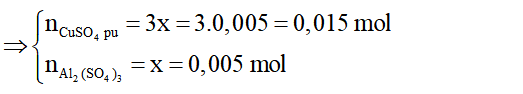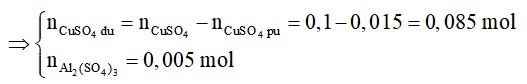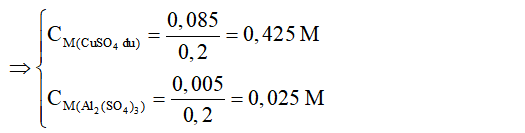nhúng một thanh sắt 8g vào 500ml dung dịch CuSO4 nồng độ 2M.Sau một thời gian lấy ra thấy thanh sắt nặng 8,8g. tính nồng độ mol của dung dịch sau phản ứng. Coi thể tích thay đổi không đáng kể

Những câu hỏi liên quan
Nhúng một thanh sắt và một thanh kẽm vào một cốc chứa 500ml dung dịch CuSO4, sau một thời gian lấy hai thanh kim loại ra khỏi cốc thì mỗi thanh có thêm đồng bám vào. khối lượng dung dịch bị giảm mất 0,27g. Trong dung dịch sau phản ứng nồng độ mol của ZnSO4 gấp 2,5 lần nồng độ mol của FeSO4.Thêm dung dịch natri hidroxit (lấy dư) lọc lấy hết kết tủa rồi nung ngoài khồn khí đến khối lượng không đổi thu được 14,5g chất rắn.Tính số gam Cu bám trên mỗi thanh kim loại và nồng độ mol của CuSO4 ban đầu
Đọc tiếp
Nhúng một thanh sắt và một thanh kẽm vào một cốc chứa 500ml dung dịch CuSO4, sau một thời gian lấy hai thanh kim loại ra khỏi cốc thì mỗi thanh có thêm đồng bám vào. khối lượng dung dịch bị giảm mất 0,27g. Trong dung dịch sau phản ứng nồng độ mol của ZnSO4 gấp 2,5 lần nồng độ mol của FeSO4.Thêm dung dịch natri hidroxit (lấy dư) lọc lấy hết kết tủa rồi nung ngoài khồn khí đến khối lượng không đổi thu được 14,5g chất rắn.Tính số gam Cu bám trên mỗi thanh kim loại và nồng độ mol của CuSO4 ban đầu
Cho một lá sắt có khối lượng 5gam vào 50ml dung dịch CuSO4 15% có khối lượng riêng 1,12g/ml. Sau một thời gian phản ứng, người ta lấy lá sắt ra khỏi dung dịch, rửa nhẹ, làm khô cân nặng 5,16g.1. Viết phương trình hóa học2. Tính số mol CuSO4 còn dư trong dung dịch sau phản ứng3. Tính nồng độ mol của các chất có trong dung dịch sau phản ứng. Biết thể tích dung dịch thay đổi không đáng kể
Đọc tiếp
Cho một lá sắt có khối lượng 5gam vào 50ml dung dịch CuSO4 15% có khối lượng riêng 1,12g/ml. Sau một thời gian phản ứng, người ta lấy lá sắt ra khỏi dung dịch, rửa nhẹ, làm khô cân nặng 5,16g.
1. Viết phương trình hóa học
2. Tính số mol CuSO4 còn dư trong dung dịch sau phản ứng
3. Tính nồng độ mol của các chất có trong dung dịch sau phản ứng. Biết thể tích dung dịch thay đổi không đáng kể
trên mạng mk thấy có một bài tượng tự trên hocmai, bạn vào đó tham khảo nhé
Đúng 0
Bình luận (2)
Nhúng 1 thanh sắt 8g vào 500ml dung dịch CuSO\(_4\) 2M sau thời gian lấy thanh sắt ra và cân thấy nặng 8,8g
a. Tính khối lượng kim loại tạo thành
b. Tính nồng độ dung dịch sau phản ứng ( coi V chất rắn ko đáng kể )
\(n_{Fe.pu}=x\)
\(n_{Fe}=\frac{8}{56}=\frac{1}{7}\left(mol\right)\)
\(PTHH:Fe+CuSO_4\rightarrow Cu+FeSO_4\)
(mol) x x x x
Theo đề bài ta có:
\(64x-56x=8,8-8\Leftrightarrow x=\frac{0,8}{8}=0,1\left(mol\right)\)
\(m_{Cu}=64x=64.0,1=6,4\left(g\right)\\ m_{Fe.du}=\left(\frac{1}{7}-0,1\right).56=2,4\left(g\right)\)
\(V_{ddspu}=22,4.0,1+0,5-22,4.0,1=0,5\left(l\right)\)
\(C_{M_{FeSO_4}}=\frac{0,1}{0,5}=0,2\left(M\right)\)
\(C_{M_{CuSO_4}}=\frac{\left(2.0,5\right)-0,1}{0,5}=1,8\left(M\right)\)
Đúng 0
Bình luận (0)
Xem thêm câu trả lời
Nhúng một thanh nhôm nặng 25g vào 200ml dung dịch CuSO4 0,5M. Sau một thời gian cân lại thanh nhôm thấy nặng 25,96g. Tính nồng độ mol của các chất có trong dung dịch sau phản ứng.
Nhúng một thanh kẽm và một thanh sắt vào cùng một dung dịch CuSO4. Sau một thời gian lấy 2 thanh kim loại ra thấy trong dung dịch còn lại có nồng độ mol ZnSO4 bằng 2,5 lần nồng độ FeSO4. Mặt khác khối lượng dung dịch giảm 2,2 gam. Khối lượng Cu bám lên kẽm và bám lên sắt lần lượt là: A. 64g; 25,6g B. 32g; 12,8g C. 64g; 12,8g D. 32g; 25,6g
Đọc tiếp
Nhúng một thanh kẽm và một thanh sắt vào cùng một dung dịch CuSO4. Sau một thời gian lấy 2 thanh kim loại ra thấy trong dung dịch còn lại có nồng độ mol ZnSO4 bằng 2,5 lần nồng độ FeSO4. Mặt khác khối lượng dung dịch giảm 2,2 gam. Khối lượng Cu bám lên kẽm và bám lên sắt lần lượt là:
A. 64g; 25,6g
B. 32g; 12,8g
C. 64g; 12,8g
D. 32g; 25,6g

Theo (1) có khối lượng Cu bám vào: mCu = 0,4.2,5.64 = 64 (gam)
Theo (2) có khối lượng Cu bám vào: mCu = 0,4.64 =25,6 (gam).
Đáp án A
Đúng 0
Bình luận (1)
Nhúng thanh sắt có khối lượng 50g vào 500ml dung dịch CuSO4. Sau một thời gian khối lượng thanh sắt tăng a% và có 0,64 gam Cu sinh ra .Xác định a và nồng độ mol/lít của dung dịch CuSO4. Coi thể tích dung dịch thay đổi không đáng kể
Help meeeee!!!!!
nCu= \(\frac{0,64}{64}\) = 0,01 mol
PTHH:
Fe + CuSO4 → FeSO4 + Cu↓
0,01___0,01_____________0,01
\(\text{m t h a n h s ắ t t ă n g = 0,01 . (64- 56)=0,08 g}\)
a=\(\frac{0,08}{50}\).100%=0,16 %'
\(CM_{CuSO4}=\frac{0,01}{0,5}=0,02M\)
Nhúng một thanh nhôm nặng 25 gam vào 200 ml dung dịch CuSO4 0,5M. Sau một thời gian, cân lại thanh nhôm thấy cân nặng 25,69 gam. Tính nồng độ mol của các chất có trong dung dịch sau phản ứng.
Al: 25 gam + 0,1 mol CuSO4 → thanh nhôm nặng 25,69 gam.
2Al + 3CuSO4 → Al2(SO4)3 + 3Cu
Sau phản ứng mtăng = 25,69 - 25 = 0,69 gam
=> \(n_{Al} = 2. \dfrac{0,69}{3 .64 - 2 . 27} = 0,01 mol\)
=> nAl2(SO4)3 = 0,005 mol; nCuSO4dư = 0,1 - 0,015 = 0,085 mol
=> CM Al2(SO4)3= 0,025 M; CM CuSO4 = 0,425 M
Đúng 2
Bình luận (0)
Nhúng một thanh nhôm nặng 25 gam vào 200 ml dung dịch
C
u
S
O
4
0,5M. Sau một thời gian, cân lại thanh nhôm thấy cân nặng 25,69 gam. Nồng độ mol của
C
u
S
O
4
và
A
l
2
S
O
4
trong dung dịch sau phản ứng lần lượt là...
Đọc tiếp
Nhúng một thanh nhôm nặng 25 gam vào 200 ml dung dịch C u S O 4 0,5M. Sau một thời gian, cân lại thanh nhôm thấy cân nặng 25,69 gam. Nồng độ mol của C u S O 4 và A l 2 S O 4 trong dung dịch sau phản ứng lần lượt là
A. 0,425M và 0,2M
B. 0,425M và 0,3M
C. 0,4M và 0,2M
D. 0,425M và 0,025M.
n C u S O 4 = 0,5.0,2 = 0,1 mol
2 A l + 3 C u S O 4 → A l 2 S O 4 3 + 3 C u
2x……3x……..x……3x (Mol)
Theo bài ta có:
m C u b á m v à o - m A l tan = m A l t ă n g
⇔ 3x.64 - 2x.27 = 25,69 - 25
⇔ 138x = 0,69
⇔ x = 0,005 mol
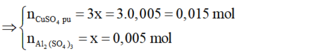

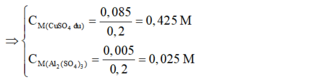
⇒ Chọn D.
Đúng 0
Bình luận (0)
Bài 2: Nhúng một thanh nhôm nặng 25 gam vào 200 ml dung dịch CuSO4 0,5M. Sau một thời gian, cân lại thanh nhôm thấy cân nặng 25,69 gam. Nồng độ mol của CuSO4 và Al2 (SO4)3 trong dung dịch sau phản ứng lần lượt là?
\(2Al+3CuSO_4\rightarrow Al_2\left(SO_4\right)_3+3Cu\\ Đặt:n_{Al\left(pứ\right)}=x\left(mol\right)\\ m_{tăng}=m_{Cu\left(sinhra\right)}-m_{Al\left(pứ\right)}=\dfrac{3}{2}x.64-x.27=25,69-25\\ \Rightarrow x=0,01\left(mol\right)\\ \Rightarrow n_{CuSO_4\left(dư\right)}=0,2.0,5-0,01.\dfrac{3}{2}=0,085\left(mol\right)\\ n_{Al_2\left(SO_4\right)_3}=0,01\left(mol\right)\\ CM_{Al_2\left(SO_4\right)_3}=\dfrac{0,01}{0,2}=0,05\left(M\right)\\ CM_{CuSO_4\left(dư\right)}=\dfrac{0,085}{0,2}=0,475M\)
Đúng 3
Bình luận (0)
nCuSO4= 0,5.0,2 = 0,1 mol
2Al+3CuSO4→Al2(SO4)3+3Cu
2x……3x……..x……3x (Mol)
Theo bài ta có:
mCu bámvào−mAl tan=mAl tăng
⇔ 3x.64 - 2x.27 = 25,69 - 25
⇔ 138x = 0,69
⇔ x = 0,005 mol
*Tham khảo
Đúng 4
Bình luận (2)