cho 12 lít hỗn hợp khí cl2 và h2 vào bình kín chiếu sáng thu đc hh khí chứa 30 %thể tích là khí sản phẩm, lượng cl còn dư 20 % so với ban đầu các khí ở cùng đk
b)tính hiệu suất phản ứng
Một bình thủy tinh có chứa 16 Cl2 và H2 . Chiếu sáng để phản ứng xảy ra thì thu đc một hỗn hợp khí chứa 30% thể tích là khí sản phẩm, lượng Cl2 còn 20% so với ban đầu ( các khí đo ở cùng nhiệt độ , điều kiện và áp suất)
a) Tính % thể tích các khí trước và sau phản ứng
b) Tính hiệu suất phản ứng
•๖ۣۜK๖ۣۜO☠๖ۣۜC๖ۣۜHẤ๖ۣۜP☠๖ۣۜN๖ۣۜHẬ๖ۣۜN☠๖ۣۜBÀ๖ۣۜI☠๖ۣۜC๖ۣۜHÉ๖ۣۜP☠๖ۣۜMẠ๖ۣۜN๖ۣۜG☠๖ۣۜN๖ۣۜH๖ۣۜA•
︵✿๖ۣۜHÓ๖ۣۜA☠๖ۣۜN๖ۣۜH๖ۣۜA‿✿
PTHH
Cl2 + H2 -> 2 HCl
=> Sau pư thể tích vẫn là 16 l
Gọi x là VCl2 (l)
Theo bài ra , VCl2 = 20% x = 0,2x(l)
PTHH Cl2 + H2 -> 2HCl
Trước x 16-x ( l )
Trong 0,8x 0,8x 1,6x ( l )
Sau 0,2x 16-1,8x ( l )
Theo bài ra ta có
VHCl = 30% . 16 = 4,8 l
(=) 1,6x = 4,8 => x= VCl2 = 3l
VH2 = 16- 2 = 14 /
%VCl2= 2/16 . 100% = 18,75%
%vH2 =14/16 .100% = 81,25%
Sau pư
VCl2 = 0,2 . 3 = 0,6 l
VH2 = 16-1,8.3= 10,6 l
%VCl2 = 0,6/16 . 100% = 3,75%
%VH2 = 10,6/16 . 100% = 66,25%
%VHCl = 30%
Vì VCl2 < VH2 pư
=> H tính theo Cl2
H= nCl2 pư / nCl2 ban đầu .100% = 2,4/3 . 100% = 80%
so sánh kết quả nha các bn mình lm đc thế thôi
Cho 1,2 lít hỗn hợp gồm hiđro và clo vào bình thủy tinh đậy kín và chiếu sáng bằng ánh sang khếch tán. Sau một thời gian, ngừng chiếu sáng thì thu được một hỗn hợp khí chứa 30% hiđroclorua về thể tích và hàm lượng clo ban đầu đã giảm xuống còn 20% so với lượng clo ban đầu. Thành phần phần trăm thể tích của hiđro trong hỗn hợp ban đầu bằng:
A. 66,25%
B. 30,75%
C. 88,25%
D. 81,25%
Hỗn hợp chất rắn A gồm FeCO3, FeS2 và tạp chất trơ. Hỗn hợp khí B gồm 20% oxi và 80% nitơ về thể tích. Cho hỗn hợp A vào bình kín dung tích 10 lít ( không đổi) chứa lượng hỗn hợp B vừa đủ. Nung nóng bình cho các phản ứng xảy ra hoàn toàn, các phản ứng cùng tạo ra một oxit sắt, oxit này phản ứng với dung dịch HNO3 dư không tạo ra khí. Sau phản ứng, đưa nhiệt độ bình về 136,50C, trong bình còn lại chất rắn X và hỗn hợp khí Y. Tỉ khối của Y so với H2 bằng 17 và áp suất trong bình là P atm. Cho dòng khí CO dư đi qua X đun nóng, biết rằng chỉ xảy ra phản ứng khử oxit sắt thành kim loại và đạt hiệu suất 80%.Sau phản ứng thu được 27,96 gam chất rắn Z, trong đó kim loại chiếm 48,07% khối lượng.
(a) Tính giá trị của P ( coi thể tích chất rắn X là rất nhỏ) và thành phần % khối lượng tạp chất trong A.
(b) Cho Y phản ứng với oxi ( dư) có V2O5 ( xúc tác) ở 4500C, hấp thụ sản phẩm vào 592,8 gam nước, được dung dịch C ( D = 1,02 gam/ml). Tính nồng độ mol của dung dịch C. Giả thiết hiệu suất của quá trình là 100%.


a) Gọi số mol của FeCO3: x (mol) ;
số mol của FeS2: y (mol)
4FeCO3 + O2 → Fe2O3 + 4CO2↑
x → 0,25x → x (mol)
4FeS2 +11O2 → 2Fe2O3 + 8SO2↑
y → 2,75y → 2y (mol)
∑ nO2 = 0,25x + 2,75y (mol)
Cùng điều kiện về nhiệt độ và áp suất nên tỉ lệ về thể tích = tỉ lệ về số mol
=> nN2 = 4nO2 = 4(0,25x + 2,75y)
=> nN2 = x + 11y (mol)
Vậy hỗn hợp Y gồm:

Khối lượng Fe có trong Z là:

Vì H = 80% => nFe2O3 (trong X) = 0,12. 100% : 80% = 0,15 (mol)
nFe2O3 dư (trong Z) = 0,15 – 0,12 = 0,03 (mol)
Khối lượng tạp chất trong Z = 27,96 – mFe – mFe2O3 dư = 27,96 – 0,24.56 – 0,03.160 = 9,72 (g)
Bảo toàn nguyên tố Fe => nFeCO3 + nFeS2 = 2nFe2O3(trong X)
=> x + y = 0,3 (2)
Từ (1) và (2) => x = 0,18 và y = 0,12 (mol)
Áp dụng công thức PV = nRT ( với n = nCO2 + nSO2 + nN2 = 0,18 + 2. 0,12 + 0,18 +11.0,12 = 1,92)
=> P.10 = 1,92.0,082. (136,5 +273)
=> P = 6,447 ( atm) ≈ 6,5 (atm)
Ta có: mA = mFeCO3 + mFeS2 + mtạp chất = 0,18.116 + 0,12.120 + 9,72 = 45 (g)
![]()
b) hỗn hợp Y gồm:

Cho hỗn hợp Y qua O2 ( xúc tác V2O5 ) có phản ứng sau:

Khối lượng dd sau: mdd sau = mSO3 + mH2O = 0,24. 80 + 592,8 = 612 (g)

TD 5: cho 4 lít N2 và 14 lít H2 vào bình kín rồi nung nóng với xúc tác thích hợp để phản ứng xảy ra , sau phản ứng thu được 16,4 lít hỗn hợp khí ( các khí đo ở cùng đều kiện về nhiệt độ và áp suất)
a. Tính thể tích khí amoniac thu được
b. Xác định hiệu suất của phản ứng.
a) PTHH: N2+ 3H2 ⇌ 2NH3
Ở cùng điều kiện thì tỉ lệ về thể tích chính là tỉ lệ về số mol
Đặt thể tích N2 phản ứng là x (lít)
=> VH2 pứ= 3x (lít) , VNH3 sinh ra=2x (lít)
VN2 dư= 4-x (lít), VH2 dư= 14-3x (lít)
Sau phản ứng thu được N2 dư, H2 dư, NH3
Tổng thể tích khí thu được sau phản ứng là:
V khí= VH2 dư+ VN2 dư+ VNH3= 14-3x + 4-x+ 2x= 16,4
=> x=0,8 lít
=>VNH3 sinh ra= 2x = 2.0,8 =1,6 (lít)
b)Do \(\dfrac{4}{1}< \dfrac{14}{3}\) =>Hiệu suất tính theo N2
=>H=\(\dfrac{V_{N_2\left(pứ\right)}}{V_{N_2\left(bđ\right)}}\)⋅100=\(\dfrac{0,8}{4}.100\)=20%
Cho 4 lít N2 và 12 lít H2 vào bình kín để thực hiện phản ứng tổng hợp NH3. Biết hiệu suất phản ứng là 25%, hỗn hợp thu được sau phản ứng có thể tích là bao nhiêu (các thể tích khí đo trong cùng điều kiện)?
A. 12 lít
B. 14 lít
C. 16 lít
D. 18 lít
N2+ 3H2 ⇌ 2NH3
Ở cùng điều kiện thì tỉ lệ về thể tích chính là tỉ lệ về số mol
Do hiệu suất phản ứng là 25% nên
VN2 pứ= 4.25%= 1 lít; VH2 pứ= 12.25%= 3 lít;
VNH3 sinh ra= 2VN2 pứ= 2 lít
VN2 dư= 4-1=3 lít, VH2 dư= 12-3=9 lít
Hỗn hợp thu được sau phản ứng có thể tích là
V= VN2 dư+ VH2 dư+ VNH3 sinh ra= 3 +9+2=14 lít
Đáp án B
Cho 3 lít Cl2 phản ứng với 2 lít H2; hiệu suất phản ứng đạt 80%. Phần trăm thể tích Cl2 trong hỗn hợp khí sau phản ứng là (các thể tích khí được đo ở cùng điều kiện t0, p)
A. 28%
B. 64%
C. 60%
D. 8%
Đáp án A
Các thể tích đo trong cùng điều kiện nhiệt độ và áp suất, nên thể tích cũng là số mol
H2 + Cl2 → 2HCl
Ban đầu 2 3
Phản ứng 2.0,8 1,6 3,2
Sau phản ứng 0,4 1,4 3,2 => nsau phản ứng = 0,4 + 1,4 + 3,2 = 5
![]() .100 = 28%
.100 = 28%
Cho 3 lít Cl2 phản ứng với 2 lít H2; hiệu suất phản ứng đạt 80%. Phần trăm thể tích Cl2 trong hỗn hợp khí sau phản ứng là: (các thể tích khí được đo ở cùng điều kiện t0, p)
A. 28%.
B. 64%
C. 60%
D. 8%
Crackinh pentan một thời gian thu được 1,792 lít hỗn hợp X gồm 8 hiđrocacbon và H2. Thêm 4,48 lít khí H2 vào X rồi nung với Ni đến phản ứng hoàn toàn thu được 5,6 lít hỗn hợp khí Y (thể tích khí đều đo ở đktc). Đốt cháy hoàn toàn Y rồi cho sản phẩm cháy hấp thụ vào dung dịch nước vôi trong dư, sau khi các phản ứng xảy ra hoàn toàn, khối lượng dung dịch thay đổi như thế nào so với ban đầu ?
A. tăng 5,0 gam.
B. giảm 6,76 gam.
C. giảm 5,0 gam.
D. tăng 6,76 gam.
Đáp án C
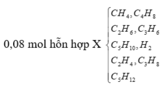
![]()
Vì phản ứng xảy ra hoàn toàn mà nanken < 0,08 nên hỗn hợp Y chứa ankan và H2 dư
→ nanken = 0,2 + 0,08- 0,25 = 0,03 mol
→ nankan (CH4, C2H6+ C3H8+ C5H12 dư) + H2 = 0,08- 0,03= 0,05
→ ∑ nC5H12 ban đầu = 0,05 mol
Đốt cháy hoàn toàn Y tương đương đốt cháy 0,05 mol C5H12 và 0,2 mol H2
→ nCO2 = 0,25 mol, nH2O = 0,05.6 + 0,2 = 0,5 mol
→ mdd = 0,25. 44 + 0,5.18-0,25. 100 = -5 gam .
Vậy dung dịch giảm 5 gam
Cho 4,0 lít N2 và 14,0 lít H2 vào một bình kín rồi nung nóng với xúc tác thíc hợp( Các khí đo ở cùng điều kiện về nhiệt đọ và áp suất).
a) Tính thể tích khí ammoniac ( NH3) thu được.
b. Xác định hiệu suất của phản ứng