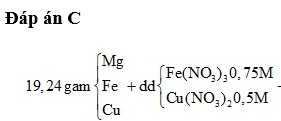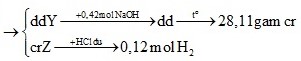Cho 14,24 gam hỗn hợp X gồm 3 Kl AL,Fe và Ag ở dạng bột td với dd HCL dư thoát ra 8.96 lít H2 (dktc).Đem lọc thu được 3,24g chất rắn . Tính Khối Lượng mỗi kl có trong trường hợp

Những câu hỏi liên quan
huhu ai giúp em với, e cần gấp, tks 1. Cho 14,24 gam hỗn hợp X gồm 3 kim loại Al, Fe, Ag ở dạng bột tác dụng vs dd HCl dư thoát ra 8,96 lít H2 (đktc), đem lọc rửa thu đc 3,24 gam chất rắn B, Viết phương trình hóa học và tính khối lượng mỗi kim loại có trog hỗn hợp2. Cho 2,24 gam hỗn hợp 2 oxit dạng bột là ZnO và Fe2O3. Dùng V lít (đktc) khí CO để khử hoàn toàn 2 oxit thành kim loại thì thu đc 1,86 gam hỗn hợp 2 kim loại. Xác định thể tích khí CO tối thiểu cần dùngE cảm ơn nhiều ạ, giúp e vs nhaa...
Đọc tiếp
huhu ai giúp em với, e cần gấp, tks ![]()
1. Cho 14,24 gam hỗn hợp X gồm 3 kim loại Al, Fe, Ag ở dạng bột tác dụng vs dd HCl dư thoát ra 8,96 lít H2 (đktc), đem lọc rửa thu đc 3,24 gam chất rắn B, Viết phương trình hóa học và tính khối lượng mỗi kim loại có trog hỗn hợp
2. Cho 2,24 gam hỗn hợp 2 oxit dạng bột là ZnO và Fe2O3. Dùng V lít (đktc) khí CO để khử hoàn toàn 2 oxit thành kim loại thì thu đc 1,86 gam hỗn hợp 2 kim loại. Xác định thể tích khí CO tối thiểu cần dùng
E cảm ơn nhiều ạ, giúp e vs nhaaaaaaaaaaaaaaaaaaaaaaaaaaa![]()
câu 4: (3,0 điểm) hỗn hợp kim loại x gồm fe, al, ag ở dạng bột. chia 24,5 gam x làm 2 phần không bằng nhau: - hoà tan phần (i) trong dung dịch hcl dư, có 4,928 lít h2 (đktc) thoát ra. - cho phần (ii) vào 660ml dung dịch cuso4 0,5m ( phản ứng xảy ra vừa đủ) thu được dung dịch y chứa 39,9 gam chất tan và m gam chất rắn z. a. tính khối lượng của phần (i) b. tính m.
\(n_{H_2}=\dfrac{4,928}{22,4}=0,22mol\)
\(n_{CuSO_4}=0,66.0,5=0,33mol\)
- Gọi số mol trong phần I là :Fe(x mol), Al(y mol), Ag(z Mol)
- Sỗ mol mỗi kim loại trong phần II: Fe(tx mol), Al(ty mol), Ag(tz Mol)
56(x+tx)+27(y+ty)+108(z+tz)=24,5(*)
- Phần I: Fe+2HCl\(\rightarrow\)FeCl2+H2(1)
2Al+6HCl\(\rightarrow\)2AlCl3+3H2(2)
x+1,5y=0,22(**)
- Phần II: Fe+CuSO4\(\rightarrow\)FeSO4+Cu(3)
2Al+3CuSO4\(\rightarrow\)Al2(SO4)3+3Cu(4)
tx+1,5ty=0,33(***)
152tx+171ty=39,9(****)
- Kết hợp(***) và(****) : tx=0,06, ty=0,18
\(y=3x\)(*****)
- kết hợp (**) và (*****) ta có: x=0,04, y=0,12
\(\rightarrow t=\dfrac{0,06}{0,04}=1,5\)
- Thay x=0,04 ,y=0,12 , t=1,5 vào (*) ta có z=0,04
mI=56x+27y+108z=56.0,04+27.0,12+108.0,04=9,8 gam
số mol Cu=tx+1,5ty=0,33 mol
chất rắn Z gồm 0,33 mol Cu và tz=0,04.1,5=0,06 mol Ag
mZ=0,33.64+0,06.108=27,6 gam
Đúng 0
Bình luận (0)
Hoà tan m gam hỗn hợp gồm 2 kim loại là Al và Fe trong dung dịch HCl dư thu được dd B và 14,56 lít H2 đktc . Cho dd B tác dụng với dd NaOH dư , kết tủa đem nung ngoài kk đến khối lượng không đổi được 16 gam chất rắn . Tính m
cho một lương ag al tác dụng với dd h2so4 dư thu được 6 72 lít khí thoát ra ngoài ở dktc. sau pu còn lại 4 6g chất rắn không tan. xác định % về khối lượng mỗi kl ban đầu
cho một lương ag al tác dụng với dd h2so4 dư thu được 6 72 lít khí thoát ra ngoài ở dktc. sau pu còn lại 4 6g chất rắn không tan. xác định % về khối lượng mỗi kl ban đầu
Cho 4,14g hỗn hợp gồm Fe và Al vào dd HCl dư sau phản ứng thu được 3,024lít khí ở DKTC và dd B
a. Viết ptrinh phản ứng
b. Tính thành phần trăm khối lượng mỗi kim loại trong hỗn hợp ban đầu
c. Cho dd B tác dụng với dd NaOH dư, lọc kết tủa đem nung trong không khí đến khi khối lượng không đổi thu được m gam chất rắn.tính m
Xem chi tiết
a) PTHH: \(Fe+2HCl\rightarrow FeCl_2+H_2\) (1)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\) (2)
b) Ta có: \(\Sigma n_{H_2}=\dfrac{3,024}{22,4}=0,135\left(mol\right)\)
Gọi số mol của Fe là \(a\) \(\Rightarrow n_{H_2\left(1\right)}=a\)
Gọi số mol của Al là \(b\) \(\Rightarrow n_{H_2\left(2\right)}=\dfrac{3}{2}b\)
Ta lập được hệ phương trình:
\(\left\{{}\begin{matrix}a+\dfrac{3}{2}b=0,135\\56b+27b=4,14\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}a=0,045\\b=0,06\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}m_{Fe}=0,045\cdot56=2,52\left(g\right)\\m_{Al}=1,62\left(g\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Fe}=\dfrac{2,52}{4,14}\cdot100\%\approx60,87\%\\\%m_{Al}=39,13\%\end{matrix}\right.\)
c) PTHH: \(FeCl_2+2NaOH\rightarrow2NaCl+Fe\left(OH\right)_2\downarrow\)
\(AlCl_3+3NaOH\rightarrow Al\left(OH\right)_3\downarrow+3NaCl\)
\(4Fe\left(OH\right)_2+O_2\underrightarrow{t^o}2Fe_2O_3+4H_2O\)
\(2Al\left(OH\right)_3\underrightarrow{t^o}Al_2O_3+3H_2O\)
Theo các PTHH: \(\left\{{}\begin{matrix}n_{Fe\left(OH\right)_2}=n_{FeCl_2}=0,045mol\\n_{Al\left(OH\right)_3}=n_{AlCl_3}=0,06mol\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}n_{Fe_2O_3}=0,0225mol\\n_{Al_2O_3}=0,03mol\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}m_{Fe_2O_3}=0,0225\cdot160=3,6\left(g\right)\\m_{Al_2O_3}=0,03\cdot102=3,06\left(g\right)\end{matrix}\right.\)
\(\Rightarrow m_{chấtrắn}=3,06+3,6=6,66\left(g\right)\)
Đúng 1
Bình luận (0)
Cho hỗn hợp A có khối lượng là 32,8 gồm ( Al, Fe, Cu) tác dụng với dung dịch NaOH thì thu được 6,72 lít khí H2 thoát ra ở đktc. Nếu đem hỗn hợp trên tác dụng với dung dịch HCl thì sinh ra 10,08 lít khí H2 thoát ra ở đktc. Tính % khối lượng mỗi kim loại trong hỗn hợp.
2Al + 2H2O + 2NaOH→ 3H2 + 2NaAlO2
0,2mol 0,3mol
mAl=0,2.27=5,4g
2Al + 6HCl→ 2AlCl3+ 3H2
0,2mol 0,3mol
Fe + 2HCl→ FeCl2+ H2
0,15mol 0,45-0,3 mol
mFe=0,15.56=8,4g
mCu=32,8-(6,4+8,4)=18g
%mFe=\(\frac{8,4}{32,8}.100=25,6\%\)
%mCu=\(\frac{18}{32,8}.100=54,8\%\)
%mAl=19,6%
Đúng 1
Bình luận (0)
Cho 2,44 gam hỗn hợp A gồm 3 kim loại Mg , Fe , và Cu ( ở dạng bột ) vào dung dịch loãng có chứa 0,05 mol H2SO4 . Sau khi phản ứng xảy ra hoàn toàn , thấy thoát ra 0,784 lít khí H2 ( đktc) và hỗn hợp B . Đem lọc , rửa B thu được 1,28 gam chất rắn
a, Viết phương trình các phản ứng xảy ra .
b, Tính % khôid lượng mỗi kim loại có trong hỗn hợp A
a)
$Mg + H_2SO_4 \to MgSO_4 + H_2$
$Fe + H_2SO_4 \to FeSO_4 + H_2$
b) Chất rắn không tan là Cu $\Rightarrow m_{Cu} = 1,28(gam)$
Gọi $n_{Mg} = a(mol) ; n_{Fe} = b(mol) \Rightarrow 24a + 56b + 1,28 = 2,44(1)$
Theo PTHH :
$n_{H_2} = a + b = \dfrac{0,784}{22,4} = 0,035(2)$
Từ (1)(2) suy ra : a = 0,025 ; b = 0,01
$\%m_{Mg} = \dfrac{0,025.24}{2,44}.100\% = 24,6\%$
$\%m_{Fe} = \dfrac{0,01.56}{2,44}.100\% = 23\%$
$\%m_{Cu} = 100\% - 24,6\% - 23\% = 52,4\%$
Đúng 1
Bình luận (0)
Cho 19,24 gam hỗn hợp gồm Mg, Fe, Cu vào dung dịch chứa
F
e
N
O
3
3
0,75M và
C
u
N
O
3
3
0,5M. Sau khi kết thúc phản ứng thu được dung dịch Y có chứa 2 muối và 20,56 gam chất rắn Z. Cho 350 ml dung d...
Đọc tiếp
Cho 19,24 gam hỗn hợp gồm Mg, Fe, Cu vào dung dịch chứa F e N O 3 3 0,75M và C u N O 3 3 0,5M. Sau khi kết thúc phản ứng thu được dung dịch Y có chứa 2 muối và 20,56 gam chất rắn Z. Cho 350 ml dung dịch NaOH 1,2M vào dung dịch Y, lọc bỏ kết tủa, cô cạn dung dịch nước lọc, lấy phần rắn đem nung đến khối lượng không đổi thu được 28,11 gam chất rắn khan. Cho dung dịch HCl dư vào rắn Z thấy thoát ra 2,688 lít khí H 2 (đktc). Phần trăm khối lượng của Mg có trong hỗn hợp X gần nhất với
A. 14,1%
B. 13,5%
C. 13,1%
D. 13,3%