nung nóng hỗn hợp 5,4g bột nhôm(Al) và 6,4g bột lưu huỳnh trong ống kín
a/ hỏi sau phản ứng còn dư chất nào bao nhiêu gam
b/ tính khối lượng Al2S3
Nung Nóng Một Hỗn Hợp Gồm 8,1 G Bột Nhôm (al ) Và 9.6G Bột Lưu Huỳnh (S) Cho Phản Ứng Sảy Thu Dc Hoàn Toàn Là Nhôm Sunfua (Al2S3)..Tinh Khối Lượng Nhôm Sunfua Thu Đc???
PTHH: 2Al + 3S ===> Al2S3
=> nAl = 8,1 / 27 = 0,3 mol
=> nS = 9,6 / 32 = 0,3 mol
Lập tỉ lệ ===> Al dư, S hết
=> nAl(pứ) = 0,2 mol
=> mAl(pứ) = 0,2 x 27 = 5,4 gam
Áp dụng định luật bảo toàn khối lượng
=> mAl2S3 = 5,4 + 9,6 = 15 gam
mAl2S3=mAl+mS
mAl2S3=8,1+9,6=17,7
=>mAl2S3=17,7g
Theo địnhluật bảo toàn khối lượng ta có:
mAl + mS = mAl2S3
8,1 + 9,6 = mAl2S3
mAl2S3 = 17,7g
Trộn 10,8 gam bột nhôm và bột lưu huỳnh dư . Cho hỗn hợp vào ống nghiệm và đun nóng để phản ứng xảy ra ta thu được 25,5 gam Al2S3 . Tính hiệu suất phản ứng ?
\(n_{Al_2S_3}=\dfrac{25.5}{150}=0.17\left(mol\right)\)
\(n_{Al}=\dfrac{10.8}{27}=0.4\left(mol\right)\)
\(2Al+3S\underrightarrow{^{t^0}}Al_2S_3\)
\(0.34...........0.17\)
\(H\%=\dfrac{0.34}{0.4}\cdot100\%=85\%\)
n Al2S3 = 25,5/150=0,17(mol)
$2Al + 3S \xrightarrow{t^o} Al_2S_3$
n Al = 2n Al2S3 = 0,34(mol)
H = 0,34.27/10,8 .100% = 85%
Câu 2: Trộn 10,8 g bột nhôm với bột lưu huỳnh dư. Cho hỗn hợp vào ống nghiệm và đun nóng để phản ứng xảy ra thu được 25,5 g Al2S3. Tính hiệu suất phản ứng ?
\(n_{Al_2S_3}=\dfrac{25,5}{150}=0,17\left(mol\right)\)
PTHH: 2Al + 3S --to--> Al2S3
0,34<----------0,17
=> \(H\%=\dfrac{0,34.27}{10,8}.100\%=85\%\)
Bạn có thể giúp mình hok 😥 khó quá chắc bạn đã làm qua r giúp với
1/1 hỗn hợp có 16 gam bột lưu huỳnh và 28 gam bột sắt.Đốt nóng hỗn hợp thu được chất thu được là Sắt(II)sunfua
Viết PTHH của phản ứng;tính khối lượng của sản phẩm
2/Hợp chất nhôm sunfua có thành phần 64%S và 36%Al
a-Tìm CTHH của hợp chất trên
Viết PTHH tạo thành nhômsunfua từ 2 chất ban đầu là nhôm và lưu huỳnh
b-Cho 5,4 gam nhôm tác dụng với 10 gam lưu huỳnh. Tính khối lượng hợp chất tạo thành và khối lượng chất còn dư sau phản ứng nếu có
Bài 1 mk ko chắc lắm nha b.B nào biết chắc đáp án đúng thì chỉ mk nha.
Đun nóng một hỗn hợp gồm có 0,650g bột kẽm và 0,224g bột lưu huỳnh trong ống nghiệm đậy kín không có không khí. Sau phản ứng, người ta thu được chất nào trong ống nghiệm? Khối lượng là bao nhiêu?
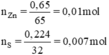
⇒ S phản ứng hết, Zn phản ứng dư
Phương trình hóa học của phản ứng
Zn + S 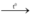 ZnS
ZnS
nZn phản ứng = 0,007 mol ⇒ nZnS = 0,007 mol.
Khối lượng các chất sau phản ứng:
mZn dư = (0,01 – 0,007) × 65 = 0,195g.
mZnS = 0,007 × 97 = 0,679g.
\(n_{Al} = \dfrac{5,4}{27} = 0,2(mol)\\ n_S = \dfrac{6,4}{32} = 0,2(mol)\)
2Al + 3S \(\xrightarrow{t^o}\) Al2S3
\(\dfrac{2}{15}\).......0,2..........\(\dfrac{1}{15}\)..........(mol)
Sau phản ứng :
\(m_{Al_2S_3} = \dfrac{1}{15}150 = 10(gam)\\ m_{Al\ dư} = (0,2 - \dfrac{2}{15}).27 = 1,8(gam)\)
dùng định luật bảo toàn khối lượng thì sẽ có khối lượng sản phẩm bằng tổng khối lượng các chất tham gia
Trộn 10g bột nhôm với bột lưu huỳnh dư , cho hỗn hợp vào ống nghiệm và đun nóng để phản ứng xảy ra thu được 25,5 gam Al2S3 . Tính hiệu suất phản ứng
cố gắng giúp mik bằng cách M lý thuyết và M thực tế nhé , mik cảm ơn :)))))))
nAl=10/27(mol)
ta ccó pthh: 2Al+3S->Al2S3( nhiệt dộ cao)
theo ptth=> nAl2S3(lý thuyết)=1/2.nAl=\(\dfrac{1}{2}.\dfrac{10}{27}\)=\(\dfrac{5}{27}\)(mol)
=> mAl2S3(lý thuyết)=\(\dfrac{5}{27}.150=\dfrac{250}{9}\)(g)
=>H=\(\dfrac{mAL2S3\left(thucte\right)}{mAL2S3\left(lythuyet\right)}.100\%=\dfrac{25,5}{\dfrac{250}{9}}=91,8\%\)
\(n_{Al}=\dfrac{10}{27}\left(mol\right)\)
\(2Al+3S\underrightarrow{^{t^0}}Al_2S_3\)
\(\dfrac{10}{27}...........\dfrac{5}{27}\)
\(m_{Al_2S_3\left(lt\right)}=\dfrac{5}{27}\cdot150=\dfrac{250}{9}\left(g\right)\)
\(H\%=\dfrac{m_{tt}}{m_{lt}}\cdot100\%=\dfrac{25.5}{\dfrac{250}{9}}\cdot100\%=91.8\%\)
Nung nóng hỗn hợp 5,4 gam cột nhôm và 6,4 gam cột lưu huỳnh
a) Hỏi sau phản ứng chất nào còn dư và còn bao nhiêu gam
b) Tính số gam chất tạo thành Al2S3
a) nAl=\(\frac{m_{Al}}{M_{Al}}\)=\(\frac{5,4}{27}\)=0,2 mol
nS=\(\frac{m_S}{M_S}\)=\(\frac{6,4}{32}\)=0,2 mol
\(\frac{n_{Al\left(đb\right)}}{n_{Al\left(pt\right)}}\)=\(\frac{0,2}{4}\)=0,05 (1)
\(\frac{n_{S\left(đb\right)}}{n_{S\left(pt\right)}}\)=\(\frac{0,2}{6}\)=0,03 (2)
0,05>0,03
Từ (1)(2) => Al có dư.Tính theo S
PTHH:\(4Al+6S=>2Al_2S_3\)
nAl(p/ư)=\(\frac{0,2.4}{6}\)=0,13 mol
\(n_{Al_2S_3\left(p.ứ\right)}\)=\(\frac{0,2.2}{6}\)=0,06 mol
nAl(dư)=nAl(đb)-nAl(p/ứ)=0,2-0,13=0,07 mol
mAl(dư)=0,07.27=1,89g
b) \(M_{Al_2S_3}\)=27.2+32.3=150 g/mol
\(m_{Al_2S_3}\)=0,06.150=9g
Đun nóng một hỗn hợp gồm có 0,650 gam bột kẽm và 0,224 gam bột lưu huỳnh trong ống nghiệm đậy kín không có không khí.Sau phản ứng người ta thu được chất nào trong ống nghiệm ? Khối lượng là bao nhiêu ?
n Zn = 0,65/65 = 0,01 mol; n S = 0,224/32 = 0,007 mol
Zn + S → ZnS (1)
Theo (1) sau phản ứng trong ống nghiệm thu được:
n ZnS = 0,007 mol
m ZnS = 0,007x97 = 0,679 (g)
n Zn dư = (0,01 - 0,007) = 0,003 mol
m Zn dư = 65.0,003 = 0,195g