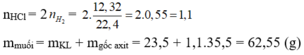Cho 0,297g hợp kim Na, Ba vào H2O thu được dd X, khí Y trung hòa dd cần 50ml HCl. Cô cạn dd thu được 0.4745 g muối. Tính thể tích Y(đktc), Cm HCl, tính lượng mỗi kim loại

Những câu hỏi liên quan
Cho 0,297g hỗn hợp kim loại Na, Ba tác dụng với H2O thu được dd X và khí Y . Trung hòa dd X cần 50ml HCl cô cạn thu được 0,4745g muối. Tính VY thoát ra ( đktc) , CM HCl . Tính lượng mỗi kim loại
\(\text{Gọi số mol của Na là x(mol)},\text{số mol của Ba là y(mol)}\)
\(\text{=> 23x +137y=0.297(1)}\)
PTPU với Hiđrô
2Na +2H2O -----> 2NaOH+ H2
x.................................. x..........x/2
Ba + 2H2O -------> Ba(OH)2 +2H2O
y.....................................y................2y
PTPU với HCl:
NaOH + HCl ------> NaCl +H2O
x................x.......................x (mol)
Ba(OH)2 +2HCl ----> BaCl2+2H2O
y.....................2y....................y (mol)
\(\text{m muối = 58,5x+208y=0,4745 (2) }\)
Giải hệ (1) và (2) => x=0,001 ; y=0,002
\(\text{V khí thoát ra= (0,001/2+0,002).22,4=0,056(l)}\)
\(\text{nHCl=0,001+0,002.2=0,005(mol)}\)
\(\text{CM HCl= 0,005/50=0,0001M}\)
\(\left\{{}\begin{matrix}\text{mNa=23.0,001=0,023(g)}\\\text{mBa =137.0,002=0,274(g)}\end{matrix}\right.\)
Cho hỗn hợp gồm 2 kim loại Na, K tác dụng với nước dư thu được dd A và 2.24 lít khí H đkc. Trung hòa dd A bằng dd HCL vừa đủ, cô cạn dd thu được 13.30 gam muối khan
a. Tính % khối lượng mỗi kim loại trong hỗn hợp đầu
b. Tính thể tích không khí đkc cần để đốt hết lượng H2 thu được từ thí nghiệm trên
Cho 0,297g kim loại Na và Ba tác dụng hết với H2O thu được dung dịch X và khí Y. để trung hòa dung dịch X cần 50ml dung dịch HCl 0,1M
a) tính thành phần % khối lượng mỗi kim loại
b) tính thể tích không khí cần dùng để đốt cháy hết khi Y biết thể tích O2= 20% thể tích không khí
nHCl=5.10-3 mol
2Na + 2H2O --> 2NaOH + H2
x mol x mol 1/2 mol
Ba + 2H2O --> Ba(OH)2 + H2
y mol y mol y mol
NaOH + HCl --> NaCl + H2O
x mol x mol
Ba(OH)2 + 2HCl--> BaCl2 + H2O
y mol 2y mol
Ta duoc: 23x + 137y =0,297 (1)
x + 2y =5.10-3 (2)
Tu (1) va (2) ta duoc => x= 10-3
=> y= 2.10-3
a/ mNa= 10-3.23=0,023g
mBa=2.10-3.137=0,274g
b/ nH2= 10-6 mol
H2 + O2 --> H2O
10-6 mol 10-6 mol
VO2= 10-6. 22,4=2,24.10-5 lit
VKK= 2,24.10-5.100/20=1,12.10-4 lit
Đúng 0
Bình luận (2)
1. Cho 0.297g hỗn hợp Na, Ba t/d hết với H2O đc dd X và khí Y. Trung hòa X cần 50ml dd HCl, cô cạn thu đc 0.4745g muối. Tính thể tích khí Y đktc, nồng độ mol HCl và khối lượng mỗi kim loại.
2. Cho 1 lượng Na, Ba t/d với H2O thoát ra 4.48 lít H2(đktc) và dd B. Trung hòa 1/2 B bằng HNO3 2M rồi cô cạn dd nhận đc 21.55g muối khan.
a)Tính thể tích HNO3 cần dùng và khối lượng mỗi kim loại
b) Tính % mỗi kim loại
Đọc tiếp
1. Cho 0.297g hỗn hợp Na, Ba t/d hết với H2O đc dd X và khí Y. Trung hòa X cần 50ml dd HCl, cô cạn thu đc 0.4745g muối. Tính thể tích khí Y đktc, nồng độ mol HCl và khối lượng mỗi kim loại.
2. Cho 1 lượng Na, Ba t/d với H2O thoát ra 4.48 lít H2(đktc) và dd B. Trung hòa 1/2 B bằng HNO3 2M rồi cô cạn dd nhận đc 21.55g muối khan.
a)Tính thể tích HNO3 cần dùng và khối lượng mỗi kim loại
b) Tính % mỗi kim loại
1. Gọi số mol Na, Ba lần lượt là x và y.
Ta có: 23x + 137y = 0,297.
Muối thu được sau PỨ là NaCl và BaCl2
=> 58,5x + 208y = 0,4745.
Từ đó => x = 0,001 và y = 0,002. => mNa = 0,001 . 23 = 0,023g và mBa = 0,002.137 = 0,274g.
Ta có: Na + H2O ---> NaOH + 1/2 H2
Ba + 2H2O ---> Ba(OH)2 + H2
=> VH2 = [(0,001. 1/2) + 0,002]. 22,4 = 0,056 l = 56 ml.
Mặt khác: nHCl = nNaCl + 2nBaCl2 (bảo toàn Cl) = 0,001 + 0,002.2 = 0,005 mol.
=> CM dd HCl =0,005: 0,05 = 0,1 M
Đúng 0
Bình luận (0)
2.
Gọi số mol Na là x và Ba là y
Ta có:
1/2 x + y = 4,48/22,4 = 0,2 và 85x/2 + 261y/2 = 21,55
=> x = 0,2 và y = 0,1
=> mNa = 0,2.23 = 4,6g và mBa = 0,1. 137 = 13,7g
nHNO3 = x/2 + y = 0,1 + 0,1 = 0,2 => VHNO3 = 0,2: 2 = 0,1 l
Đúng 0
Bình luận (0)
Hòa tan 8,9g hh X gồm 2 kim loại A và B bằng dd HCl dư thấy hh X tan hết, sau pư thu được dd Y và khí Z(đktc). Cô cạn dd Y thì thu được 23,1g chất rắn khan
a) Viết PTHH, tính thể tích khí Z
b) Thêm 50% lượng kim loại B trong X vào hh X, sau đó cũng hào tan bằng dd HCl dư thì thu được 5,6 lít Z (đktc), cô cạn dd sau pư thì thu được 27,85g chất rắn khan. Tìm kim loại A và B
a)
PTHH: 2A + 2nHCl --> 2ACln + nH2
2B + 2mHCl --> 2BClm + mH2
Gọi số mol H2 là a (mol)
=> nHCl = 2a (mol)
Theo ĐLBTKL: mkim loại + mHCl = mmuối + mH2
=> 8,9 + 36,5.2a = 23,1 + 2a
=> a = 0,2 (mol)
=> VH2 = 0,2.22,4 = 4,48 (l)
b)
\(n_{H_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
=> \(n_{H_2\left(tăng\right)}=0,25-0,2=0,05\left(mol\right)\)
PTHH: 2B + 2mHCl --> 2BClm + mH2
\(\dfrac{0,1}{m}\)<------------\(\dfrac{0,1}{m}\)<---0,05
Khối lượng rắn sau pư tăng lên do có thêm BClm sinh ra
=> \(m_{BCl_m}=\dfrac{0,1}{m}\left(M_B+35,5m\right)=27,85-23,1=4,75\left(g\right)\)
=> MB = 12m (g/mol)
Xét m = 2 thỏa mãn => MB = 24 (g/mol) => B là Mg
\(n_{Mg\left(thêm\right)}=\dfrac{0,1}{m}=\dfrac{0,1}{2}=0,05\left(mol\right)\)
=> \(n_{Mg\left(bđ\right)}=0,1\left(mol\right)\)
=> \(m_A=8,9-0,1.24=6,5\left(g\right)\)
PTHH: Mg + 2HCl --> MgCl2 + H2
0,1-------------------->0,1
2A + 2nHCl --> 2ACln + nH2
\(\dfrac{0,2}{n}\)<-------------------0,1
=> \(M_A=\dfrac{6,5}{\dfrac{0,2}{n}}=32,5n\left(g/mol\right)\)
Xét n = 2 thỏa mãn => MA = 65 (g/mol)
=> A là Zn
Đúng 1
Bình luận (0)
hh gồm kali và natri tác dụng hết với H2O cho 22,4l H2 ở đktc và dd B. Trung hòa dd B bằng HCl 0,5M rồi cô cạn dd thu được 13,3g muối khô.
a) Tính thể tích HCl đã dùng
b) Tính % khối lượng của mỗi kim loại
Hòa tan hỗn hợp Zn và Al tác dụng vs dd HCl thu được dd X và 8,96 lít khí thoát ra (đktc). Cô cạn dd X thu đc 40,3 gam muối khan, tính %khối lượng các kim loại
\(n_{Zn}=a\left(mol\right),n_{Al}=b\left(mol\right)\)
\(n_{H_2}=\dfrac{8.96}{22.4}=0.4\left(mol\right)\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
\(2Al+6HCl\rightarrow2AlCl_3+H_2\)
\(n_{H_2}=a+1.5b=0.4\left(mol\right)\left(1\right)\)
\(m_{Muối}=m_{ZnCl_2}+m_{AlCl_3}=136a+133.5b=40.3\left(g\right)\left(2\right)\)
\(\left(1\right),\left(2\right):a=0.1,b=0.2\)
\(m_{hh}=0.1\cdot65+0.2\cdot27=11.9\left(g\right)\)
\(\%Zn=\dfrac{0.1\cdot65}{11.9}\cdot100\%=54.62\%\)
\(\%Al=100-54.62=45.38\%\)
Đúng 2
Bình luận (1)
Cho 0,297g hỗn hợp Na, Ba vào H2O thu được dung dịch X và khí Y. Trung hòa dung dịch cần 50ml dung dịch HCl. Cô cạn dung dịch thu được 0,4745g muối.
a)Tính thể tích khí Y(đktc)
b)Tính nồng độ mol dung dịch HCl?
c)Tính khối lượng mỗi kim loại trong hỗn hợp.
Cho 23,5 g hỗn hợp 2 kim loại đứng trước H tác dụng vừa đủ với dd HCl thu được 12,32 lít H2 (đktc) và dd Y. Cô cạn dd Y thu được khối lượng muối khan là: A. 55,62 g B. 52,65 g C. 56,25 g D. 62,55 g
Đọc tiếp
Cho 23,5 g hỗn hợp 2 kim loại đứng trước H tác dụng vừa đủ với dd HCl thu được 12,32 lít H2 (đktc) và dd Y. Cô cạn dd Y thu được khối lượng muối khan là:
A. 55,62 g
B. 52,65 g
C. 56,25 g
D. 62,55 g