Một Oxít của Nitơ có dạng NxOy. Biết khối lượng của Nitơ trong phân tử chiếm 30,4 % ngoài ra cứ 1,15 g Oxít này chiếm thể tích 0,28 lít (đktc). Xác định công thức của Oxít.

Những câu hỏi liên quan
Một oxit của Nitơ có dạng NxOyNxOy. Biết khối lượng của Nitơ trong phân tử chiếm 30,4 % ngoài ra cứ 1,15 g oxit này chiếm thể tích 0,28 lít (đktc). Xác định công thức của oxit.
Đọc tiếp
Một oxit của Nitơ có dạng NxOyNxOy. Biết khối lượng của Nitơ trong phân tử chiếm 30,4 % ngoài ra cứ 1,15 g oxit này chiếm thể tích 0,28 lít (đktc). Xác định công thức của oxit.
Bình chọn giảm
Công thức oxit là NxOyNxOy
1,15 g oxit này chiếm thể tích 0,28 lít (đktc)
=>n oxit=0,28/22,4=0,0125 mol
=>M NxOyNxOy =1,15/0,0125=92
=>14x+16y=92(1)
% NN=14x/(14x+16y).100%=30,4%
=>14x=0,304.92=28
=>x=2
thay vào(1)=>y=4
=> oxit Nitơ là N2O4
Đúng 0
Bình luận (0)
b ơi 0,304 lấy đâu ra vậy . Chỉ m chút m chưa hiểu lắm hihi
Đúng 0
Bình luận (2)
1. Cho 10 lít khí H2 tác dụng với 6,72 lít Cl2 (đktc). Tính khối lượng của HCl thu được, biết hiệu suất phản ứng là 60% và mất mát là 5%.
2. Một Oxít của Nitơ có dạng NxOy. Biết khối lượng của Nitơ trong phân tử chiếm 30,4 % ngoài ra cứ 1,15 g Oxít này chiếm thể tích 0,28 lít (đktc). Xác định công thức của Oxít.
Bài 2 :
nNxOy = V/22,4 = 0,28/22,4 = 0,0125(mol)
MNxOy = m/n = 1,15/0,0125 = 92(g)
CÓ : %N = x. MN : Mhợp chất .100% = 30,4%
=> x . 14 : 92 = 0,304
=> x = 2
Có : MNxOy = 92 (g)
=> 2 .14 + y .16 = 92 => y =4
=> CTHH của oxit là N2O4
Đúng 0
Bình luận (0)
Bài 1 : H2 + Cl2 \(\rightarrow\) 2HCl
nH2 = V/22,4 = 10/22,4 = 0,446 (mol)
nCl2 = V/22,4 = 6,72/22,4 = 0,2(mol)
Lập tỉ lệ
\(\frac{n_{H2\left(ĐB\right)}}{n_{H2\left(PT\right)}}=\frac{0,446}{1}=0,446\) > \(\frac{n_{Cl2\left(ĐB\right)}}{n_{Cl2\left(PT\right)}}=\frac{0,3}{1}=0,3\)
=> Sau phản ứng : H2 dư và Cl2 hết
=> mCl2(thực tế) = n .M = 0,3 x 71 =21,3(g)
mà H = 60% => mCl2(phản ứng) = 21,3 x 60 % =12,78(g)
=> nCl2(phản ứng) = m/M = 12,78/71 = 0,18(mol)
Theo PT => nHCl = 2 . nCl2 = 2 x 0,18 = 0,36(mol)
=> mHCl(lý thuyết) = n .M = 0,36 x 36,5 = 13,14(mol)
mà mất mát 5%
=> mHCl(thu được) = 13,14 - 5% . 13,14 =12,483(g)
Đúng 1
Bình luận (0)
1) xác định công thức hóa học của nhôm oxit, biết tỉ lệ khối lượng của 2 nguyên tố nhôm và oxit bằng 9 : 8.2) Một oxít của lưu huỳnh trong đó có oxi chiếm 60 phần trăm về khối lượng. Tìm công thức phân tử của oxit đó?3) Cho 11,2 gam sắt vào 200 ml dung dịch H2SO4 2M. Hãy: a) Tính lượng khí H2 tạo ra ở đktc ? b) Chất nào còn dư sau phản ứng và lượng dư là bao nhiêu ? c) Tính nồng độ của các chất sau phản ứng ?
Đọc tiếp
1) xác định công thức hóa học của nhôm oxit, biết tỉ lệ khối lượng của 2 nguyên tố nhôm và oxit bằng 9 : 8.
2) Một oxít của lưu huỳnh trong đó có oxi chiếm 60 phần trăm về khối lượng. Tìm công thức phân tử của oxit đó?
3) Cho 11,2 gam sắt vào 200 ml dung dịch H2SO4 2M. Hãy:
a) Tính lượng khí H2 tạo ra ở đktc ?
b) Chất nào còn dư sau phản ứng và lượng dư là bao nhiêu ?
c) Tính nồng độ của các chất sau phản ứng ?
1.\(\dfrac{m_{Al}}{m_O}=\dfrac{9}{8}\)
\(Al_xO_y\)
\(x:y=\dfrac{9}{27}:\dfrac{8}{16}=\dfrac{1}{3}:\dfrac{1}{2}=2:3\)
Vậy CTHH là \(Al_2O_3\)
2.\(\rightarrow\%S=100-60=40\%\)
\(S_xO_y\)
\(x:y=\dfrac{40}{32}:\dfrac{60}{16}=1,25:3,75=1:3\)
Vậy CTHH là \(SO_3\)
3.
a.b.
\(n_{Fe}=\dfrac{11,2}{56}=0,2mol\)
\(n_{H_2SO_4}=2.0,2=0,4mol\)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
0,2 < 0,4 ( mol )
0,2 0,2 0,2 0,2 ( mol )
\(V_{H_2}=0,2.22,4=4,48l\)
Chất dư là H2SO4
\(m_{H_2SO_4\left(dư\right)}=\left(0,4-0,2\right).98=19,6g\)
c.Nồng độ gì bạn nhỉ?
Đúng 1
Bình luận (1)
. a. Hợp chất khí với hidro của R là: RH3. Trong oxít cao nhất R chiếm 43,66% về khối lượng. Tìm R.
b. Oxít cao nhất của nguyên tố R có dạng R2O3. Trong hiđroxít tương ứng, R chiếm 34,61% về khối lượng. Tìm R.
a.– Hóa trị cao nhất với oxi của nguyên tố = STT nhóm A.
– Hóa trị với H( nếu có) = 8 – hóa trị cao nhất với oxi.
=> Hóa trị cao nhất với oxi của nguyên tố R là 8-3=5
=> Công thức oxit cao nhất của R: R2O5
Ta có : \(\dfrac{2.R}{2.R+5.16}=43,66\%\\ \Rightarrow R=31\left(P\right)\)
Đúng 1
Bình luận (0)
b. Oxít cao nhất của nguyên tố R có dạng R2O3.
Hiđroxít tương ứng: R(OH)3
Ta có : \(\dfrac{R}{R+17.3}=34,61\%\\ \Rightarrow R=27\left(Al\right)\)
Đúng 2
Bình luận (0)
1 loại đồng oxít màu đen có khối lượng mol nguyên tử 80g/mol và 20%O
hãy tìm công thức hóa học của loại đồng oxít trên
CuxOy
\(\frac{16y}{80}\) .100% = 20% => y= 1
=> 64x + 16= 80 => x= 1
=> công thức CuO
Đúng 0
Bình luận (0)
16y/80*100%=20% ta duoc y=1
64x+16=80 ta duoc x=1
vay cong thuc hoa hoc CuO
Đúng 0
Bình luận (0)
Lấy 0,166 (g) một hợp chất A có chứa Nitơ, oxi hoá A hết bằng CuO được hỗn hợp khí gồm
C
O
2
,
H
2
O
,
N
2
. Cho nước hấp thụ hết trong
H
2
S
O
4
(khối lượng tăng 0,162(g)),
C
O...
Đọc tiếp
Lấy 0,166 (g) một hợp chất A có chứa Nitơ, oxi hoá A hết bằng CuO được hỗn hợp khí gồm C O 2 , H 2 O , N 2 . Cho nước hấp thụ hết trong H 2 S O 4 (khối lượng tăng 0,162(g)), C O 2 hấp thụ hết trong NaOH (khối lượng tăng 0,44 (g)). Khí N 2 chiếm thể tích 0,0224 lít (đktc). Biết tỉ khối của A đối với không khí bằng 2,862. Công thức phân tử A là:
A. C 4 H 9 N
B. C 5 H 9 N
C. C 3 H 7 N
D. Một kết quả khác
Hỗn hợp khí A chứa nitơ và hai hiđrocacbon kế tiếp nhau trong một dãy đồng đẳng. Khối lượng hỗn hợp A là 18,3 g và thể tích của nó là 11,2 lít. Trộn A với một lượng dư oxi rồi đốt cháy, thu được 11,7 gam
H
2
O
và 21,28 lít
C
O
2
. Các thể tích đo ở đktc.Hãy xác định công thức phân tử và phần trăm về khối lượng của từng hiđrocacbon trong hỗn hợp A.
Đọc tiếp
Hỗn hợp khí A chứa nitơ và hai hiđrocacbon kế tiếp nhau trong một dãy đồng đẳng. Khối lượng hỗn hợp A là 18,3 g và thể tích của nó là 11,2 lít. Trộn A với một lượng dư oxi rồi đốt cháy, thu được 11,7 gam H 2 O và 21,28 lít C O 2 . Các thể tích đo ở đktc.
Hãy xác định công thức phân tử và phần trăm về khối lượng của từng hiđrocacbon trong hỗn hợp A.
Số mol
C
O
2
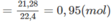
Khối lượng C trong A là: 0,95.12 = 11,4 (g).
Số mol
H
2
O
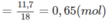
Khối lượng H trong A là: 0,65.2 = 1,3 (g).
Tổng khối lượng của C và H chính là tổng khối lượng 2 hiđrocacbon. Vậy, khối lượng N2 trong hỗn hợp A là : 18,30 - (11,4 + 1,3) = 5,6 (g)
Số mol
N
2
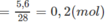
Số mol 2 hidrocacbon 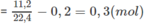
Đặt lượng C x H y là a mol, lượng C x + 1 H y + 2 là b mol :
a + b = 0,2 (1)
Số mol C = số mol C O 2 , do đó :
xa + (x + 1)b = 0,95 (2)
Số mol H = 2.số mol H 2 O , do đó :
ya + (y + 2)b = 2. 0,65= 1,3
Từ (2) ta có x(a + b) + b = 0,95 ⇒ b = 0,95 - 0,3x
Vì 0 < b < 0,3, nên 0 < 0,95 - 0,3x < 0,3
Từ đó tìm được 2,16 < x < 3,16 ⇒ x = 3.
⇒ b = 0,95 − 3.0,3 = 5. 10 - 2
⇒ a = 0,3 − 0,05 = 0,25
Thay giá trị tìm được của a và b vào (3), ta có y = 4.
% về khối lượng của C 3 H 4 trong hỗn hợp A:

% về khối lượng của C 4 H 6 trong hỗn hợp A :

Đúng 0
Bình luận (0)
Khử hoàn toàn 32g oxít sắt chưa rõ hóa trị trong khí CO thu được 22,4g chất rắn.Xác định công thức hóa học của oxít
Khử hoàn toàn 24 gam Oxit của một kim loại hóa trị II cần dùng hết 6,72 lít khí Hidro( đktc) ở nhiệt độ cao thu được kim loại và nước. Xác định kim loại, Công thức Oxit và gọi tên Oxít trên
Gọi CTHH oxit là RO
\(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH: RO + H2 --to--> R + H2O
0,3<-0,3
=> \(M_{RO}=\dfrac{24}{0,3}=80\left(g/mol\right)\)
=> MR = 64 (g/mol)
=> R là Cu
CTHH của oxit là CuO (đồng(II) oxit)
Đúng 2
Bình luận (0)
gọi cthh là R
nH2 = 6,72 : 22,4 = 0,3 (mol)
pthh : RO + H2 -t--> R +H2O
0,3<-0,3 (mol)
=> M Oxit = 24 : 0,3 = 80 (g/mol)
=> M R = 80 - 16 = 64 (g/mol )
=> R là Cu
=> CTHH của Oxit là CuO ( đồng (!!) Oxit)
Đúng 0
Bình luận (0)
Gọi công thức của oxit cần tìm là RO.
RO (0,3 mol) + H2 (0,3 mol) \(\underrightarrow{t^o}\) R + H2O.
Phân tử khối của oxit là 24/0,3=80 (g/mol).
Kim loại và công thức của oxit lần lượt là đồng (Cu) và CuO (đồng (II) oxit).
Đúng 0
Bình luận (0)
Xem thêm câu trả lời



























