Hỗn hợp A có H2 và 1 ankin , dA/H2=4.8, đun A có Ni hiệu suất 100% , tạo ra hh B không làm mất màu dd brom , dB/H2=8.CTPT và %V từng chất trong A và B

Những câu hỏi liên quan
Hỗn hợp A chứa H2 và anken X , dA/H2 = 6 , đun A có Ni đc hhB , không làm mất màu hh brom và dB/H2 = 8 .Xác định CTPT và % thể tích của từng chất trong hh A và hh B
Hỗn hợp khí A chứa H2 và 2 anken kế tiếp.Tỉ khối của A đv H2 là 8.26.Đun nóng nhẹ A có Ni đc hh khí B không làm mất màu dd brom và dB/H2 = 11.8 . Xác định CTPT và %V từng chất trong hh A và B
Gọi CTTQ của 2 anken là CnH2n
CnH2n + H2 --> CnH2n+2 (1)
MA = 16,52 (g/mol)
MB = 23,6 (g/mol)
Vì hh khí B ko làm mất màu Br2 => Anken hết sau pư (1)
Gọi n2anken =x(mol)
nH2 (bđ) =y(mol)
Theo (1) : nH2(pư)=nankan= nanken =x (mol)
=> nH2(dư)= y-x (mol)
Khi đó :
MA = \(\frac{14nx+2y}{x+y}=16,52\) (I)
MB= \(\frac{x\left(14n+2\right)+2\left(y-x\right)}{x+y-x}=23,6\) (II)
Từ (I,II) => y=7/3 x thế vào (I) => n=3,6
=> CTPT là C3H6 và C4H8
Đúng 0
Bình luận (0)
Hỗn hợp khí A chứa hiđro và một ankin. Tỉ khối của A đối với hiđro là 4,8. Đun nóng hỗn hợp A có mặt chất xúc tác Ni thì phản ứng xảy ra với hiệu suất được coi là 100%, tạo ra hỗn hợp khí B không làm mất màu nước brom và có tỉ khối đối với Hiđro là 8.Hãy xác định công thức phân tử và phần trăm về thể tích của từng chất trong hỗn hợp A và hỗn hợp B.
Đọc tiếp
Hỗn hợp khí A chứa hiđro và một ankin. Tỉ khối của A đối với hiđro là 4,8. Đun nóng hỗn hợp A có mặt chất xúc tác Ni thì phản ứng xảy ra với hiệu suất được coi là 100%, tạo ra hỗn hợp khí B không làm mất màu nước brom và có tỉ khối đối với Hiđro là 8.
Hãy xác định công thức phân tử và phần trăm về thể tích của từng chất trong hỗn hợp A và hỗn hợp B.
Giả sử trong 1 mol A có X mol C n H 2 n - 2 và (1 - x) mol H 2 . Khối lượng của 1 mol A là :
M A = (14n - 2)x + 2(1 - x) = 4,8.2 = 9,6 (g/mol) (1)
Khi đun nóng 1 mol A có mặt Ni, tất cả ankin đã biến hết thành ankan (vì B không tác dụng với nước brom) :
C n H 2 n - 2 + 2 H 2 → C n H 2 n + 2
x mol 2x mol x mol
Số mol khí còn lại trong B là (1 - 2x) mol nhưng khối lượng hỗn hợp B vẫn bằng khối lượng hỗn hợp A tức là bằng 9,6 g. Khối lượng của 1 mol B:
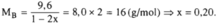
Thay x = 0,2 vào (1), tìm được n = 3.
Hỗn hợp A: C 3 H 4 chiếm 20%, H2 chiếm 80%.
Hỗn hợp B:
C
3
H
8
chiếm 
Vậy H 2 chiếm 67%.
Đúng 0
Bình luận (0)
Cho 11,424 lít (đktc) hỗn hợp khí X gồm H2 và hai h.c A,B mạch hở (B hơn A một ngtử cacbon) vào bình khí có sẵn bột Ni. Nung hỗn hợp X, sau một thời gian thu được hh Y gồm 6 h.c có tỉ khối hơi đối với H2 là 17,63a. Đốt cháy hoàn toàn hỗn hợp Y trong oxi dư thu được 14,112 lít (đktc) khí CO2 và 11,52 gam H2O. Xác định CTPT của 2 h.c A và B.b. HH Y làm mất màu tối đa V lít dd Br2 M và thoát ra 1,568 lít (đktc) hh khí Z. Tính V và tổng thể tích các khí A, B trong hh Y. Biết phản ứng xảy ra hoàn to...
Đọc tiếp
Cho 11,424 lít (đktc) hỗn hợp khí X gồm H2 và hai h.c A,B mạch hở (B hơn A một ngtử cacbon) vào bình khí có sẵn bột Ni. Nung hỗn hợp X, sau một thời gian thu được hh Y gồm 6 h.c có tỉ khối hơi đối với H2 là 17,63
a. Đốt cháy hoàn toàn hỗn hợp Y trong oxi dư thu được 14,112 lít (đktc) khí CO2 và 11,52 gam H2O. Xác định CTPT của 2 h.c A và B.
b. HH Y làm mất màu tối đa V lít dd Br2 M và thoát ra 1,568 lít (đktc) hh khí Z. Tính V và tổng thể tích các khí A, B trong hh Y. Biết phản ứng xảy ra hoàn toàn.
c. Viết các pt điều chế polietilen và etyl axetat từ chất A, các chất vô cơ cần thiết khác và đk xem như có đủ.
Hỗn hợp A gồm 0,3 mol C2H4 và 0,2 mol H2. Đun nóng hỗn hợp A có Ni làm xúc tác, thu được hỗn hợp B. Hỗn hợp B làm mất màu vừa đủ 2 lít dung dịch Br2 0,075M. Hiệu suất phản ứng giữa etilen và hiđro là: A. 75% B. 50% C. 100% D. Tất cả đều không đúng
Đọc tiếp
Hỗn hợp A gồm 0,3 mol C2H4 và 0,2 mol H2. Đun nóng hỗn hợp A có Ni làm xúc tác, thu được hỗn hợp B. Hỗn hợp B làm mất màu vừa đủ 2 lít dung dịch Br2 0,075M. Hiệu suất phản ứng giữa etilen và hiđro là:
A. 75%
B. 50%
C. 100%
D. Tất cả đều không đúng
Dẫn 13.44l A gồm H2 , 1 ankan và 1 anken qua Ni,to đc 10.08l hh khí B . Dẫn B qua bình nước brom thì màu của dd nhạt đi,khối lượng của bình tăng thêm 3.15g , còn lại 8.4l hh khí C ,dC/H2=17.8.(pư xảy ra hoàn toàn) Xđ CTPT và %Vtừng chất trong hh A ,B,C
Đun nóng hh A gồm 0,3 mol C2H4 và 0,2 mol H2 (Ni,t°) thu được hh B . Hỗn hợp B làm mất màu vừa đủ 2l đ Brom 0,075M. Tính hiệu suất PƯ giữa etilen và H2
C2H4+H2\(\rightarrow\)C2H6
- Nếu hiệu suất 100% thì dựa vào PTHH ta thấy H2 dư nên iệu suất tính theo H2
C2H4+Br2\(\rightarrow\)C2H4Br2
\(n_{Br_2}=2.0,075=0,15mol\)
\(n_{C_2H_4}=n_{Br_2}=0,15mol\)
Theo PTHH 1: \(n_{H_2}=n_{C_2H_4}=0,15mol\)
- Hiệu suất phản ứng: H=\(\dfrac{0,15}{0,2}.100=75\%\)
Đúng 1
Bình luận (0)
Hỗn hợp khí X chứa
H
2
và một hidrocacbon không no có 1 liên kết đôi. Tỉ khối của X đối với
H
2
là 9. Đun nóng nhẹ X có mặt xúc tác Ni thì nó biến thành hỗn hợp Y không làm mất màu nước brom và có tỉ khối đối với
H
2
là 15. Công thức phân tử của anken là? A.
C
H
4
B. ...
Đọc tiếp
Hỗn hợp khí X chứa H 2 và một hidrocacbon không no có 1 liên kết đôi. Tỉ khối của X đối với H 2 là 9. Đun nóng nhẹ X có mặt xúc tác Ni thì nó biến thành hỗn hợp Y không làm mất màu nước brom và có tỉ khối đối với H 2 là 15. Công thức phân tử của anken là?
A. C H 4
B. C 2 H 4
C. C 3 H 6
D. C 3 H 8
Hỗn hợp Y không làm mất màu nước Brom, suy ra Hidrocacbon không no phản ứng hết thành hidrocacbon no, H 2 còn dư.
Theo định luật bảo toàn khối lượng ta có:
m X = m Y
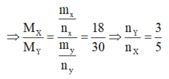
C n H 2 n + H 2 → C n H 2 n + 2
Giả sử số mol Y là 3 mol, số mol của X là 5 mol.
Khi đó số mol X giảm sau phản ứng chính là số mol H2 phản ứng và cũng là số mol của Hidrocacbon.
⇒ n X g i a m = 5-3 = 2 mol
⇒ n H 2 (bđ) = 5-2 = 3 mol
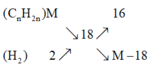
⇒ 16 M − 18 = 2 3 ⇒ M = 42 ⇒ 14 n = 42 ⇒ n = 3
Vậy CTPT của anken là C 3 H 6 .
⇒ Chọn C.
Đúng 0
Bình luận (0)
Hỗn hợp khí gồm H2 và anken có khả năng cộng HBr cho sản phẩm hữu cơ duy nhất. Tỉ khối của X so với H2 bằng 9,1. Đun nóng X có xúc tác Ni, sau khi phản ứng xảy ra hoàn toàn, thu được hỗn hợp khí Y không làm mất màu nước brom; tỉ khối của Y so với H2 bằng 13. Công thức cấu tạo của anken là: A. CH3-CH CH-CH3 B. CH2CH-CH2-CH3 C. CH2 C(CH3)2 D. CH2 CH2
Đọc tiếp
Hỗn hợp khí gồm H2 và anken có khả năng cộng HBr cho sản phẩm hữu cơ duy nhất. Tỉ khối của X so với H2 bằng 9,1. Đun nóng X có xúc tác Ni, sau khi phản ứng xảy ra hoàn toàn, thu được hỗn hợp khí Y không làm mất màu nước brom; tỉ khối của Y so với H2 bằng 13. Công thức cấu tạo của anken là:
A. CH3-CH = CH-CH3
B. CH2=CH-CH2-CH3
C. CH2 =C(CH3)2
D. CH2 =CH2
Đáp án A
Giả sử có 1 mol hỗn hợp X gồm H2 và anken ![]()
Ta có:
![]()
Áp dụng định luật bảo toàn khối lượng ta có:
![]()
![]()
Phương trình phản ứng:
![]()
Ta có: nX = 1 mol; nY = 0,7 mol
![]()
![]()
Ta có: anken đó là C4H8
X phản ứng với HBr cho 1 sản phẩm duy nhất nên X là But-2-en
Đúng 0
Bình luận (0)








