Tính % các nguyên tố trong các hợp chất sau :
1,H2SO4
2,CH3COOH
3,NH3
4,SO2
5,SO3
6,NH4 HO3
Xác định số oxi hóa của các nguyên tố trong các hợp chất, đơn chất và ion sau: MnO4-, SO42-, NH4+.
Tương tự số oxi hóa của Mn trong các chất
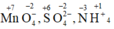
Tính phần trăm mỗi nguyên tố có trong các hợp chất: Al2O3, MgCl2, Na2S, (NH4)2CO3
tham khảo
- Xét phân tử Al2O3:
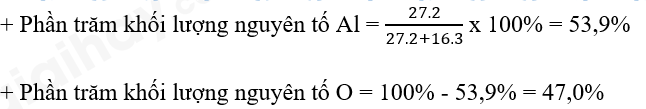
- Xét phân tử MgCl2:
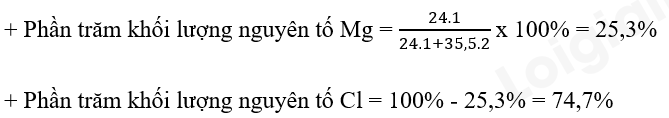
- Xét phân tử Na2S:

- Xét phân tử (NH4)2CO3:

Câu 1: Xác định số oxi hóa của các nguyên tố trong các phân tử và ion sau: CO2, H2O, SO3, NO, NO2, Na+, Cu2+, Fe2+, Fe3+, Al3+ , NH4+ Câu 2: Xác định số oxi hóa của các nguyên tố trong hợp chất , đơn chất và ion sau: a) H2S, S, H2SO3, H2SO¬4. b) HCl, HClO, NaClO2, HClO3. c) Mn, MnCl2, MnO2, KMnO4. d) MnO4- , SO42- , NH4+. Câu 3: Xác định số oxi hóa của Mn, Cr, Cl, P, S, C, Br : a) Trong phân tử KMnO4, Na2Cr2O7, KClO3, H3PO4 . b) Trong ion: NO3−, SO42−, CO32− , Br−, NH4+ .
O có số oxi hóa -2, H có số oxi hóa + 1
⇒ Số oxi hóa của các nguyên tố trong các phân tử và ion là:
CO2: x + 2.(-2) = 0 ⇒ x = 4 ⇒ C có số oxi hóa +4 trong CO2
H2O: H có số oxi hóa +1, O có số oxi hóa -2.
SO3: x + 3.(-2) = 0 ⇒ x = 6 ⇒ S có số oxi hóa +6 trong SO3
NH3: x + 3.1 = 0 ⇒ x = -3 ⇒ N có số oxi hóa -3 trong NH3
NO: x + 1.(-2) = 0 ⇒ x = 2 ⇒ N có số oxi hóa +2 trong NO
NO2: x + 2.(-2) = 0 ⇒ x = 4 ⇒ N có số oxi hóa +4 trong NO2
Cu2+ có số oxi hóa là +2.
Na+ có số oxi hóa là +1.
Fe2+ có số oxi hóa là +2.
Fe3+ có số oxi hóa là +3.
Al3+ có số oxi hóa là +3.
NH4+ có số õi hóa là -3
1/ a. Một loại phân đạm có công thức (NH4)2SO4 em hãy tính phần trăm theo khối lượng của các nguyên tố trong hợp chất ?
b/ Tính khối lượng nguyên tố dinh dưỡng N có trong 20kg phân đạm trên? (N= 14; H=1; S=32; O=16)
\(a.\%m_N=\dfrac{14.2}{\left(14+4.1\right).2+32+4.16}.100\approx21,212\%\\ \%m_H=\dfrac{4.2}{\left(14+4.1\right).2+32+4.16}.100\approx6,061\%\\ \%m_S=\dfrac{32}{\left(14+4.1\right).2+32+4.16}.100\approx24,242\%\\ \%m_O=\dfrac{4.16}{\left(14+4.1\right).2+32+4.16}.100\approx48,485\%\)
\(b.m_{N\left(20kg\right)}=20.\dfrac{2.14}{\left(14+4.1\right).2+32+4.16}.100\%\approx4,2424\left(kg\right)\)
(Mg = 24; C = 12; O = 16; Al = 27; N = 14; H = 1; P = 31; S = 32; Cu = 64; Fe = 56; )
Bài 1: Tính thành phần phần trăm (theo khối lượng) của các nguyên tố hóa học trong các hợp chất sau:
1) MgCO3 2) Al(OH)3 3) (NH4)2HPO4 4) C2H5COOCH3
Bài 2:
a,Chất nào có phần trăm khối lượng của nguyên tố sắt lớn nhất, nhỏ nhất trong các công thức hóa học sau: FeO; Fe2O3; FeS; FeS2.
b,Chất nào sau đây có phần trăm khối lượng oxi lớn nhất, nhỏ nhất: NO2; NO; N2O; N2O3.
c,Chất nào có phần trăm khối lượng của nguyên tố sắt lớn nhất, nhỏ nhất trong các công thức hóa học sau: AlCl3; Al2O3; AlBr3; Al2S3.
Bài 1:
\(1,M_{MgCO_3}=84(g/mol)\\ \begin{cases} \%_{Mg}=\dfrac{24}{84}.100\%=28,57\%\\ \%_{C}=\dfrac{12}{84}.100\%=14,29\%\\ \%_{O}=100\%-28,57\%-14,29\%=57,14\% \end{cases}\)
\(2,M_{Al(OH)_3}=78(g/mol)\\ \begin{cases} \%_{Al}=\dfrac{27}{78}.100\%=31,62\%\\ \%_{H}=\dfrac{3}{78}.100\%=3,85\%\\ \%_{O}=100\%-31,62\%-3,85\%=64,53\% \end{cases}\)
\(3,M_{(NH_4)_2HPO_4}=132(g/mol)\\ \begin{cases} \%_{N}=\dfrac{28}{132}.100\%=21,21\%\\ \%_{H}=\dfrac{9}{132}.100\%=6,82\%\\ \%_{P}=\dfrac{31}{132}.100\%=23,48\%\\ \%_{O}=100\%-23,48\%-6,82\%-21,21\%48,49\% \end{cases}\)
\(4,M_{C_2H_5COOCH_3}=88(g/mol)\\ \begin{cases} \%_{C}=\dfrac{48}{88}.100\%=54,55\%\\ \%_{H}=\dfrac{8}{88}.100\%=9,09\%\\ \%_{O}=100\%-9,09\%-54,55\%=36,36\% \end{cases}\)
Bài 2:
\(c,\%_{Al(AlCl_3)}=\dfrac{27}{27+35,5.3}.100\%=20,22\%\\ \%_{Al(Al_2O_3)}=\dfrac{27.2}{27.2+16.3}.100\%=52,94\%\\ \%_{Al(AlBr_3)}=\dfrac{27}{27+80.3}.100\%=10,11\%\\ \%_{Al(Al_2S_3)}=\dfrac{27.2}{27.2+32.3}.100\%=36\%\)
Vậy \(Al_2O_3\) có \(\%Al\) cao nhất và \(AlBr_3\) có \(\%Al\) nhỏ nhất
Bài 2:
\(a,\%_{Fe(FeO)}=\dfrac{56}{56+16}.100\%=77,78\%\\ \%_{Fe(Fe_2O_3)}=\dfrac{56.2}{56.2+16.3}.100\%=70\%\\ \%_{Fe(FeS)}=\dfrac{56}{56+32}.100\%=63,64\%\\ \%_{Fe(FeS_2)}=\dfrac{56}{56+32.2}=46,67\%\)
Vậy \(FeO\) có \(\%Fe\) lớn nhất và \(FeS_2\) có \(\%Fe\) thấp nhất
\(b,\%_{O(NO_2)}=\dfrac{16}{16.2+14}.100\%=69,57\%\\ \%_{O(NO)}=\dfrac{16}{16+14}.100\%=53,33\%\\ \%_{O(N_2O)}=\dfrac{16}{14.2+16}.100\%=36,36\%\\ \%_{O(N_2O_3)}=\dfrac{16.3}{14.2+16.3}.100\%=63,16\%\)
Vậy \(NO_2\) có \(\%O\) lớn nhất và \(N_2O\) có \(\%O\) nhỏ nhất
1)cho các CTHH sau. Tính % khối lượng mỗi nguyên tố đó: a)CaCO3. b)H2SO4. C)Al2S3. d)CuO. e)Fe2(SO4)3
2)trong các chất sau,chất nào có hàm lượng N cao nhất: NH4NO3. NH4CL. (NH4)2SO4. (NH4)3PO4
3)trong các chất sau chất nào có hàm lượng K cao nhất: K3PO4 KCL KNO3 K2SO4 KHSO3
4)Trong các chất sau, chất nào giầu Oxi hơn: H2O. H2O2. CO Co2 SO3 P2O5
5)cho các CTHH sau, tính % khối lượng mỗi nguyên tố: a)Na2SO3 b)K2PO4 c)Fe2(so4)3 d) Fe(NO3)2
6)tính % khối lượng mỗi nguyên tố trong các CTHH sau: a)C2H5O2N. b)C3H7O2CL. c)K2HPO4. d)Ba(HSO4)2
Bài này khá dài nè, em đăng tách ra nha ^^
So sánh tính axit của các chất sau
1 CH 2 Cl - CH 2 COOH 2 CH 3 COOH 3 HCOOH 4 CH 3 - CHCl - COOH
A. (3) > (2) > (1) > (4)
B. (4) > (2) > (1) > (3)
C. (4) > (1) > (3) > (2)
D. (4) > (1) > (2) > (3)
Đáp án C
tính axit của các chất là: (4) > (1) > (3) > (2)
Bài 1: Tính thành phần phần trăm theo khối lượng của các nguyên tố trong hợp chất
sau: (NH4)2SO4.
\(M_{\left(NH_4\right)_2SO_4}=\left(14+1.4\right).2+32+16.4=132\left(\dfrac{g}{mol}\right)\)
\(\%N=\dfrac{14.2}{132}.100\%=21,2\%\)
\(\%H=\dfrac{1.4.2}{132}.100\%=6\%\)
\(\%S=\dfrac{32}{132}.100\%=24,2\%\)
\(\%O=\dfrac{16.4}{132}.100\%=48,5\%\)