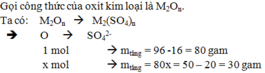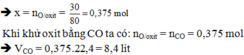để khử hoàn toàn a gam một oxit kim loại AxOy phải cần 6,72 lít CO (đktc), sau PƯ thu được 11,2 gam kim loại A. Hãy lập PTHH dạng tổng quát và tìm giá trị a của oxit kim loại trên?

Những câu hỏi liên quan
để khử hoàn toàn a gam một oxit kim loại AxOy phải cần 6,72 lít co (đktc) sau phản ứng thu được 11,2 gam kim loại A . hãy lập pthh dạng tổng quát và tìm giá trị của A hãy lập pthh dạng tổng quát và tìm giá trị a của oxit kim loại trên
Để khử hoàn toàn a gam một ooxit kim loại AxOy phải cần 6,72 lít CO (ĐKTC). Sau phản ứng thu được 11,2 gam kim loại A tính giá trị a
\(A_xO_y+yCO\) ➜ \(xA+yCO_2\)
\(n_{CO}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
⇒ \(m_{CO}=0,3.28=8,4\left(g\right)\)
Theo PT: \(n_{CO_2}=n_{CO}=0,3\left(mol\right)\)
⇒ \(m_{CO_2}=0,3.44=13,2\left(g\right)\)
Áp dụng ĐL BTKL ta có:
\(m_{A_xO_y}+m_{CO}=m_A+m_{CO_2}\)
⇒ \(m_{A_xO_y}=m_A+m_{CO_2}-m_{CO}=11,2+13,2-8,4=16\left(g\right)=a\)
Vậy giá trị của a là 16
Đúng 0
Bình luận (1)
Khử hoàn toàn 24 gam Oxit của một kim loại hóa trị II cần dùng hết 6,72 lít khí Hidro( đktc) ở nhiệt độ cao thu được kim loại và nước. Xác định kim loại, Công thức Oxit và gọi tên Oxít trên
Gọi CTHH oxit là RO
\(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH: RO + H2 --to--> R + H2O
0,3<-0,3
=> \(M_{RO}=\dfrac{24}{0,3}=80\left(g/mol\right)\)
=> MR = 64 (g/mol)
=> R là Cu
CTHH của oxit là CuO (đồng(II) oxit)
Đúng 2
Bình luận (0)
gọi cthh là R
nH2 = 6,72 : 22,4 = 0,3 (mol)
pthh : RO + H2 -t--> R +H2O
0,3<-0,3 (mol)
=> M Oxit = 24 : 0,3 = 80 (g/mol)
=> M R = 80 - 16 = 64 (g/mol )
=> R là Cu
=> CTHH của Oxit là CuO ( đồng (!!) Oxit)
Đúng 0
Bình luận (0)
Gọi công thức của oxit cần tìm là RO.
RO (0,3 mol) + H2 (0,3 mol) \(\underrightarrow{t^o}\) R + H2O.
Phân tử khối của oxit là 24/0,3=80 (g/mol).
Kim loại và công thức của oxit lần lượt là đồng (Cu) và CuO (đồng (II) oxit).
Đúng 0
Bình luận (0)
Xem thêm câu trả lời
Hoà tan hoàn toàn 20,0 gam một oxit kim loại bằng dung dịch
H
2
S
O
4
loãng thu được 50,0 gam muối. Khử hoàn toàn lượng oxit đó thành kim loại ở nhiệt độ cao cần V lít khí CO (đktc). Giá trị của V là A. 2,80 lít. B. 5,60 lít C. 6,72 lít D. 8,40 lít
Đọc tiếp
Hoà tan hoàn toàn 20,0 gam một oxit kim loại bằng dung dịch H 2 S O 4 loãng thu được 50,0 gam muối. Khử hoàn toàn lượng oxit đó thành kim loại ở nhiệt độ cao cần V lít khí CO (đktc). Giá trị của V là
A. 2,80 lít.
B. 5,60 lít
C. 6,72 lít
D. 8,40 lít
Gọi oxit kim loại cần tìm là M 2 O n .
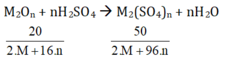
Ta có:
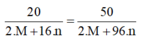
⇒ 40M + 1920.n = 100M + 800n
⇒ 1120n = 60M

Vậy M là Fe, oxit là F e 2 O 3 .
F e 2 O 3 + 3CO → 2Fe + 3 C O 2
⇒ nCO = 3 n F e 2 O 3
= 3.20/160 = 0,375 mol
⇒ VCO = 0,375.22,4 = 8,4 lit
⇒ Chọn D.
Đúng 1
Bình luận (0)
để khử hoàn toán 34,4 g hh gồm kim loại a và oxit của nó axoy người ta cần dùng hết 8,96 l h2 đktc toàn bộ lượng kim loại thu đc sau phản ứng được hòa tan hoàn toàn bằng dung dịch hcl dư thấy thoát ra 11,2 l h2 đktc tìm kim loại a
Hoà tan hoàn toàn 20 gam một oxit kim loại bằng dung dịch H 2 SO 4 loãng thu được 50 gam muối. Khử hoàn toàn lượng oxit đó thành kim loại ở nhiệt độ cao cần V lít khí CO (đktc). Giá trị của V là
A. 2,80
B. 5,60
C. 6,72
D. 8,40

Vậy n = 3, R = 56 thỏa mãn, oxit là F e 2 O 3
n F e 2 O 3 = 20 160 = 0,125 m o l
m m u o i = m F e S O 4 + m F e 2 ( S O 4 ) 3
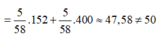
![]()
Đáp án: D
Đúng 0
Bình luận (0)
Hoà tan hoàn toàn 20 gam một oxit kim loại bằng dung dịch H 2 S O 4 loãng thu được 50 gam muối. Khử hoàn toàn lượng oxit đó thành kim loại ở nhiệt độ cao cần V lít khí CO (đktc). Giá trị của V là
A. 2,80 lít
B. 5,60 lít
C. 6,72 lít
D. 8,40 lít
Hoà tan hoàn toàn 20,0 gam một oxit kim loại bằng dung dịch H2SO4 loãng thu được 50,0 gam muối. Khử hoàn toàn lượng oxit đó thành kim loại ở nhiệt độ cao cần V lít khí CO (đktc). Giá trị của V là: A. 2,80 lít. B. 5,60 lít. C. 6,72 lít. D. 8,40 lít.
Đọc tiếp
Hoà tan hoàn toàn 20,0 gam một oxit kim loại bằng dung dịch H2SO4 loãng thu được 50,0 gam muối. Khử hoàn toàn lượng oxit đó thành kim loại ở nhiệt độ cao cần V lít khí CO (đktc). Giá trị của V là:
A. 2,80 lít.
B. 5,60 lít.
C. 6,72 lít.
D. 8,40 lít.
Khử hoàn toàn 17,4 gam một oxit kim loại cần dùng 6,72 lít khí H2 (ở đktc) sau phản ứng thu được chất rắn A. Hòa tan hoàn toàn chất rắn A vào axit clohiđric dư thấy có 16,425 gam axit tham gia phản ứng. Xác định công thức phân tử của oxit kim loại