Bài 1:
a) Ta có: \(m_{NaCl}=30\cdot20\%=6\left(g\right)\) \(\Rightarrow C\%_{NaCl}=\dfrac{6}{30+50}\cdot100\%=7,5\%\)
b) Ta có: \(m_{NaCl}=30\cdot20\%+70\cdot10\%=13\left(g\right)\) \(\Rightarrow C\%_{NaCl}=\dfrac{13}{30+70}\cdot100\%=13\%\)
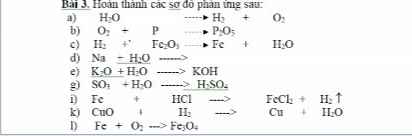
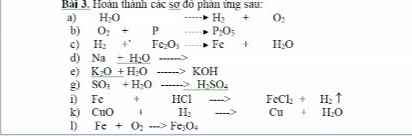
Bài 3:
Ta có: \(Na+H_2O\rightarrow NaOH+\dfrac{1}{2}H_2\uparrow\)
\(Na_2O+H_2O\rightarrow2NaOH\)
Ta có: \(\left\{{}\begin{matrix}n_{Na}=\dfrac{6,9}{23}=0,3\left(mol\right)\\n_{Na_2O}=\dfrac{9,3}{62}=0,15\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}n_{NaOH}=0,6\left(mol\right)\\n_{H_2}=0,15\left(mol\right)\end{matrix}\right.\)
Mặt khác: \(m_{dd}=6,9+9,3+284,1-0,15\cdot2=300\left(g\right)\)
Gọi số gam NaOH cần thêm là a (gam)
\(\Rightarrow\dfrac{0,6\cdot40+a}{300+a}=0,15\) \(\Leftrightarrow a=24,7\left(g\right)\)
Bài 1:
a) mNaCl= 20%. 30=6(g)
mddNaCl(sau)= 30+50=80(g)
=>C%ddNaCl(sau)= (6/80).100= 7,5%
b) mddNaCl(sau)=30+70=100(g)
mNaCl(tổng)= 20%.30 + 70.10%= 13(g)
=>C%ddNaCl(sau)= (13/100).100=13%
Bài 2:
KL dd KOH ban đầu là x(g) (x>0)
=> KL dd KOH sau là (x-100) (g)
Ta có hpt:
\(10\%x=25\%.\left(x-100\right)\\ \Leftrightarrow x=\dfrac{1000}{6}\left(g\right)\)
Vậy : KL dd KOH ban đầu là 1000/6 (g) (Tức khoảng 166,667 gam)
Bài 3:
nNa=0,3(mol); nNa2O= 0,15(mol)
PTHH; Na + H2O -> NaOH + 1/2 H2
0,3_____________0,3____0,15(mol)
Na2O + H2O -> 2 NaOH
0,15_________0,3(mol)
mddNaOH(sau p.ứ)= mNa + mNa2O + mH2O - mH2= 6,9+9,3+284,1 - 0,15.2=300(g)
mNaOH(sau p.ứ)= (0,3+0,3).23= 13,8(g)
Gọi KL NaOH lấy thêm là x (g) (x>0)
Vì sau khi trộn thêm NaOH vào ta được dd NaOH 15% nên ta có pt:
\(\dfrac{13,8+x}{300+x}.100\%=15\%\\ \Leftrightarrow x\approx30,706\left(g\right)\)
=> KL NaOH lấy thêm khoảng 30,706(g)
Bài 4:
mH2O= 50,1(g)
=> mddNa2CO3=12,42+50,1= 62,52(g)
mNa2CO3= (106/286).12,42=4,603(g)
=> C%ddNa2CO3= (4,603/62,52).100=7,362%